发布日期:2018-10-06 10:17 来源:活性炭网 作者:活性炭网 浏览数:
制备具有不同化学特性的花生壳衍生的活性炭(ACPNS),其适于在水溶液中除去灭多威农药。 蒸汽活性炭是在氮气存在下,在973-1373K的温度范围内从碳化花生壳中获得的。 使用NaOH和Z
制备具有不同化学特性的花生壳衍生的活性炭(ACPNS),其适于在水溶液中除去灭多威农药。蒸汽活性炭是在氮气存在下,在973-1373K的温度范围内从碳化花生壳中获得的。使用NaOH和ZnCl 2进一步化学活化碳化花生壳。通过77K的N2吸附,扫描电子显微镜和FTIR表征ACPNS的结构。BET方法用于推导有效表面积。使用批量实验研究影响花生壳衍生的活性炭对从水溶液中去除灭多威的吸附能力的参数(例如初始pH,温度等)。对包括伪一阶和伪二阶的动力学模型进行了研究。研究了吸附等温线。平衡吸附数据符合Langmuir吸附等温线,R2> 0.9980。计算花生壳衍生的活性炭去除灭多威的最大吸附容量。计算了ACPNS上灭多威吸附过程的热力学参数ΔG°,ΔH°和ΔS°,ΔG°的负值表明吸附的自发性。制备的花生壳衍生活性炭成功应用于从不同水样中去除灭多威农药,回收率> 95,RSD <3%。提出了吸附机理。平衡吸附数据符合Langmuir吸附等温线,R2> 0.9980。计算花生壳衍生的活性炭去除灭多威的最大吸附容量。计算了ACPNS上灭多威吸附过程的热力学参数ΔG°,ΔH°和ΔS°,ΔG°的负值表明吸附的自发性。制备的花生壳衍生活性炭成功应用于从不同水样中去除灭多威农药,回收率> 95,RSD <3%。提出了吸附机理。平衡吸附数据符合Langmuir吸附等温线,R2> 0.9980。计算花生壳衍生的活性炭去除灭多威的最大吸附容量。计算了ACPNS上灭多威吸附过程的热力学参数ΔG°,ΔH°和ΔS°,ΔG°的负值表明吸附的自发性。制备的花生壳衍生活性炭成功应用于从不同水样中去除灭多威农药,回收率> 95,RSD <3%。提出了吸附机理。计算了ACPNS上灭多威吸附过程的热力学参数ΔG°,ΔH°和ΔS°,ΔG°的负值表明吸附的自发性。制备的花生壳衍生活性炭成功应用于从不同水样中去除灭多威农药,回收率> 95,RSD <3%。提出了吸附机理。计算了ACPNS上灭多威吸附过程的热力学参数ΔG°,ΔH°和ΔS°,ΔG°的负值表明吸附的自发性。制备的花生壳衍生活性炭成功应用于从不同水样中去除灭多威农药,回收率> 95,RSD <3%。提出了吸附机理。
关键词:灭多威; 农药; 花生壳; 活性炭; 吸附
地下水和地表水的污染被认为是威胁人类,动物,植物和水生生物的最重要问题。水污染的一个常见原因是使用最近用于农业的杀虫剂杀死昆虫,细菌,真菌和以作物为食的其他东西。
农药是化学和人工合成的化合物,它被认为是有毒的生物累积剂[ 1 ]。有几种不同类型的农药,如除草剂,杀虫剂,杀线虫剂和杀菌剂。农药的毒性变化很大,对生命系统和环境有潜在危害。农药具有皮肤,口腔和呼吸道接触的有害影响。这些影响包括致癌性,肝损伤,致畸性,致癌性,生殖障碍,致突变性,神经损伤和过敏原致敏。因此,农药具有有害作用,对地表水和地下水源构成威胁。这种污染主要通过工业废水排放,浸出,地表径流和空中应用沉积[ 3 ]。根据欧盟饮用水卫生指令和规定,允许的最大农药总浓度为0.1μg/ L 。根据化学结构,灭多威是不同类型的农药之一。它是一种剧毒的氨基甲酸酯杀虫剂,最初于1968年由美国环保署注册为“限用农药 ”,用于各种作物。它是一种胆碱酯酶抑制剂,通常对抗已经产生抗药性的害虫最有效有机磷酸盐 。它在水中迅速溶解,不会在土壤中持久存在。灭多威的有害作用,因为它通过口腔接触通过皮肤或肺部吸收[ 6 ]。口服吸收和中等毒性皮吸收时,当它是高毒性和其慢性效果与它的急性效果。灭多威对鱼类,水生无脊椎动物,鸟类和哺乳动物具有高毒性[ 9 ]。对于相对高剂量的人来说,它可能是致命的。由于其有害作用和有毒污染,因此从水供应和水净化中除去有不同的技术。一些技术包括好氧降解,光催化降解。超声结合光 - 芬顿治疗[ 12 ],电透析膜[ 13 ],过滤,臭氧化,与自由基等氧化剂反应,消毒,浮选[ 15 ],预浓缩[ 16 ]和吸附[ 17 ]。在这些技术中,吸附被认为是最有效和广泛使用的用于味道和气味控制以及去除合成有机化合物和从废水和供水[广泛的污染物。在水净化中使用吸附技术有许多优点。它是低成本,简单和简单的系统。通过吸附过程处理后没有副产物的形成,并且没有或更少地产生有毒物质。如今,有许多不同的吸附剂可用于水处理和净化,如硅胶[ 20 ],活性氧化铝[ 21 ],沸石,聚合物和树脂,粘土和活化碳。
花生壳衍生的活性炭很少用于从水溶液中[去除有机污染物的27,28 ]。
据我们所知,没有关于使用花生壳衍生的活性炭从水溶液中去除灭多威农药的报道数据。
本研究的目的是花生壳衍生活性炭(ACPNS)的制备,表征和改性。花生是一种在埃及广泛培养的油料植物。花生壳成本低,被认为是环境中的废物。花生壳通过蒸汽物理改性,并使用NaOH和ZnCl2进行化学改性。彻底研究了改性花生壳衍生的活性炭,用于从水溶液中除去灭多威农药。研究了影响灭多威去除的不同实验因素。研究了农药初始浓度,接触时间,活性炭用量和温度对花生壳活性炭对灭多威吸附容量的影响。此外,建立动力学和热力学研究以期望吸附行为。
试剂和解决方案
灭多威(方案1)购自Kafr El-Zayat Pesticides&Chemicals Company,Kafr El Zayat,Gharbia,Egypt。通过将1g溶解在1L蒸馏水中制备1000ppm灭多威的储备溶液。花生壳是从埃及当地市场获得的。NaOH,ZnCl 2和HCl购自Sigma-Aldrich。
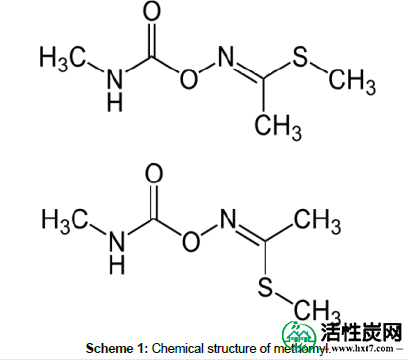
方案1:灭多威的化学结构。
仪器
使用pH计(Hi 931401,HANNA,Portugal)进行pH测量。使用UV-Vis分光光度计(Chrom Tech-Co.,Ltd.,USA)分析灭多威的浓度。使用分析天平称量吸附剂。水浴振荡器用于吸附实验。
将花生壳压碎,用0.5%HCl洗涤以除去所有污垢,在378K的烘箱中干燥过夜,用研磨机研磨,筛分至1-4mm的筛目尺寸并在平板炉中在873K下碳化2小时。
将碳化材料浸泡在氢氧化钠(NaOH)溶液中,其中两种浸渍比为char:NaOH(w / w)等于1:1(CN11)和1:3(CN13)24小时。然后将两种混合物在烘箱中在378K下脱水过夜以除去水分,然后在1023K下活化2小时。冷却后,用蒸馏水洗涤所得的AC数次,直到滤液的pH达到(7-8)。然后在378K的烘箱中将AC干燥过夜。
通过将干燥的花生壳浸泡在氯化锌中,以两种浸渍比例即制备氯化锌活性炭样品。碳化花生壳:ZnCl 2(w / w)等于2:1(CZ21)和1:2(CZ12)。将两种混合物在378K的烘箱中干燥过夜以除去水分,然后在873K下活化2小时。然后,用蒸馏水洗涤AC数次,直至从氯离子中滤出。然后将两个样品在378K的烘箱中干燥过夜。
用不同时间的蒸汽流量等于150ml / min活化碳化花生壳,以获得活性炭样品(CS20和CS48)的20%和48%燃尽。
吸附剂的表征
使用表面积和尺寸分析仪(QUANTACHROME-NOVA 2000系列)在77K下通过氮气吸附进行碳的BET表面积(S BET)测量。通过使用扫描电子显微镜JSE-T20(JEOL,日本)拍摄碳的表面显微照片。该仪器的功率为40千瓦。在分析之前,将样品在383K下干燥4小时。在样品上涂覆一层薄薄的金,用于样品金属化和电荷耗散。
傅里叶变换红外光谱(FT-IR)技术用于定性测量存在于活性炭表面上的官能团。通过使用吉之仪器(型号6100,日本),通过在玛瑙研钵中混合1毫克500毫克溴化钾(Merck)上的样品制备的样品盘和在扫描范围从4000至400 厘米-1。
应用表面酸度和Boehm滴定技术,通过用各种强度的碱中和来测定碳表面上官能团的类型和数量。
吸附实验
通过在250ml锥形瓶中摇动0.02g活性炭和50ml灭多威水溶液进行分批吸附实验,所述锥形瓶置于不同浓度(100至1600mg / l)的温控摇床水浴中,pH值(2)之间12),离子强度(在0.002和0.09摩尔/升之间),温度(在289和313K之间)和吸附剂剂量(在0.01和0.02g之间),在125rpm的恒定摇动速率下。吸附剂去除的农药量(qe)Eqn(1)和去除的百分比(R%)Eqn(2):
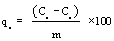 (1)
(1)
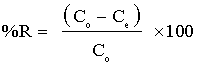 (2)
(2)
其中q e是吸附的农药量(mg / g)。C o和C e分别是农药的初始和平衡液相浓度(mg / g)。V是溶液(L)的体积,m是所用吸附剂(g)的重量。
吸附剂的表征
纹理属性
氮吸附-解吸分析:碳的表面积和孔隙率是决定其吸附容量[突出因素29,30 ]。固体的结构性质通常是由下述的氮气的吸附在77K测定和吸附数据通常是由BET方程[应用分析31,32 ]。
所研究的碳对氮的吸附发现相对较快,在25分钟内达到平衡,表明吸附不受超细孔中遇到的活化扩散控制,同时指整个孔结构对氮分子的可接近性[ 33 ]。图1描绘了在77K下测量的碳C,CS20,CS48,CZ21,CZ12,CN11和CN13的氮吸附等温线。
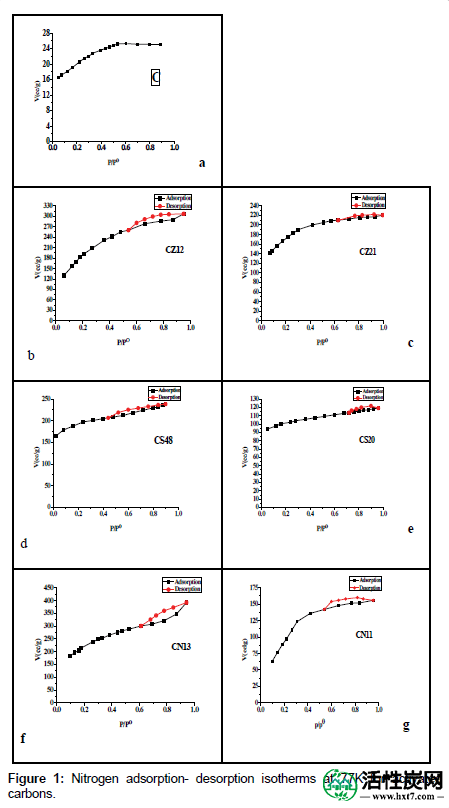
图1:活性炭在77K下的氮吸附 - 解吸等温线。
对于碳C,根据BDDT分类,等温线主要是I型,没有磁滞回线[ 34 ]。ACPNS的等温线显示出I型和IV型的混合特征; 它们不那么陡峭并且表现出闭合的磁滞回线。
ACPNS样品的表面积值由77K 下N 2吸附的线性BET曲线计算。结果如表1所示:
| 样品 | SBET(m 2 / g) | VT(毫升/克) | R(nm)的 |
|---|---|---|---|
| C | 66.640 | 0.039 | 1.167 |
| CS20 | 801.550 | 0.189 | 1.272 |
| CS48 | 1449.002 | 0.342 | 1.493 |
| CZ21 | 1270.030 | 0.336 | 1.464 |
| 十二生肖 | 1783.520 | 0.476 | 1.533 |
| CN11 | 1242.860 | 0.242 | 1.389 |
| CN13 | 2362.850 | 0.608 | 1.655 |
表1: N 2吸附和表面积数据。
(i)由于活化剂NaOH,ZnCl 2或蒸汽的吸收,与活性炭相比,非活性炭的表面积非常低。CN13的SBET是C的35.5倍,而CS48是C的20.8倍,CZ12是C的26.8倍。
(ii)NaOH活性炭(CN13)样品具有比其他ACPNS更高的表面积值。
(iii)当炭:NaOH比率从(1:1)增加到(1:3)时,由于浸渍比增加,CN13 的S BET值从1242.86m 2 / g增加到2362.85m 2 / g。
(iv)随着前体:ZnCl2从(1:2)增加到(2:1)的比例增加,ZnCl2的浸渍率导致S BET值从1449.03m 2 / g增加到1783.52m 2 / g,这是分别设计为CZ12和CZ21样品。
(v)蒸汽活性炭的S BET从801. 55 m 2 / g增加到1388.00 m 2 / g,分别增加CS20和CS48样品的燃烧程度。
vi)未活化样品的总孔体积与活化样品相比非常低,并且(ml / L)随着活化和活化剂%的增加而增加。
(vii)活化样品的孔半径范围在0.389和0.514nm之间。
扫描电子显微镜(SEM):扫描电子显微镜图像可以了解花生壳结构的形状。暗区是大孔,浅灰区是由碳基质引起的。图2表示分别通过物理(CS)和化学(CN11,CN13,CZ12,CZ21)活化方法制备的所得活性炭的形态。可以清楚地看到,物理和化学活化在活化后表现出颗粒表面的一些变化。观察到由物理(使用蒸汽作为活化剂)或化学(使用NaOH或ZnCl 2)活化制备的活性炭的不同孔结构,这取决于不同的反应机理。图2图4描绘了四个图片(a)碳质前体,(b)使用NaOH的化学活性炭,(c)使用ZnCl 2和(d)物理活性炭(CS)化学活化。在这个问题中,由蒸汽激活的样品(d)表明碳基质大于暗区。这是指由活化蒸汽产生的微孔的性质。在化学活化中使用NaOH或ZnCl 2作为活化剂,暗区大于碳基质。这意味着样品(b,c)的较高表面积是由于中孔和微孔造成的。

图2:(a)碳质前体(1000x),(b)活性炭与NaOH(500x),(c)活性炭与ZnCL2(500x)和(d)蒸汽活性炭(1000x)的SEM。
而且,这表明由NaOH和ZnCl 2活化的花生壳具有不规则的碳基质。即,具有不同的形状和大小。这通过活化花生壳的氮吸附等温线证明,这表明它们主要仅在物理活化中是微孔,在化学活化中是微孔和中孔的混合物。这可以通过使用如图2所示的NaOH和ZnCl 2溶液的母体细胞结构表面的逐渐变化来解释。。纤维素单元通过所使用的化学品水解或脱水,因此细胞间壁的主要组分被分解成更小的结构。因此很明显,花生壳的外表面非常粗糙,由空腔,裂缝和不规则突起组成。
化学性质:碳的表面化学在确定其对水溶液中害虫的吸附能力方面比其质地特性更重要,特别是当吸附涉及通过离子交换和/或复合物形成与表面官能团相互作用时可能是活性炭吸附害虫的情况。
FTIR:碳表面的化学性质归因于表面存在酸性或碱性的碳 - 氧官能团。记录了样品ACPNS的FTIR光谱(吸附灭多威之前和之后),图3。记录的CZ21,CN11和CS20的IR光谱(在灭多威之前)表明:在(3414-3446)cm -1附近存在宽带,这归因于由于存在游离羟基而引起的OH伸缩振动,键合OH的羧酸和吸附的水带[ 35,36 ]。观察周围的峰(1034年至1116年)厘米-1归因于CO组中的羧酸和醇基[35- 38]。观察周围的峰(610-875)厘米-1归因于进出在苯衍生物[平面环的变形35,38,39 ]。
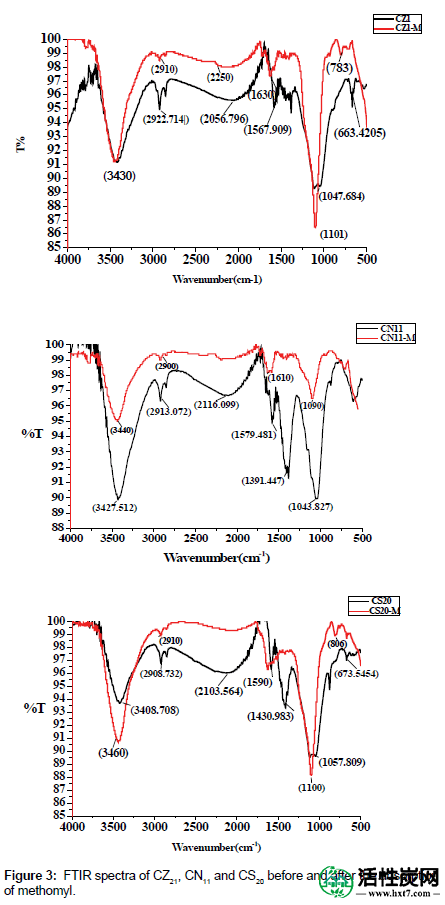
图3:在灭多威吸附之前和之后CZ21,CN11和CS20的FTIR光谱。
吸附灭多威后ACPNS的FTIR光谱显示以下变化:
在CZ21-M:一个峰在1630厘米外观-1由于NH弯表示伯胺[存在40在1101厘米]和峰的外观-1由于CO伸缩由于醇,羧酸的存在,酯类和醚类[ 37 ]。
对于CN11-M:峰在2116厘米消失-1和峰在1391厘米-1。这表明不存在-C≡C-伸展的炔基并且分别没有芳环的CC伸展(环内)。
最后,CS 20 -M图显示峰的消失在2103厘米-1,1430厘米-1和1057厘米-1表明不存在-C≡C-拉伸炔基的,不存在的CC拉伸(IN-环)的芳环和CH链段分别为脂族胺。此外,由于CO伸展,新的峰出现在1100 cm -1处,这表明存在醇,羧酸,酯或胺基团[ 41 ]。
表面酸度和Boehm滴定:碳材料的含水浆料的pH提供了所研究的AC的化学参数的类型和浓度的方便指示。表2显示(i)碳C的表面pH为(7.9),表明其表面碱性,即非氧化碳表面上的碱性官能团与酸型相比更具主导性。对于表面pH = 8.2和8.3的蒸汽活化的ACPNS也是如此。在1223K处的蒸汽活化通常导致在基本特征的CO基团的碳表面上形成[ 42 ]。用NaOH(CN11,CN12)处理使CN11和CN12的表面pH分别从7.98增加到8.77和8.90。另一方面,用ZnCl处理2总酸度从7.98增加到6.66。
由于碱性官能团的影响,活化样品的ACPNS的零点电荷pH pzc的pH范围在7.0和8.8之间。
表面酸性基团可以通过用一系列不同强度的碱进行选择性中和来确定(m.eq / g),即。NaHCO 3,Na 2 CO 3,NaOH和NaOC 2 H 5。NaHCO 3中和羧基,其中被Na 2 CO 3中和但不被NaHCO 3中和的是内酯。由NaOH中而不是由Na 2 CO 3中和的弱酸基团被假定为酚。与NaOC 2 H 5反应但不与NaOH反应的基团被认为是羰基[ 43 ]。表2 表明了非活化和活性炭样品表面的酸性和不同酸性基团的丰度。
| 样品 | 贝姆 | 滴定 | pHPCZ | 上清液的pH值 | 失败 | 灰分含量 | |
|---|---|---|---|---|---|---|---|
| 羧酸(meq / g) | 酚醛(meq / g) | 乳酸(meq / g) | 干燥% | % | |||
| P | 0.018 | 0.042 | 0.638 | 6.00 | 5.10 | 5.60 | 1.22 |
| C | 0.020 | 0.002 | 0.474 | 8.00 | 7.98 | 4.01 | 2.57 |
| CH | 0.482 | 0.096 | 0.916 | 3.00 | 2.18 | 2.31 | 0.42 |
| CS20 | 0.010 | 0.115 | 0.147 | 8.00 | 8.20 | 3.71 | 4.16 |
| CS48 | 0.001 | 0.112 | 0.089 | 8.20 | 8.30 | 3.44 | 7.62 |
| 十二生肖 | 0.034 | 0.012 | 0.418 | 7.00 | 6.57 | 3.95 | 0.90 |
| CZ21 | 0.074 | 0.014 | 0.288 | 7.20 | 6.66 | 5.48 | 1.00 |
| CN11 | 0.000 | 0.081 | 0.115 | 8.60 | 8.77 | 2.71 | 8.88 |
| CN13 | 0.000 | 0.010 | 0.034 | 8.80 | 8.90 | 4.18 | 17.93 |
表2:活性炭样品的表征。
由于H 2 O(蒸汽)或NaOH作为活化剂的碳含量损失,在NaOH和蒸汽活性炭的情况下灰分含量高,并且由于ZnCl 2对灰分的挥发作用,在ZnCl 2样品的情况下灰分含量低内容。
灭多威的吸附
pH的影响:溶液的pH值影响吸附剂的表面电荷和吸附物的形态程度,是吸附过程中的重要控制参数。灭多威的化学名称是S-甲基N-(甲基氨基甲酰氧基)硫代乙酰亚胺,分子量为162.根据危险物质数据库[ 29 ] 报道的灭多威的物理化学性质,灭多威在水环境中的水解半衰期取决于关于溶液的pH值。因此,用图4中显示的结果研究了溶液的pH值对灭多威的影响。所得结果表明,在2至8的pH范围内,灭多威相当稳定。相反,当pH值升至10时,灭多威的残留量仅为原始的12%。此外,在高pH值为12时,灭多威完全降解为其他化合物,解释了灭多威在碱性溶液中相当显着降解。因此,在2-8的pH范围内检查pH值对吸附容量的影响。如上述图图4,其吸附能力随pH值的增加而减小,这表明的溶液pH值的降低提高了灭多威的吸附。ACPNS是弱碱性阴离子,pHpzc(零电荷点)7-8,如表3所示。灭多威对ACPNS的吸附可能主要是由于π电子的分散力和极化(吸附质的富电子部分)。
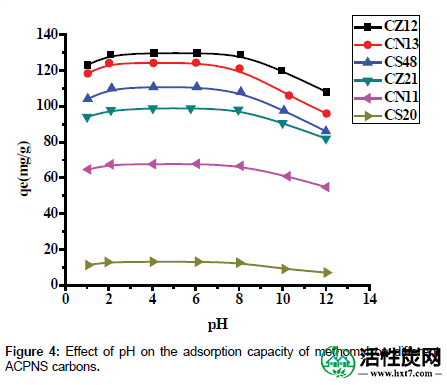
图4: pH对灭多威对不同ACPNS碳的吸附能力的影响。
| 样品 | T = 289K | T = 313K | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Langmuir常数 |
Freundlich 常数 |
Langmuir常数 | Freundlichconstants | |||||||||
| QE(毫克/克) | B(L /毫克) | R 2 | ķ | ñ | R 2 | QE(毫克/克) | B(L /毫克) | R 2 | ķ | ñ | R 2 | |
| CS20 | 41.67 | 0.040 | 0.997 | 1.79 | 1.50 | 0.997 | 50.00 | 0.150 | 0.999 | 32.43。 | 12.20 | 0.996 |
| CS48 | 166.67 | 0.250 | 0.999 | 51.94 | 3.15 | 0.993 | 212.77 | 0.100 | 0.999 | 39.92 | 2.58 | 0.997 |
| CZ21 | 142.86 | 0.023 | 0.999 | 28.96 | 2.47 | 0.995 | 200.00 | 0.037 | 0.998 | 29.22 | 2.18 | 0.999 |
| 十二生肖 | 166.67 | 0.083 | 0.999 | 75.19 | 8.47 | 0.999 | 204.08 | 0.089 | 0.998 | 40.85 | 3.50 | 0.996 |
| CN11 | 71.43 | 0.049 | 0.999 | 8.36 | 2.24 | 0.993 | 80.00 | 0.057 | 0.998 | 10.49 | 2.34 | 0.997 |
| CN13 | 217.39 | 0.092 | 0.999 | 65.24 | 3.86 | 0.992 | 250.00 | 0.138 | 0.998 | 48.38 | 2.58 | 0.997 |
表3:用于在活性炭上吸附灭多威的Langmuir和Freundlich等温线常数。
相反,在酸性pH(<2)下较低的害虫去除可能是由于存在过量的H +离子与带正电荷的灭多威分子竞争吸附剂的吸附位点。此外,在较低的pH值(低于羧基的pKa,约4.6),ACPNS中的-COO-基团质子化为-COOH基团并且形成-COOH和-NH 2基团之间的氢键导致灭多威吸收。此外,ACPNS的带正电荷的氨基与阳离子农药分子之间的排斥导致酸性介质中的害虫去除减少。
初始灭多威浓度的影响:在正常农药pH下,在不同温度下研究了初始浓度对ACPNS去除灭多威的影响。结果如图5所示。可以看出,吸附剂的平衡吸附容量随着初始害虫浓度的增加而增加,并且不同浓度下的吸附在初始阶段是快速的,并且随着吸附的进行逐渐降低直至达到平衡。这可归因于以下事实:初始灭多威浓度越高,固 - 液界面处浓度梯度的驱动力越大,这导致吸附剂上吸附的灭多威的量增加。在较高的灭多威浓度下,吸附容量达到平台,表明吸附剂上可用的结合位点饱和。
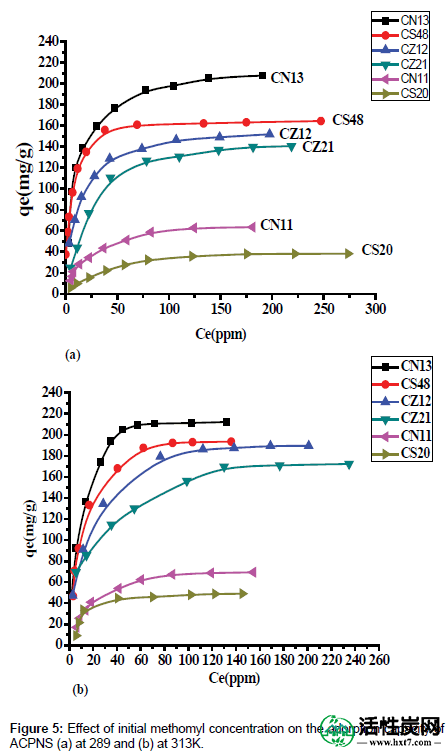
图5:初始灭多威浓度对ACPNS(a)在289和(b)在313K的吸附能力的影响。
吸附剂用量的影响:实验研究了吸附剂用量对灭多威吸附的影响。将不同量的CN13作为选择的ACPNS样品加入到固定的初始农药浓度中。在24小时的接触时间与所用的吸附剂剂量(g / L)之后摄入灭多威如图6所示。可以注意到,当CN13剂量分别从0.12g / L增加到1.57g / L时,灭多威摄取量从19%增加到87%。这是因为随着吸附剂用量的增加,更多的吸附位点可用于吸附物增强灭多威吸收[ 44 ]。此外,随着吸附剂负载的增加,吸附在吸附剂单位重量上的灭多威的量减少,导致q的减少e(mg / g)值随着活性炭载量的增加而增加。
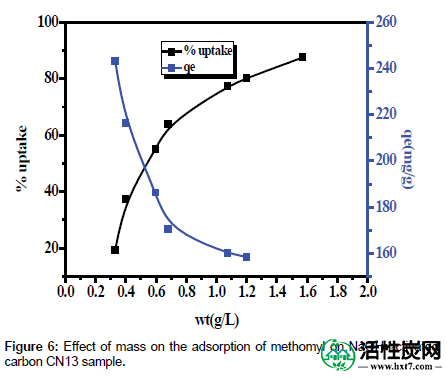
图6:质量对NaOH活性炭CN13样品上灭多威吸附的影响。
接触时间的影响:图7显示了接触时间对于CN13的吸附容量的影响,例如对于灭多威。随着接触时间从0到20 min的增加,CN13的吸附容量迅速增加,并且在15 min内发生了对灭多威的平衡吸附容量的90%以上。60分钟后,吸附容量变得恒定,吸附达到平衡。因此,选择60分钟作为在我们的实验条件下将灭多威吸附到ACPNS上的接触时间。
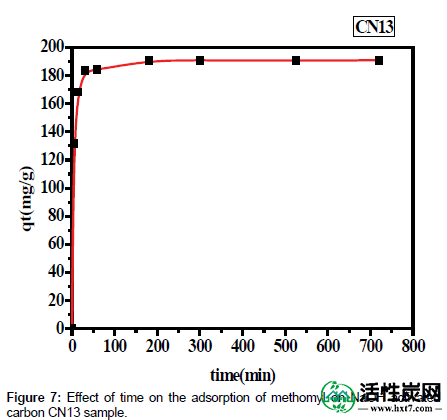
图7:时间对甲醇在NaOH活性炭CN13样品上吸附的影响。
如图所示,吸附过程分为三个阶段:(1)立即吸附发生的初始阶段,(2)随后,缓慢吸附,和(3)吸附达到平衡并保持恒定的最终阶段。第一阶段可归因于通过表面质量转移将灭多威迅速附着于ACPNS的表面。在这个阶段,在所有情况下都发现超过80%的灭多威吸附。第二阶段较慢,可能是因为许多可用的外部位点已被占用,并且由于灭多威分子缓慢扩散到ACPNS的网络中。无论施加于吸附系统的初始灭多威浓度如何,在约20分钟后发现渐近趋势。吸附量在接触时间长于平衡时间(60分钟)时没有显着变化。吸附过程的动力学表明,灭多威对ACPNS的吸附可被认为是一种快速吸附过程,因为超过80%的灭多威在20分钟内被吸附,特别是在低于最大吸附的灭多威浓度下。这些发现揭示了使用这种低成本吸附剂或所谓的生态吸附剂来处理一般富含农药的水溶液和特别是灭多威的益处。
离子强度的影响:从水溶液中去除农药很大程度上取决于静电参数,如表面电荷,pH值和离子强度[ 45 ]。离子强度在水合颗粒的电双层(EDL)结构中起主要作用。随着离子强度的增加,DEL的厚度减小,导致吸附减少[ 46 ]。在这项工作中,在灭多威(6.0)的天然pH下研究了额外量的NaCl在0.002-0.05M浓度范围内的影响。结果表明吸附容量随着NaCl吸附剂浓度的增加而降低。随着NaCl浓度的增加和Na +的增加,离子强度增加离子可以筛选吸附剂的负位点,导致静电引力的降低,因此,灭多威的吸附量减少。离子强度还可以导致灭多威分子的二聚化过程,从而在高浓度的Na +和Cl -离子存在下降低静电力。
离子强度进一步增加超过0.05M时,吸附容量急剧下降至0.15M,其中任何进一步增加导致吸附容量急剧下降,因为从水溶液中盐析出农药分子。这些结果表明离子强度对农药吸附有不利影响,这可能是由于阳离子和农药之间对富电子位点的竞争所致。
温度的影响:在不同温度下研究灭多威对ACPNS的吸附,结果如表3所示。吸附的灭多威的量随着温度的升高而增加,这意味着在改性和未改性的碳上从水溶液中的灭多威吸附是吸热过程。的吸附能力的提高可能是由于吸附物和吸附剂,创建了一些新的吸附位点,或颗粒内部的扩散速率增加到吸附剂的孔隙中在较高温度下[之间的化学相互作用38,39 ]。当温度从289K增加到313K时,ACPNS去除了最大量的灭多威。
吸附等温线
在平衡分析中,Langmuir [ 3 ]和Freundlich [ 4 ]模型是最常用的等温模型,用于研究常用的等温模型,用于研究吸附行为和系统。在不同温度下研究的系统的Langmuir和Freundlich等温线分别在图8和9中给出。
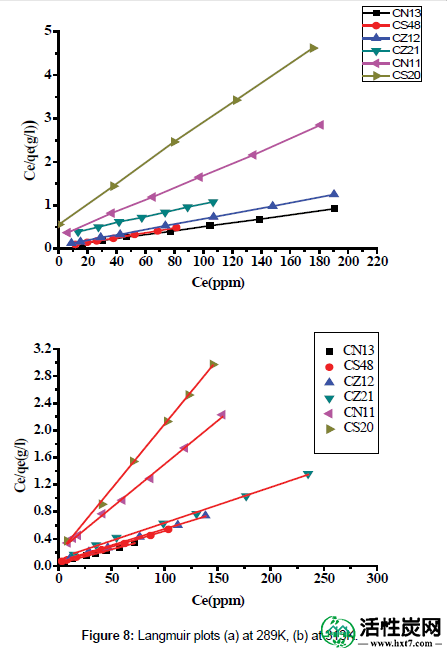
图8: Langmuir图(a)在289K,(b)在313K。
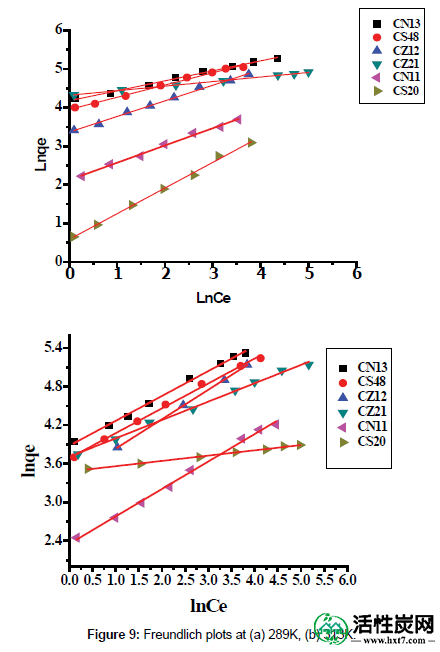
图9:(a)289K,(b)313K的Freundlich图。
表3还显示了在289和313K处不同吸附的Langmuir和Freundlich吸附参数。表3的检查描述了:(i)通过相关系数(R2)证明,灭活剂对ACPNS吸附剂的吸附遵循Freundlich和Langmuir模型,其范围在0.996和0.999之间。在所有样品上吸附灭多威的最佳拟合模型是Langmuir吸附模型。(ii)随着温度的升高,吸附容量增加,这表明对灭多威吸附的所有过程都具有吸热性质;(iii)随着活化剂的比例随着ZnCl 2或NaOH的增加而增加,吸附容量增加。活化样品。
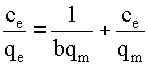 (3)
(3)
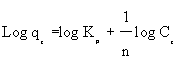 (4)
(4)
吸附动力学
为了解吸附过程,应用四种动力学模型分析实验数据。Lagergren的伪一级动力学模型的线性形式[ 47 ],Ho的伪二阶动力学的线性形式[ 48 ],粒子内扩散模型[ 49 ]和Boyd模型[ 5 ]。在该研究中,在ACPNS上测试了四种模型的灭多威。根据线性相关系数R 2确定最佳拟合模型。结果显示在图10a,b中并且在表4中示出。
| 一阶动力学方程 |
二阶动力学 方程 |
粒子内扩散 方程 |
博伊德方程 | QE,实验值(毫克/克) | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| q1(mg / g) | K 1(1 / min)* 103 | R 2 | q2(mg / g) | K 2(g / mgmin)* 104 | R 2 | K int(mg /(g min1/2)) | C |
R 2 int |
一世 | R 2 | |
| 31.77 | -3.365 | 0.377 | 192.31 | 2.97 | 0.999 | 1.59 | 159.66 | 0.307 | 0.249 | 0.849 | 217.39 |
表4:在CN11上吸附灭多威的动力学参数。
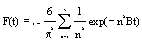 (5)
(5)
接近单位的伪二阶相关系数远高于伪一阶,伪二阶计算的理论q 2 e值与表4中给出的实验q exp值非常接近,表明伪二阶模型更适用于该系统,而从伪一级动力学估计的理论q 1 e值没有给出合理的值,表明该模型不能用于描述灭多威对该系统的吸附数据。吸附剂。
为了确定吸附过程中的吸附机理和速率限制步骤的预测以了解吸附现象,应用了颗粒内扩散和Boyd模型。对于颗粒内扩散,图10c,获得的结果表明q t对t 0.5的图用于灭多威的CN11是多线性的,含有至少三个线性链段,表明在吸附过程中发生三个步骤。第一个更尖锐的部分是通过扩散通过边界层将有害分子从本体溶液输送到吸附剂外表面(膜扩散)。第二部分是有害生物分子从外表面扩散到吸附剂的孔中。第三部分是最终平衡阶段,其中有害生物分子被吸附在孔内表面上的活性位点上,并且由于溶质浓度在溶液中越来越低,颗粒内扩散开始减慢[ 50,51]。而且,曲线的线性部分没有通过原点,这表明孔扩散不是控制吸附开始时总传质速率的步骤。在表4中,线性片段粒子内扩散模型的相关系数(R 2)为0.307,表明粒子内扩散不是唯一的速率控制步骤; 其他过程可以控制吸附速率。
因此,应用Boyd动力学模型(图10d)来预测吸附过程中涉及的缓慢步骤。对于Boyd动力学模型,获得的结果表明,对于灭多威的B(t)对CN11的(t)的线性图不通过原点,表明吸附过程受膜扩散控制。
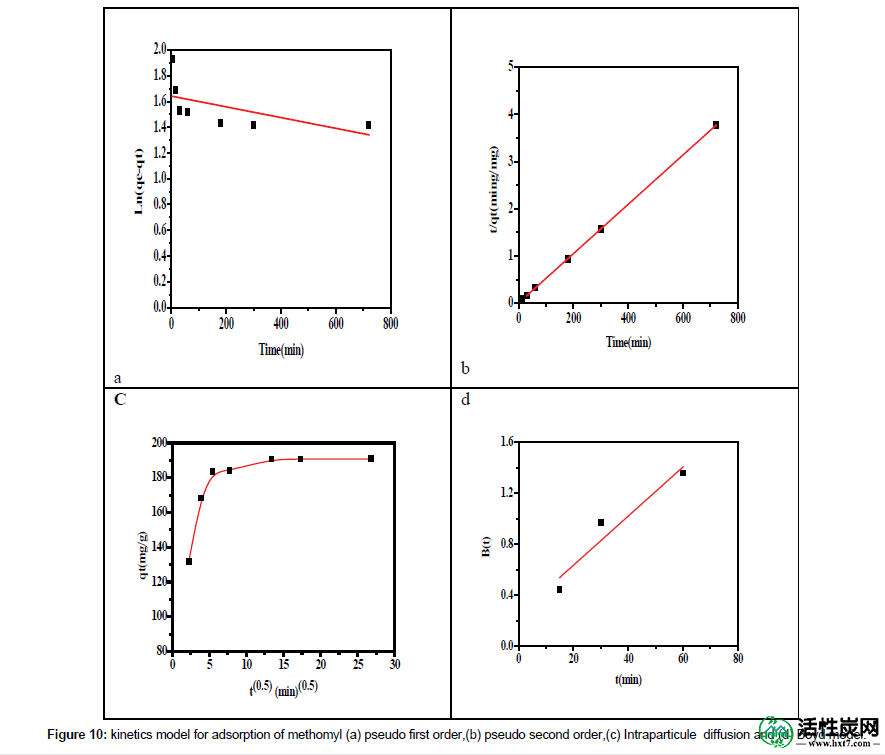
图10:灭多威的吸附动力学模型(a)伪一级,(b)假二级,(c)分子内扩散和(d)博伊德模型。
热力学研究
为了确定温度对灭多威吸附的影响,还分别在16和40℃下进行吸附实验。如图5所示,灭多威对ACPNS的吸附容量随着温度的升高而明显增加,表明吸热反应。的热力学参数,如在吉布斯自由能的变化(ΔG ø,千焦/摩尔),焓(ΔH ø,千焦/摩尔)和熵(ΔS ø,J /(摩尔•K))来计算[ 52 ]。
甲氧基吸附在ACPNS上的热力学参数如表5所示。ΔH°的正值反映了灭多威吸附ACPNS的吸热性质,表明吸附在高温下是有利的,这是由于升高温度下灭活酶对ACPNS的吸附增加所支持的。在较高温度下吸附更有利,并且灭多威强烈吸附在两种ACPNS的表面上。
| 样品 | -ΔG°(KJ / mol)的 | ΔH°(KJ / mol)的 | +ΔS°(焦耳/ mol.K) | |
|---|---|---|---|---|
| 289K | 313K | |||
| CS20 | 14.43 | 18.22 | 41.43 | 190.00 |
| CS48 | 20.00 | 21.68 | 28.72 | 70.02 |
| CZ21 | 17.76 | 18.67 | 14.90 | 113.00 |
| 十二生肖 | 19.25 | 20.19 | 2.19 | 75.00 |
| CN11 | 16.25 | 18.06 | 4.74 | 73.00 |
| CN13 | 19.78 | 21.36 | 12.71 | 109.10 |
表5:灭多威吸附在活性炭上的热力学系数。
负ΔG°表示吸附过程是自发的。ΔG°的大小随着温度的升高而增加,这也表明在较高温度下实际获得了更好的吸附,因为更负的ΔG°意味着更大的吸附驱动力,导致更高的吸附容量。
正ΔS°建议引线吸附过程中,在固/液界面增加随机性。
吸附机理
通过蒸汽,NaOH或ZnCl 2对碳表面的改性引入了多种酸性碳氧官能团。这些基团在水溶液中解离并参与金属结合过程。其他表面氧原子(其中一些可能不是质子源官能团的组分)可能参与复合物形成。因此,可以预期灭多威与从羧基和酚表面基团释放的H +之间的离子交换,因此这些基团显着促进农药摄取的增强。另一方面,羰基和/或内酯基更可能参与与灭多威的复合物形成[ 55 ]。
分析应用
制备的ACPNS成功地用于去除掺入不同天然水样品中的已知量的灭多威。回收率介于和之间,相对标准偏差(RSD,%,<3)。
本研究的结果表明,ACPNS可能是非常可行的吸附剂,用于从水溶液中去除灭多威。通过蒸汽,NaOH和ZnCl 2对ACPNS的改性显着增加活性炭表面的含氧基团,表面形态和纹理性质发生明显变化。灭多威的吸附取决于初始浓度,反应温度和pH。灭多威对甲基的吸附容量随pH的增加而增加,在3-8的范围内,羧基发生电离。灭多威对活性炭的吸附在约60分钟内达到平衡。Langmuir吸附等温线可以很好地描述吸附平衡,即在均匀表面上的单层吸附。吸附动力学遵循伪二级动力学模型,并且颗粒内扩散参与吸附过程。热力学结果表明吉布斯自由能变化(ΔG°)与在应用条件下的自发过程所预期的一样是负的。制备的ACPNS成功应用于从天然水样中去除灭多威。