发布日期:2018-11-07 11:27 来源:活性炭网 作者:活性炭网 浏览数:
抽象 设计具有孔隙率的吸附剂允许去除蛋白质结合的和高分子量的尿毒症毒素可以改善血液透析治疗慢性肾病(CKD)的有效性。 设计用于直接血液接触的纳米多孔活性炭整体原型首先
对于进展为慢性肾病第5阶段(CKD5d)并且未接受移植的患者,血液透析是一种成熟的,维持生命的疗法。但是发病率和死亡率,特别是那些患有心血管疾病(CVD)有关的改进尽管疾病管理与垫款高通量和血液渗滤技术仍然很高[ 1,2 ]。与CKD5d相关的患病率增加,成本上升和预后不良已经确立。全世界有超过200万CKD5患者接受透析,发达国家的患病率每年上升5-8%,与糖尿病,高血压和肥胖的发病率增加有关[ 3 - 5]]。虽然不到0.1%的欧洲人口接受血液透析治疗,但费用总额占医疗保健预算的2%[ 6 ]。尽管透析费用相对较高,但患者的存活率仍然很低。来自英国肾脏登记处的五年生存数据显示,透析患者的生存率略高于卵巢癌,但比结肠癌的生存率更差[ 7]。
与CKD和CVD进展相关的病理生理学是多方面的,但与内皮细胞长期暴露于与慢性细胞因子表达相关的炎症和促动脉粥样硬化环境以及蛋白结合和高分子量尿毒症毒素的作用明显相关[ 8 - 15 ]。目前的血液透析系统主要通过扩散和对流去除小的水溶性代谢物和一些低分子量蛋白质,但是不能去除那些保留可能最具破坏性的尿毒症毒素。目前的研究使用了充分表征的高分子量细胞因子白细胞介素6(IL-6)和蛋白质结合的吲哚硫酸盐(IS)和对甲苯基硫酸盐(p-CS)作为该组的标记分子。升高的IL-6是CKD患者所有原因和CVD相关发病率和死亡率的预测标志物[ 16 ]。IS(213Da )和p- CS(188Da)是源自膳食蛋白的肠细菌代谢的小分子,但主要在血浆中非共价结合至66kDa白蛋白,因此通过血液透析很难除去。两者都与心血管,肾脏和骨骼生理随后,负面影响持续的氧化应激的煽动者和通过基于策略的吸附剂[被认为是去除的主要目标17 - 23 ]。
含有体外装置的吸附剂的实例包括分子吸附剂再生系统(MARS™),分馏血浆分离和吸附系统(普罗米修斯™)和Hemocleanse SSR [ 24,25]。MARS和Prometheus都被设计用于治疗肝功能衰竭,其中HD单独用于桥接肝脏再生或移植。MARS含有微孔活性炭柱,通过将患者血液透过白蛋白不可渗透的高通量膜透析成富含白蛋白的透析液。然后通过低通量透析膜,微孔活性炭柱和阴离子交换树脂柱过滤再生透析液。Prometheus系统包含两个吸附剂盒,采用不同的方法,其中白蛋白和毒素都通过白蛋白可渗透的250 kDa截止膜和白蛋白结合的毒素,然后通过中性树脂吸附器过滤在二级回路中除去,然后阴离子交换器。通过第二高通量透析器的血液过滤除去水溶性毒素。Hemocleanse装置还含有活化的微孔碳,并用于治疗急性肝功能失代偿。然而,与标准支持性医疗管理相比,这些设备中没有一个能够显着改善患者预后。
用活性炭微孔血液灌注系统,用于肾功能衰竭的治疗超过40年前进行了测试,结果显示显著的疗效,但与碳微粒,凝血,电解质紊乱及血小板损失有限的进一步发展[释放技术问题26 - 28 ]。为了改善血液相容性,目前临床使用的大多数活性炭吸附剂往往涂有纤维素或水凝胶/肝素共聚物[ 29]。不幸的是,这种涂层也限制了高分子量分子的吸附能力,并且在欧盟临床上用于直接血液接触的唯一碳血液吸附剂是用于治疗严重药物过量的那些[ 30]]。在碳技术的最新进展已经允许衍生的活性炭的新型酚醛树脂,其可以用于未涂覆与血液直接接触的发展,并具有定制的纳米多孔结构允许上述50kDa的[大生物毒素吸附31 - 33 ]。可以沿着其长度使用直的传输通道制造三维挤出的碳整体块,以便通过直接血液接触进行吸附。我们曾报道,这些活性炭不激活补体或吸附凝血因子改变内在或外在的凝血级联[ 31,34]。该研究是概念研究的证明,首先设计用于测量整体孔隙度对使用体外方法去除选择的标记物尿毒症毒素的影响。在证明标记物分子去除后,然后进行使用临床血液透析患者血液样品的初步研究以确定这些代表性的尿毒症毒素在标准血液透析治疗后是否保留在血液中,然后可以在吸附剂整体血液灌注后除去。
整体式吸附剂由MAST Carbon International Ltd(Basingstoke,UK)合成。所使用的整料为0.7cm宽和10cm长,并且包含沿着整料的长度延伸的32个通道,每个通道具有0.5mm的宽度。通过混合和固化Novalac树脂,乙二醇和六胺的不同配方形成整料。将所得树脂饼压碎,干燥或洗涤以除去多余的成孔剂,研磨形成面团,然后挤出。将得到的整料碳化并在高达900℃的温度下在二氧化碳中活化,纳米孔隙率主要由初始树脂成孔剂组合物控制。所得材料的孔隙率通过扫描电子显微镜(SEM)使用Sigma场发射枪(FEG)-SEM显微镜(Carl Zeiss NTS,Cambridge,®水银压入孔隙率计(Quantachrome Instruments Ltd,Hook,UK)。使用Quantachrome软件进行与表面积,孔体积和孔径分布有关的计算。
使用掺有p- CS(250μM),IS(125μM)和IL-6(1,000pg / ml)的健康供体血液测量吸附性整料去除标记物尿毒症毒素的能力。使用连续循环系统来比较不同孔隙率的整体块从血浆和血液中去除尿毒症毒素。将20ml储存体积的加标血液循环通过以磷酸盐缓冲盐水(PBS)预先润湿的每个整料,以5ml / min的速率,并以定时间隔取样。将血液样品以3,500rpm离心15分钟并除去血浆。在分析之前将所有样品储存在-20℃。
HPLC方法改编自de Loor等人描述的方法。[ 35 ]使用竞争性白蛋白与辛酸钠结合来测量血浆中的总p- CS和IS。将血浆(200μl)与250μl辛酸钠(0.24μM)一起温育30分钟。加入内标(萘磺酸,0.5mM,20μl)。将样品与2ml冰冷的丙酮混合以沉淀蛋白质并以4,000rpm离心10分钟。除去上清液,与2ml冰冷的二氯甲烷混合,并以4,000rpm离心10分钟。除去顶部水相,加入40μl1MHCl以稳定溶液。使用Fortis C 18实现峰分离(150 mm×4.6 mm OD,3μM)色谱柱,配有0.5μm烧结Krudkatcher预料筒。将柱保持在25℃。将含有样品的壳小瓶置于弹簧尖端插入物中,置于15℃的Waters 717 plus自动取样器中,其设定为10μl注射,20分钟运行时间和10分钟报告延迟。对Perkin Elmer Series 200四元梯度泵进行程序设计,以提供流动相[A(%)= 0.2%三氟乙酸(TFA)的水溶液,B(%)= 0.2%TFA的乙腈溶液如下:85/15(保持5 min)-80 / 20(5分钟)-0/100(2分钟,保持3分钟),0.6ml / min,然后85/15(2分钟),1.0ml / min]。使用Varian Prostar 363荧光检测器进行时间程序。使用双检测波长。最初在280和360nm的激发和发射波长下检测IS和内标。p- CS分别在260和296nm的激发和发射波长下完成。使用Totalchrom软件通过PE Nelson 900系列(A-D)接口可视化和集成峰。使用以下等式计算检测限(LOD)和定量(LOQ)。
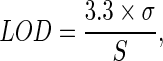
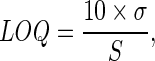
其中S是校准曲线的斜率,σ是基于校准曲线的响应的标准偏差。
来自吸附研究的血浆样品在测定稀释剂中进行1/2稀释,并根据制造商的说明书(BD Biosciences,Oxford,UK)通过ELISA进行分析。通过ELISA分析来自临床取样研究的血浆样品的IL-6含量,而不进行进一步稀释。
使用血液透析患者血液样本进行了小概念证明研究。该研究的伦理批准来自东南海岸国家研究伦理委员会 - 布莱顿和苏塞克斯REC参考11 / H1111 / 7。使用批准的知情同意方案将11名在苏塞克斯肾脏单位接受血液透析的患者招募到该研究中。患者接受标准的4小时,每周三次血液透析方案,使用高通量FX-10聚砜血液透析仪。血液透析前后抽取血液测定尿素,肌酐,钙,总蛋白,白蛋白,血红蛋白,白细胞,红细胞,血小板计数,IS,p-CS和IL-6。将另外20ml透析后患者血液收集到肝素化管(16IU / ml血液)中,并在连续循环系统中通过纳米多孔碳单块灌注90分钟。在0,30,60 和90分钟时分析该系统中的血液,以评估随着时间的推移灌注通过整料后IS,p -CS,IL-6和纤维蛋白原的去除。在90分钟后,再次分析血液中的尿素和上面列出的整体再循环之后的其他参数的变化。通过以3,500rpm离心15分钟分离血浆,并在通过HPLC,ELISA和凝血测定法分析之前储存在-20℃。使用START 4凝血计和Fibri-perst试剂盒,使用1:20稀释的血浆样品(Diagnostica Stago,Theale,UK)测量纤维蛋白原浓度的变化。
使用Student's t检验分析来自体外研究的数据的统计学显着性,比较整体过滤与对照组在60分钟时的比较。使用Student's t检验比较来自试验研究的数据的统计学显着性,比较血液透析前后和整体过滤前后的配对数据。数据表示为平均值±平均值的标准误差(sem)。
来自水银孔隙率测定法的孔径分布图显示由不同树脂和成孔剂组合制成的整料的孔隙率的差异。两种类型的碳单块用于体外研究。纳米多孔整料在介孔至小的大孔范围内具有孔,直径为2-100nm(图 1a)。微孔活性炭单块仅具有小于2nm的孔。氮气孔隙率测定数据分析表明,介孔整体材料的表面积为852 m 2 / g,孔体积为1.14 cc / g,表面积为782 m 2/ g和微孔单块的孔体积为0.51cc / g。纳米多孔结构域上所采取的纳米多孔活性炭块(图的横截面的高倍率扫描电子显微镜照片可见 1 b)中。
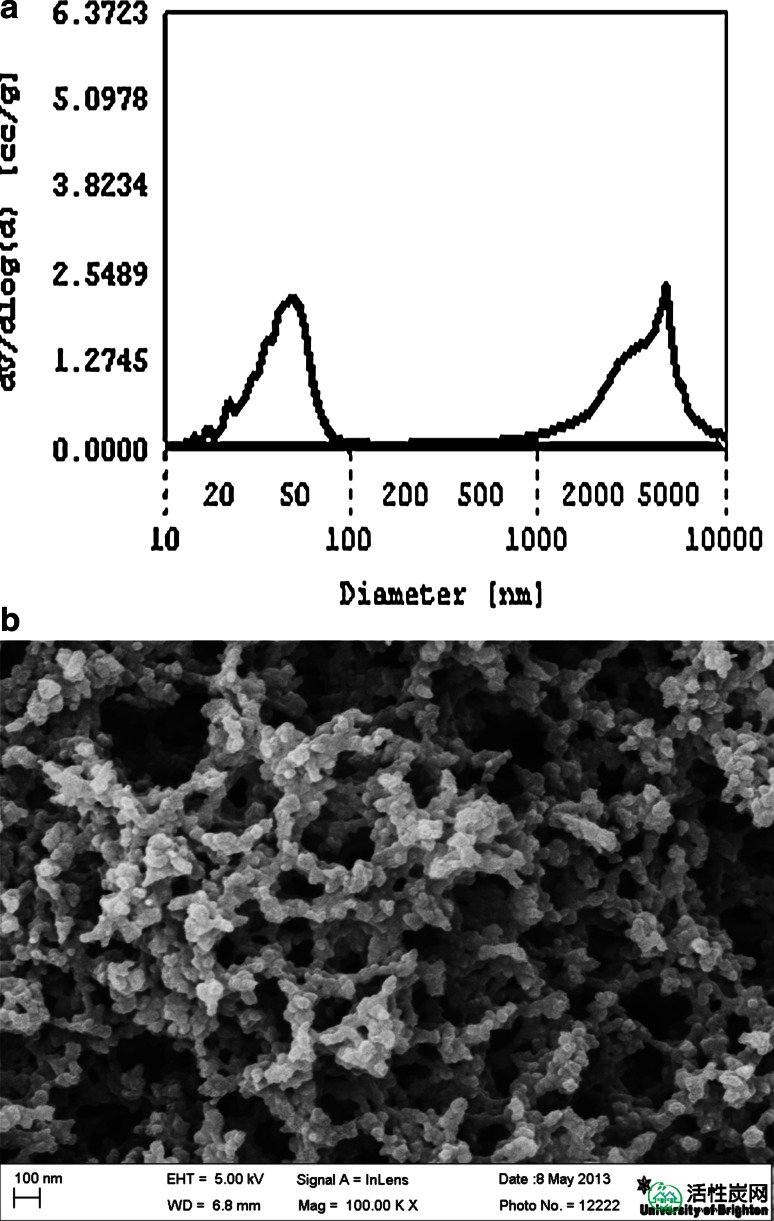
纳米多孔整料孔隙率的表征是使用仪PoreMaster水银压入法和Sigma场发射枪扫描电子显微镜(FEG-SEM)一个康塔数据还原软件用于计算表示2-100纳米的纳米多孔结构域的水银孔径分布曲线图在原型碳单块内。所述第二峰值是由颗粒间的空间,其是在直径1-10微米制造。b纳米多孔活性炭整料横截面的SEM显微照片显示内部纳米多孔区域(放大倍数×100,000)
体外整料再循环研究表明通过在纳米多孔整料(图中IL-6浓度的显著减少连续过滤15分钟后 2 A,P <0.01)。在60分钟的过滤循环中,IL-6浓度从900降至400pg / ml。相反,通过微孔单块的过滤几乎不降低IL-6的浓度。在连续灌注加标的全血通过微孔碳单块后,发生一些IS和p- CS的去除。IS和p的浓度-CS分别从120μM降至60μM,从275μM降至150μM。然而,在通过纳米多孔整料灌注后,浓度降低最大。IS浓度从140至20μM降低和p -CS从350至75μM降低(图 2 B,C)。仅纳米多孔整料除去了显着量的高分子量细胞因子IL-6。白蛋白结合的尿毒症毒素IS和PCS在一定程度上被微孔碳除去,但在通过纳米多孔碳单块灌注后去除更有效。因此,纳米多孔整料用于使用血液透析后血液样品进行初步研究。
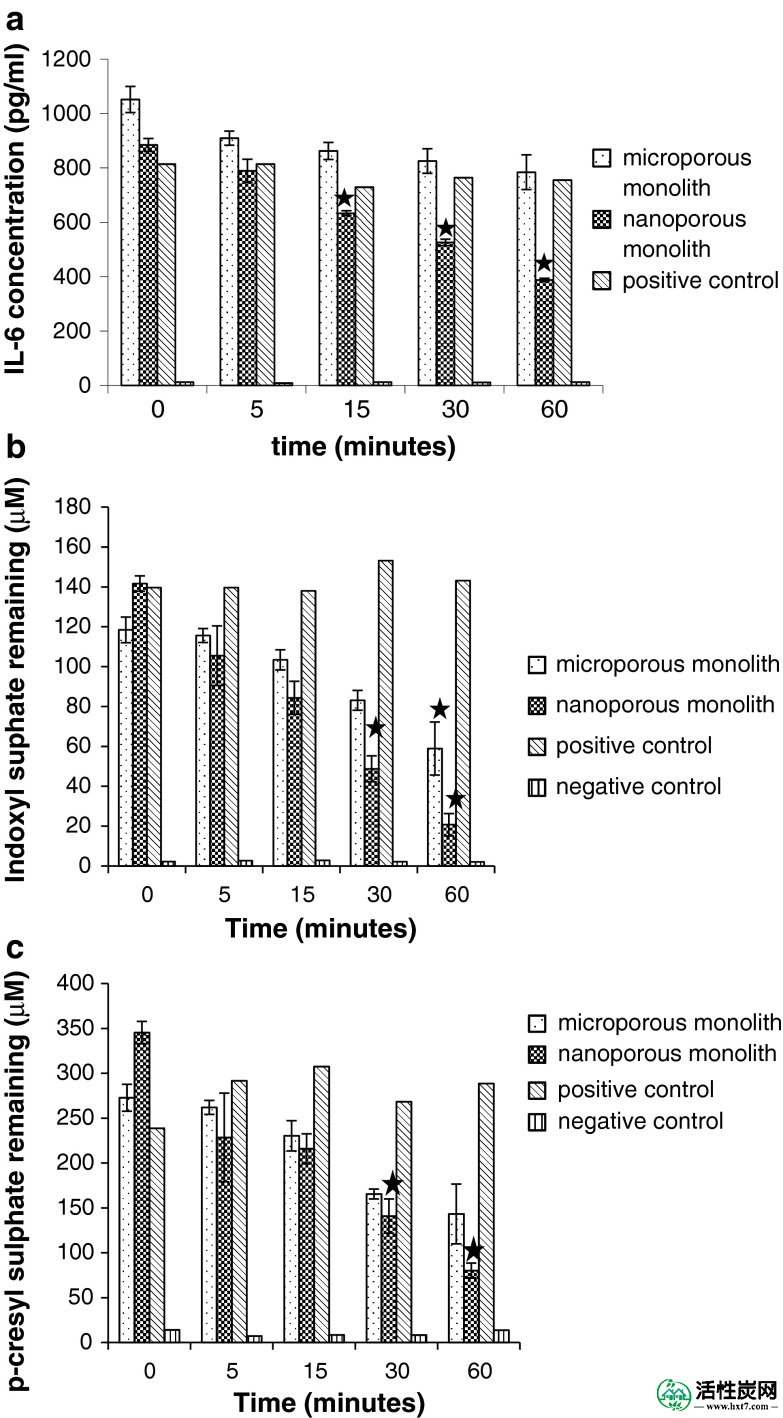
一个 IL-6,b硫酸吲哚酚和Ç p通过纳米多孔整料,微孔整料和掺入和非掺加对照-cresyl硫酸盐剩余的掺料新鲜人血以下过滤(Ñ = 3,平均值±SEM)。在整体过滤后剩余 的IL-6,IS,p- CS 浓度的填充星P <0.01 与在每个时间点没有整体循环的加标血液的阳性对照相比
在透析之前,在所有血液透析患者血液样品中检测到高浓度的IS和p -CS。标准高通量血液透析后发生IS和p- CS 无显着降低(图 3a,b)(P > 0.01)。然而,在高通量血液透析患者血液样本通过纳米多孔碳单块连续灌注30分钟后,两者的浓度均降低至可忽略的水平(图 3)(P <0.01)。存在IL-6水平升高仅在一个整体过滤组血样中(患者3,表 1))和一个对照组样品使用透析患者血液,在没有整料的假电路中(患者10,表 1)。碳单块过滤后IL-6浓度降低了50%,但在对照组样品中没有降低(表 1)。
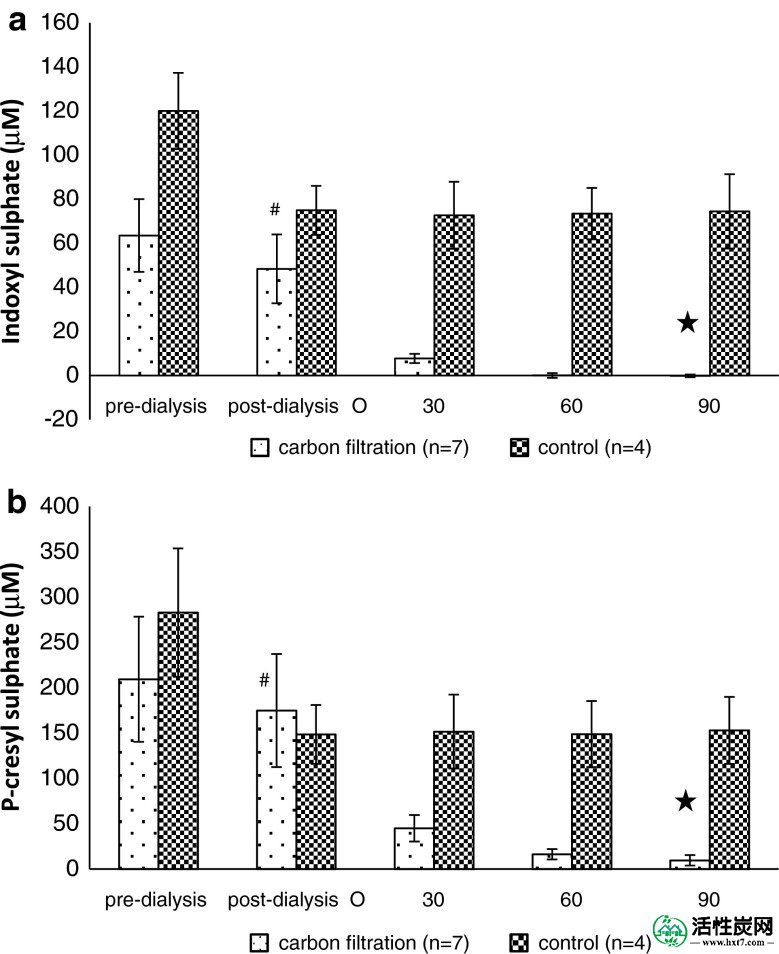
的浓度一硫酸吲哚酚(IS)和b p -cresyl硫酸盐(p -CS)剩余的透析患者的血液样品透析前,透析后和30在此之后,60和90分钟,通过过滤所述纳米多孔碳单块中(Ñ = 7)或仅管道对照(n = 4)。对取自透析后患者的20ml血液样品进行单片过滤。# P > 0.01透析前与IS和透析后的水平p -CS。 与IS和P的整体后过滤水平相比,透析前的填充星P <0.01 与p- CS 的整体后过滤水平相比,预透析= 0.01
血液透析患者血液样本中IL-6浓度(pg / ml)的测量,透析前,透析后和透析后患者血液样本通过纳米多孔碳单块(患者1-7)灌注90分钟后整体控制(患者8-10)。仅在一个整体(患者3)和一个对照组样品(患者10)中检测到显着升高的IL-6水平
| 患者 | 1 | 2 | 3 | 4 | 五 | 6 | 7 | 8 | 9 | 10 |
|---|---|---|---|---|---|---|---|---|---|---|
| 透析前IL-6(pg / ml) | <10 | <10 | 72 | <10 | <10 | <10 | <10 | 14 | 0 | 421 |
| 透析后IL-6(pg / ml) | <10 | <10 | 125 | 0 | <10 | <10 | <10 | <10 | 0 | 435 |
| 后整块或对照IL-6(pg / ml) | 0 | <10 | 53 | 0 | 0 | 0 | 0 | <10 | 0 | 431 |
表2中显示了血液生化前透析,透析后,整体过滤后以及通过系统过滤后没有整体结构的变化 。与除肌酸酐和总蛋白之外的所有标志物的对照水平相比,发生整体后灌注水平没有显着差异。血液透析后肌酐水平从平均值647±190μM下降至256±61μM。整体过滤后肌酐水平显着降低至37±16μM(P <0.01),而对照组水平保持不变(表 2)。与对照组相比,总蛋白水平降至正常范围以下(P <0.05) <0.01)。整体灌注组和对照组血小板计数均降低(P > 0.01),表明通过体外循环血液灌注导致血小板减少,但不是单块接触的直接结果(表 2)。与对照相比,在碳单块过滤样品中未观察到纤维蛋白原浓度的显着差异(P <0.01,图 4)。
与无整体对照相比,在血液透析后患者血液样品的纳米多孔整体过滤之后关键血液参数的变化
| 单块(n = 7,平均值±SD)对照(n = 4,平均值±SD) | |||||||
|---|---|---|---|---|---|---|---|
| 普通范围 | 透析前的 | 透析后 | 后整体过滤 | 透析前的 | 透析后 | 后控制过滤 | |
| 尿素 | 1.7-8.3 mmol / L. | 20.8±7.6 | 6.5±2.7 | 4.6±1.8 | 18.5±4 | 6.25±1.2 | 6.65±2 |
| 肌酐 | 62-106μmol/ L. | 647±190 | 255.6±61 | 37±16 a | 928±247 | 373±112 | 373±112 |
| 调整钙 | 2.15-2.55 mmol / L. | 2.27±.2 | 2.4±.3 | 1.98±.3 | 2.2±.09 | 1.9±.05 | 1.9±.05 |
| 总蛋白质 | 66-87克/升 | 65.7±6.5 | 75±4 | 56±36 a | 65.75±2.8 | 68.25±2.6 | 68.2±5.5 |
| 白蛋白 | 34-48克/升 | 39.3±4 | 45.6±4 | 34.7±2.9 | 40.5±1.73 | 41±1.4 | 39.5±2.6 |
| HB | 13.5-18克/分升 | 11.6±.7 | 12.8±.55 | 9.9±2.03 | 10.9±1.2 | 11±1 | 11.8±4.3 |
| WBC | 4-11×10 * 9 / L. | 73±164 | 7±2.9 | 7.2±2.9 | 6.4±1.6 | 6.35±1 | 5.8±2.4 |
| 血小板 | 150-450×10 * 9 / L. | 188±96 | 203.7±1.9 | 142.9±108 | 195±38 | 185±11 | 116±44 |
| RBC | 4.5-6.5×10 * 12 / L. | 3.8±.5 | 4.2±.4 | 3.2±0.65 | 3.4±.2 | 3.5±2 | 3.6±1.3 |
| HCT | 0.4-.54 fL | .35±.03 | .38±.02 | .3±.06 | .3±.04 | .34±.03 | .34±.1 |
a与无整体对照相比,只有肌酐和总蛋白质降低到正常水平以下
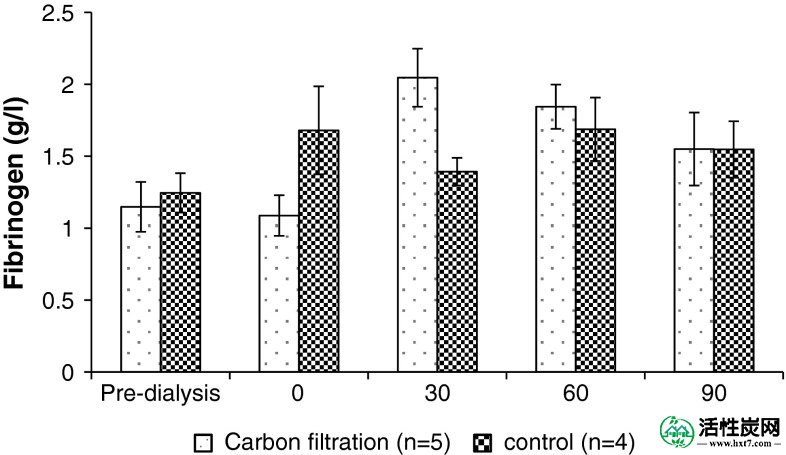
透析患者血液样品在透析前,透析后和30,60和90分钟后通过纳米多孔碳单块(n = 5)或对照(n = 4)过滤测量的纤维蛋白原浓度。 整体过滤的P > 0.01对比纤维蛋白原的对照样品浓度
蛋白质结合的,中等和高分子量的尿毒症毒素在CKD进展期间积累,并且通过目前的血液透析治疗很难去除。我们的研究已经证明,具有大的吸附表面积的活性炭单块可以选择性地定制为包含高达100nm的纳米多孔区域,其能够吸附高分子量和蛋白质结合的尿毒症毒素。以这种方式,这里使用的活性炭的不同之处在于,在先前的体外研究中使用的微孔“炭”中添加了纳米孔。我们的纳米多孔整料来自合成前体,可以提供更一致的产品外形,并消除细碳颗粒释放的倾向。整体结构本身在体外装置中也是独特的,并且允许直接血液沿挤出的碳块内的直通道流动。尽管可以从填充的碳珠系统获得更高的每克碳吸附表面积,但是整体结构允许血液流动而没有显着的压降穿过系统。我们之前已经报道了体外研究,这些研究显示这些纳米多孔整料的生物相容性得到改善,观察到补体未被激活,并且类似的凝血因子未被消耗[31,34 ]。
我们首先寻求确定哪些多孔特征是必要的,以确保从加标的人血液中吸附高分子量细胞因子IL-6和蛋白质结合的p- CS和IS。我们的体外研究证实了专门定制的2-100 nm纳米多孔结构域对于去除高分子量分子(如IL-6)的重要性以及与碳吸附剂结合蛋白结合分子有关的复杂机制。具有高达100nm的孔的整料靶向高分子量和蛋白质结合的物质,不同于由标准微孔碳制成的整料,其显示可忽略不计的IL-6去除。发生了蛋白质结合的IS和p- CS的一些去除,但吸附远小于纳米多孔单块所实现的吸附。
在研究的第二部分,使用血液透析前后血液样本,IS和p在血液透析前后均检测到高浓度的-CS,然后在通过碳单块灌注后降至可忽略的水平。与对照回路相比,血液直接泵送通过纳米多孔整料,而不会导致血小板计数的额外减少或白蛋白的显着去除,尽管两组中血小板计数总体下降。在所研究的10个临床样本中的2个中提高了IL-6水平,表明在小样本试验研究中需要更普遍存在的高分子量标记来评估吸附剂功效。需要进一步的工作来开发和评估可以与透析回路结合使用的按比例放大的装置。虽然,初步数据表明蛋白质结合的尿毒症毒素去除的持续能力应当注意,并非所有推定的尿毒症溶质都适合通过活性炭吸附去除。具有芳香环的分子和疏水相互作用的倾向被吸附,但是电解质和高度水溶性的分子如尿素没有被去除到任何显着程度,如在此和之前的体外研究中所证明的[32 ]。
值得注意的是,在体外研究期间,显着的IL-6整体吸附需要存在较大的纳米孔。相反,一些白蛋白结合的IS和p- CS的去除发生在仅具有小于2nm的孔的微孔单块中。IL-6是一种185氨基酸的多效蛋白,分子量范围为21-26 kDa,三级结构由四个α螺旋组成[ 36 ]。IL-6的结构尺寸为5×5×12.2nm,导致微孔碳没有显着的吸附。同样,人血清白蛋白是一种球状蛋白,大小约为8×8×3 nm [ 37 ],表明IS和p的吸附由于复合物不适合2nm宽的多孔区域,因此不应发生-CS作为由微孔碳结合的白蛋白复合物。血浆中白蛋白的正常浓度范围约为500-700μM。我们在透析后患者样品中观察到平均IS浓度为49± 16μM,平均p -CS浓度为174±17μM。这些分子竞争相同的白蛋白结合位点,因此如果整个白蛋白-IS / p,预计会有更大的白蛋白下降。假设结合比为1:1,通过碳单块吸附简单地除去-CS络合物。血液透析患者血液样品中的白蛋白浓度在整体过滤后下降,但保持在正常范围内,表明整体物质有一些吸附但不足以解释几乎完全去除IS和p- CS。我们的研究结果表明,通过破坏白蛋白和这些分子之间的非共价键,更有可能发生去除。活性炭的孔壁对芳香物质如p- CS和IS 具有高吸附亲和力,促进其络合物与白蛋白的解离。
透析后血液样品中IS和PCS浓度的快速降低表明与使用健康供体血液的体外加标研究的结合动力学不同。CKD与白蛋白的浓度,三级结构和结合能力的变化有关。白蛋白含有大量的硫醇基团和行为作为密钥通过形成二硫键与过量循环自由基[循环抗氧化剂38,39 ]。长期暴露于氧化应激会增加高氧化形式白蛋白的数量,从而诱导构象变化并降低IS和p等分子的结合和转运能力。-CS。结果表明,由于白蛋白结合能力降低,血液透析患者血液样品中白蛋白结合分子的碳吸附倾向更大。然而,需要进一步的工作来强调分子与碳表面结合的特定性质以及CKD5d患者中蛋白质结合毒素与白蛋白和纳米多孔活性碳的相互作用的变化。
许多问题围绕着将吸附装置引入临床实践,包括潜在的有益物质去除和装置维持尿毒症毒素充分清除的能力。以前的出版物表明血液透析后30分钟p- CS从组织到血管空间的反弹释放有限[ 40 ]。已知在血液透析后第一个小时内CKD中出现小水溶性分子尿素和钾的反弹,并且在败血症相关的急性肾损伤中细胞因子的反弹发生,其中血液滤过的去除与进一步的产生和组织释放回到血浆中相匹配。没有观察到细胞因子水平整体下降[ 41]。在炎症介质的情况下,从血液中完全清除它们可能是不利的,但仅仅是为了去除峰值浓度以便抑制过度的炎症失调。考虑到在CKD5d中积累的尿毒症毒素的光谱,活性炭吸附的非特异性优于单一靶向疗法。尽管在等效分子量范围内可能存在一些有益分子的去除,但是通过正常的稳态机制可以进行替换。吸附倾向于仅限制主要血浆蛋白(如白蛋白和纤维蛋白原)的峰值浓度,但显着降低病理生理学高水平的尿毒症毒素,如IS和p-CS通过肾脏排泄的稳态调节失败。在目前的研究中,与对照相比,整体过滤样品中没有发生白蛋白和纤维蛋白原水平的显着降低,尽管所有样品的纤维蛋白原浓度都很低。
CKD5患者的发病率上升以及使用目前的血液透析方案缺乏关于生存获益的明确数据需要新的和创新的方法。初步的初步数据表明,如上所述的吸附系统可用于增加高分子量和蛋白质结合的尿毒症毒素去除,减少慢性炎症刺激并影响CKD5d患者的不良预后。