发布日期:2018-10-09 17:27 来源:活性炭网 作者:活性炭网 浏览数:
在这项工作中,评估了橄榄石活性炭(COSAC)从水溶液中除去Pb(II),Cd(II),Ni(II)和Cu(II)金属离子的能力。 研究了初始pH,接触时间和初始浓度对金属离子吸附的影响。 结果表
在这项工作中,评估了橄榄石活性炭(COSAC)从水溶液中除去Pb(II),Cd(II),Ni(II)和Cu(II)金属离子的能力。研究了初始pH,接触时间和初始浓度对金属离子吸附的影响。结果表明,pH 5是金属去除的最佳值。发现吸附动力学速度快; 4小时后达到总平衡。动力学实验数据很好地拟合了伪二阶方程,并计算了吸附速率常数的值。通过应用Langmuir和Freundlich方程,根据最大吸附容量和吸附亲和力评估平衡等温线。结果表明Langmuir模型比Freundlich模型更适合吸附等温线数据。
| 关键词 | |
| 重金属离子; 吸附; 活性炭橄榄石; 动力学; 平衡 | |
| 介绍 | |
| 重金属造成的环境污染已经成为最危险的问题之一,因为它们即使在相对较低的浓度下也会对水生动植物产生危险的影响。美国环境保护局的优先污染物清单中列入了几种重金属离子,如铜,镍,镉和铅[ 1 ]。铜导致毒性作用,包括肝损伤和胃肠道紊乱。镍是一种众所周知的人类致癌物质,尤其是人类肺癌[ 2 ]。镉导致肾功能不全,高血压和糖尿病[ 3 ],铅具有高度肝毒性[ 4]。许多工业过程,例如熔炼,金属电镀,采矿颜料,镉镍电池,黄铜制造和排出含有高水平这些重金属离子的含水废水。各种物理和化学过程已被广泛用于去除水溶液中的重金属污染物,如化学沉淀,离子交换,生物吸附,吸附,膜过滤等。活性炭上的吸附被认为是最广泛应用的污染物去除技术之一来自污染介质,因为它的效率特别是在低浓度和工艺简单的情况下。大多数研究都集中在由不同前体制备的活性炭吸附重金属,这些前体包括杏石[ 5 ],竹子[ 6 ]橄榄果肉,樱桃木,稻壳等。许多因素都会影响金属离子在活性炭上的吸附程度。在一方面,必须考虑到:(i)溶液pH,溶质性质和浓度,金属离子的物理化学性质,例如物种形成,离子半径,水合能和电负性。在另一方面,必须考虑吸附剂特性为(i)吸附剂表面的零电荷点(pH pzc); (ii)吸附剂比表面积和孔隙率; (iii)吸附剂表面官能团。这些吸附剂性质中的一些与活化过程和氧化剂有关。 | |
| 这项工作的目的是评估橄榄石碳化学活化的吸附能力,以及研究水溶液中铜,镍,镉和铅二价离子的吸附平衡和动力学。 | |
| 试验 | |
| 化学品和设备 | |
| 本研究中使用的所有化学品均为分析级。通过在Milli-Q水质中溶解适量的Cu(NO 3)2 .6H 2 O,Ni(NO 3)2 .12H 2 O,Cd(NO3)2 .4H 制备1 gL-1的储备金属溶液2 O和Pb(NO 3)2。稀释每种硝酸盐的储备溶液以获得所需的初始金属离子浓度(C 0)。由Cu(II),Ni(II),Cd(II)和Pb(II)标准溶液(1 gL -1)制备的不同稀释金属浓度对于FAAS,Merck)用于获得火焰原子吸收光谱法(VARIAN吸收光谱仪(Model220FS))的校准曲线。使用NaOH(0.1M)和HNO 3(0.1M)的溶液调节pH。 | |
| 吸附剂 | |
| 根据Ghrib等人的说法,通过化学活化产生的橄榄石活性炭(COSAC)。[ 7 ],用作吸附剂。在使用之前,用蒸馏水洗涤COSAC以除去可溶性有机物质,在60℃下干燥,然后研磨并筛分,选择的粒度范围为0.250-0.500mm。橄榄石活性炭的比表面积和孔隙特征通过氮吸附和解吸等温线在77.7K下用自动Sorptiometer Autosorb-1C Quantachrome装置测定。通过分批平衡技术[ 8 ]和Boehm滴定分别测定pH pzc和表面官能团[ 9 ]。 | |
| 吸附实验 | |
| 在30±2℃的温度下以分批模式进行平衡实验。为了获得吸附平衡等温线,将0.3g(具有粒径范围:0.25-0.5mm)COSAC的样品直接放入250ml含有50mL金属离子溶液的玻璃塞锥形烧瓶中,所述金属离子溶液具有在该范围内的不同初始浓度Pb(II)为0.2至5.0mM,Cd(II)为0.2至8.0mM,Cu(II)和Ni(II)均为0.2至14.0mM。将烧瓶搅拌10小时,搅拌速度为400rpm。然后,将样品通过0.45μm纤维素滤纸过滤。在实验期间,通过使用恒温浴将温度保持在30±2℃。 | |
| 初始溶液pH值对COSAC吸附Cu(II),Ni(II),Cd(II)和Pb(II)的影响在上述相同的条件下进行,初始金属离子浓度为1mM,平衡时间为10h。通过添加一定体积的0.1M NaOH或0.1M HNO 3将初始pH溶液调节在2.0至5.5的范围内。 | |
| 在三种不同的初始金属浓度(0.5,1和1.5mM)和6gL -1 COSAC 的固定吸附剂量下,在具有500mL金属溶液的分批混合悬浮液中研究吸附动力学。通过使用恒温浴将悬浮液的温度保持在30±2℃。以预定的时间间隔取出2mL体积的溶液样品。 | |
| 在用HNO 3溶液酸化以防止金属沉淀后,测量初始浓度和平衡时的最终浓度,通过FAAS在波长324.8,232.0,228.8nm和217.0nm处,对于Cu(II),Ni(II),Cd(II) )和Pb(II)分别使用空气 - 乙炔火焰。 | |
| COSAC的金属离子吸收量使用以下等式计算: | |
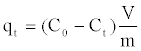 (1) (1) |
|
| 其中C 0是溶液中的初始金属浓度(mmol),C t是给定时间内溶液中残留的金属浓度(mmol),m是COSAC(g)的重量,q t是金属离子吸收(mmol.g -1)和V是烧瓶中溶液的体积。 | |
| 用于关联吸附平衡的Langmuir和Freundlich模型的线性方程分别用等式(2)和等式(3)计算。 | |
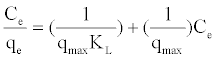 (2) (2) |
|
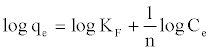 (3) (3) |
|
| 其中K L是与吸附自由能(l mg -1)和q max相关的平衡吸附常数:最大吸附容量(mmol g -1),Ce是平衡浓度(mmol l -1),q e在平衡时吸附的量(mmol g -1)。K F,(mmol l -1)(lg -1)(1 / n)和n分别是Freundlich方程的常数。 | |
| 每个实验一式两份进行,平均结果如本文所示。 | |
| 结果与讨论 | |
| 活性炭的表征 | |
| 活性炭的吸附行为通常取决于表面积,pH pzc和碳表面的化学性质[ 10 ]。通过应用BET方法测定的COSAC的比表面积为1086m 2 ; g-1。计算出微孔和中孔体积分别为0.51和0.01cm 3 g -1(表1)。这表明COSAC是微孔活性炭。 | |
| pHpzc提供了有关碳表面电荷的信息[ 8 ],我们的碳表面在低于pH pzc的 pH值下带正电。相反,在高于pH pzc的溶液pH值下,负表面电荷增加。COSAC的pH值pzc = 3,因此碳表面带负电荷,pH值高于3。 | |
| 一些官能团发生在COSAC表面(表1)。COSAC含有羧酸,内酯,酚和羰基,产生4.77meq.g -1的总酸度。COSAC的总碱度为0.75 meqg -1。表1中报告的表面官能团的结果表明酸性官能团的优势,特别是COSAC表面上的羰基和酚官能团。物理COSAC特性显示出更高的比表面积和发达的微孔。 | |
| pH对COSAC吸附容量的影响 | |
| 的金属溶液的pH值被认为是可以影响的,因为它的上金属溶解度为影响[位于吸附剂表面官能团的解离度的活性炭的吸附容量的最重要的参数11,12 ]。 | |
| 通常,在酸性pH下离子吸收的减少是由于相同吸附位点的氢离子和金属离子之间竞争的增加。然而,碱度的增加提高了金属吸附速率,这是由于重金属的水合物质的主要存在,表面电荷的变化和适当盐的沉淀。因此,存在最佳pH值,其中氢离子的竞争最小化并且因此避免金属离子沉淀,增强金属吸附。 | |
| 实验在低于pH的选定pH值下进行,其中可发生金属氢氧化物化学沉淀:Pb(II)和Cu(II)的pH> 5,Ni(OH)2的 pH> 6 ,Cd的pH> 7.8( OH)2。通过使用MEDUSA计算机程序[ 13 ] 计算的化学物种分布图检索了这些pH值。 | |
| 图1显示了吸附的金属量以及Pb(II),Cd(II),Ni(II)和Cu(II)与初始溶液pH的吸附百分比。结果表明,金属吸附具有很强的pH依赖性,随着pH值的增加而增加,直至pH值为5左右达到最大值。最初,随着溶液pH从2.2增加到5.0,Cu(II),Ni的去除率达到最大值。 (II),Cd(II)和Pb(II)分别从16.4%增加到62%,从21%增加到78%,从34%增加到97%,从50%增加到100%。低pH下的低吸附性,主要是铜和镍,是由于相同吸附位点的质子和金属离子之间的竞争。pH的影响也可以通过考虑吸附剂表面电荷来解释。如前所述,COSAC pH pzc因此,当溶液pH低于3时,由于金属离子和带正电的官能团之间的静电排斥,COSAC的表面带正电荷并且金属吸附受到抑制。相反,对于pH> 3,COSAC表面上的带负电位点的数量增加,并且金属吸附变得更重要。 | |
| 在大多数关于金属离子的吸附到活性碳上吸附摄取报道的研究的示出了用于初始pH为约5 [最大14 - 16 ]。 | |
| 即使在低pH下,镉和铅的重要吸收也可能与COSAC的表面官能团对这两种金属离子的亲和力高于对铜和镍的亲和力有关。 | |
| 基于这些结果,这些金属离子吸附的最佳初始pH被认为是5,并且在该pH下进行动力学和平衡实验。 | |
| 不同初始浓度下的吸附动力学 | |
| 平衡时间:研究了不同初始浓度下达到铜,镍和铅吸附平衡所需的时间。对于这些实验,固液比6gL -1和pH 5保持恒定。结果如图2所示。如图所示,Cu(II),Ni(II)和Pb(II)离子在COSAC上的吸附随着时间的推移而增加,直到约200分钟,之后变得恒定。对于所有研究的初始浓度,吸附过程在270分钟内达到平衡。随着金属离子溶液初始浓度从0.5到1.5 mM的变化,Cu(II),Ni(II)和Pb(II)离子的吸收量从0.061 mmol.g -1增加到0.101 mmol.g -1,从0.052mmol.g -1至0.090mmol.g-1和0.0701mmol.g -1至0.109mmol.g -1。 | |
| 根据这些结果,所选择的进一步实验的接触时间为10小时,以确保达到平衡。 | |
| 动力学:吸附机理取决于吸附剂的物理和化学特性以及流体 - 固体质量传递过程。将动力学数据提交给伪第一和伪第二动力学模型[17 ],以确定哪个模型更适合实验数据。 | |
| 使用的伪第一顺序是Lagergren的伪顺序,由下式给出: | |
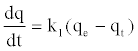 (4) (4) |
|
| 等式(4)在条件(t = 0,qt = 0)和(t = t,q = qt)中的积分给出: | |
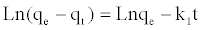 (5) (5) |
|
| 其中k 1是伪一阶的速度常数(min -1)。 | |
| 伪二阶或Ho方程由流动表达式给出: | |
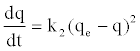 (6) (6) |
|
| 通过将方程(6)积分到边界条件(t = 0,q = 0)和(t = t,q = qt),我们得到: | |
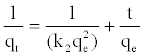 (7) (7) |
|
| 其中k 2是伪二阶的速度常数(gmmol -1 min -1)。 | |
| 表1中列出了伪一阶和伪二阶理论拟合参数。结果表明,伪一阶模型计算的金属吸附量(q e,cal)与实验测量值大不相同,而这些从伪二级动力学模型获得非常接近实验数据和相关系数值相当好(0.985≤[R 2 ≤0.999),比那些高得多伪一阶模型的发现,这表明通过伪二级动力学模型可以很好地描述吸附系统。图2说明了COSAC对Cu,Ni和Pb吸附动力学实验结果的拟二阶模型的拟合。 | |
| 表2一方面显示,对于所有研究的金属,k 2值随着初始浓度的增加而降低。因此,可能是由于金属阳离子本身之间以及金属阳离子和H +质子之间竞争的增强导致相同的活性位点。另一方面,对于相同的初始浓度,对于每种金属离子发现的k 2值按以下顺序降低:Pb(II)> Ni(II)≥Cu(II)。这表明COSAC比镍和铜更容易和更快地吸附铅。 | |
| 吸附等温线:进行平衡吸附研究以确定COSAC的最大金属吸附容量。在pH5.0和30℃下测定的Pb(II),Cd(II),Ni(II)和Cu(II)离子的实验平衡等温线如图3所示。使用通常使用的Langmuir和Freundlich模型评估等温线[ 18 ]。 | |
| 图3显示了Langmuir和Freundlich模型拟合的实验等温线数据,该模型吸附了橄榄石活性炭在30°C和pH下从水溶液中吸附Pb(II),Cd(II),Ni(II)和Cu(II)金属离子5.相应的Freundlich和Langmuir参数和相关系数在表3中重新分组。 | |
| 等温线属于Giles分类的L型[ 19 ],描述了高吸附质 - 吸附剂的相互作用,并且最初表明快速吸附倾向于在较高浓度下渐近。图3还显示,与镍和铜相比,能够结合Pb(II)和Cd(II)的位点在高金属离子浓度下饱和(达到平衡)。很显然,Langmuir模型拟合实验数据非常好,高相关系数(0.98≤[R 2 ;≤0.999)相比,由符合Freundlich线性方程(0.880≤式给出:R的那些2 ≤0.947)。表3还表明Langmuir方程给出的COSAC吸附容量的理论最大值(q max)与实验相当,发现Pb(II)≥Cd(II)> Ni(II)≥Cu(II)的顺序降低。这种趋势与金属离子半径(r i)的顺序相符。水化能但与表4中列出的其他特性值不匹配.Pb(II)具有最大的离子半径(1.19A°),其次是Cd(II)(0.97A°),Ni(II)( 0.72A°)和Cu(II)(0.69A°)。对于大的非水合离子,由于电荷更加分散,因此水合水的保持力较弱。离子半径越大,离子的吸附越强,因为离子的水合能力越小,导致离子和水相的结合越弱。Pb(II)和Cd(II)对Ni(II)和Cu(II)的吸附偏好也可能是由于水合能的差异[20 ]。 | |
| 与吸附剂能量有关的亲和常数K L遵循以下顺序:Cu(II)(24.302 l.mmol -1)> Pb(II)(14.091 l.mmol -1)> Cd(II)( 12.068 l.mmol -1)> Ni(II)(6.609 l.mmol -1)。这些结果表明,由于其相对较高的水合能,可能并非COSAC表面上的所有结合位点都可用于Cu(II)结合[ 20 ]。 | |
| 吸附剂吸附重金属的能力反映在K F Freundlich常数中。该参数的值遵循COSAC的最大实验容量给出的逆序,以去除金属离子(Cu(II)> Ni(II)> Cd(II)> Pb(II))。此外,Freundlich模型的非常高的n值反映了吸附物和吸附剂之间的高亲和力,并且还表明存在化学吸附过程。我们还可以注意到铜吸附的最高强度,这突出了COSAC对这种金属的巨大亲和力。 | |
| 与研究相同金属离子吸附的其他活性炭相比,吸附顺序从一种吸附剂强烈变化到另一种吸附剂。Ucer等。[ 14 ]发现Cu(II)金属离子比Cd(II)更多地吸附在单宁酸活性炭上,并且与金属离子的电负性有关。对于铜和镉,Lo等人发现了同样的趋势。[ 6 ],当他们研究金属离子吸附到竹子活性炭上时。发现吸附选择性按以下顺序降低:Pb(II)> Cu(II)> Cd(II)。吸附容量顺序由Faur-Brasquet等人确定。[ 16],在活性炭布上遵循Cu(II)> Ni(II)> Pb(II)的趋势,由于使用的活性炭是微孔吸附剂,当离子直径变小时,金属离子容易通过吸附位点。根据该顺序,Cu(II)必须具有小于Ni(II)和Pb(II)的离子直径。这与我们的实验结果不同。这些作者解释了基于离子半径的吸附差异,Pb(II)的大离子半径与Cu(II)相比诱导了吸附位点的快速饱和,因为空间过度拥挤因此可用于Cu(II)的表面然后,离子大于Pb(II)。Gao等人给出了相同的解释。[ 20当他们研究去除氧化碳纳米管上的重金属离子时; 吸收量遵循以下顺序:Cd(II)> Cu(II)> Ni(II)。而由Ricordel等人确定的与铅,镍和镉在花生壳碳上的最大吸附有关的顺序。[ 18 ],发现所用重金属的离子直径顺序为:Pb(II)> Cd(II)> Ni(II)。如表4所示,铅是具有大离子半径的金属,一些作者报道,具有较大离子半径的金属的吸附高于具有较小离子半径的金属(表3)。 | |
| 似乎吸附亲和力顺序和吸附量的差异不仅与金属离子性质有关,而且与吸附剂的物理 - 化学性质(形态,表面积,孔隙破坏,官能团)有关。其原因在于,作为一种吸附物的良好吸附剂的物质可能不是另一种吸附物的良好吸附剂(表5)。 | |
| 表5列出了不同吸附剂对所研究金属的最大吸附容量的比较,数据已在不同条件下收集。可以看出,对于Ni(II),Cu(II),Cd(II)和Pb(II)离子,COSAC分别具有相对高的吸附容量13.54,14.55,60.02和112.35mg.g -1。因此,COSAC具有从水溶液中去除这些金属离子的巨大潜力。 | |
| 从表5可以看出,金属离子的吸附量不同于一种活性炭,这部分是由于官能团,比表面积,孔容,微孔体积,平均直径等的差异。 。 | |
| 对于研究的活性炭,表1表明酸性官能团占主导地位,最重要的化合物是羰基(2.720 meq.g -1),而羧基仅存在0.100 meq.g -1。 | |
| 许多研究人员报告了吸附容量为重金属离子[酸官能团的重要性效果6,21,22 ]。Kadirvelu等。[ 15 ]表明吸附剂上的羧基可以在Cu(II),Pb(II)和Ni(II)的吸附中起重要作用。Faur-Brasquet等人发现的结果。[ 16 ],当他们研究将Cu(II)和Ni(II)去除到三种活性炭上时; 表明具有高羧酸官能度和较低pH pzc的活性炭对铜和镍金属离子的去除非常有效。 | |
| Lo等人。[ 6],比较两组活性炭的去除效率; S1M1和S2C1,基于比表面积,微孔体积和平均孔径的差异。结果表明,对于同一组活性炭,具有较大比表面积,孔容和微孔面积的碳可以获得重金属离子的吸附容量和去除效率。然而,当我们比较两组不同的活性炭时,这些解释并不总是正确的。当比较表5中显示的结果时,我们可以得出结论,重金属离子的吸附取决于吸附剂及其通过不同氧化剂的制备,这些氧化剂影响表面积,孔隙分布,并给出形成的官能团的酸性或碱性特征。在吸附剂表面上。23 ],和碳研究无论是从橄榄核衍生的和由氧化正磷酸。 | |
| 结论 | |
| 通过吸附在使用磷酸(COSAC)的热化学过程产生的橄榄石活性炭上去除水溶液中的重离子金属。 | |
| 在不同的初始pH,接触时间和初始离子浓度下评价了吸附剂的吸附性能,并根据吸附剂的物理和化学性质讨论了结果。得到的结果表明,金属吸附是pH依赖性的,并且在初始pH值为5时发现最大吸附。吸附平衡很快,并且在所研究的三种不同初始浓度下4小时后达到吸附平衡。COSAC上金属吸附的动力学遵循伪二级速率表达。与Freundlich模型相比,Langmuir模型更好地拟合了平衡吸附数据,COSAC的吸附容量依次降低:Pb(II)≥Cd(II)> Ni(II)≈Cu(II)。用磷酸浸渍赋予酸性官能团的COSAC特征(低pH值)pzc),高表面积和发达的微孔。与其他吸附剂相比,所有这些特性使COSAC成为去除重金属离子的有希望的吸附剂。 | |