发布日期:2018-10-09 17:21 来源:活性炭网 作者:活性炭网 浏览数:
在这项工作中,通过磷酸(1:3)和改性活性炭茎叶(MACS)的化学活化,从干燥的水葫芦茎和叶(DS,DL)制备的活性碳茎和叶(ACS,ACL)的潜力研究了用硝酸(1:1)从水溶液中除去铅
在这项工作中,通过磷酸(1:3)和改性活性炭茎叶(MACS)的化学活化,从干燥的水葫芦茎和叶(DS,DL)制备的活性碳茎和叶(ACS,ACL)的潜力研究了用硝酸(1:1)从水溶液中除去铅的MACL)。生产的碳样品合理产率约为75%,表面积显着(DS,DL,ACS和ACL,MACS和MACL分别为57.46,71.83,864.52,493.78,381.22和265.22 m2 / g)研究了各种操作参数,溶液pH值(1~6),铅离子初始浓度(50~400 mg / l),接触时间(2~250 min)的影响。和温度(298-323 K)。很明显,在pH 5下铅的最大吸附顺序为:MACS(175.63 mg / g)> MACL(164.56 mg / g)> DS(90.50 mg / g)> DL(66.60 mg / g)> ACS (36.00mg / g)> ACL(33.40mg / g)。这可能归因于改性活性炭上活性位点数量的增加。使用平衡数据进行分析Langmuir和Freundlich等温线。结果表明,Langmuir模型很好地拟合了实验数据。动力学结果表明,吸附过程遵循伪二阶模型,粒子内扩散是速率控制步骤。热力学研究表明,吸附是自发和吸热过程。使用约0.6M HCl实现从碳中吸附约90%的吸附铅。
水葫芦; 活性炭; 改性活性炭; 铅; 吸附
从水溶液中去除重金属污染物是最重要的环境问题之一,因为金属是生物耐火的,并且对许多生命形式有毒。水中重金属的各种来源是电池制造,基础钢,纸张,纸浆,金属电镀,皮革鞣制,农用化学品,石化产品以及化学制造,采矿和化肥工业。在重金属中,即使在低浓度下,铅也是毒性最大的元素之一。它会影响中枢神经系统,肾脏,肝脏和胃肠系统,并可能直接或间接导致贫血,脑病,肝炎和肾病等疾病[ 1]]。由于上述因素,有必要从废水中除去这些金属,以防止含有有毒金属的废水污染天然水体。从水和废水中去除金属离子的常用方法包括化学沉淀,氧化,还原,反渗透,膜过滤和吸附。在上述方法中,从水和废水中去除金属离子的有希望的方法是吸附,因为所用的吸附剂可以通过适当的解吸过程再生,并且它是高效和经济的[ 2 ]。
活性炭是最常用的从水溶液中除去金属离子的吸附剂之一。目前,活性炭被广泛用作废水处理中的吸附剂。它具有高度发达的孔隙度,内表面积大,机械强度相对较高。尽管其在工业中广泛使用,但活性炭仍然是昂贵的材料。因此,有必要研究和开发可用于水污染控制的低成本有效碳。表面电荷,表面官能团类型,比表面积和孔径分布等性质影响金属离子对活性炭的吸附能力。所有上述活性炭的物理和化学性质取决于所用的前体材料和活化方法[ 3 ]。
在本文中,将研究使用干燥水葫芦,碳化(茎,叶)和改性活性炭(茎和叶)作为从水溶液中去除Pb 2+的有效吸附剂的可能性。还研究了pH,初始Pb 2+浓度,温度和接触时间对吸附容量的影响。使用一级动力学,伪二级动力学和粒内扩散模型分析实验数据。此外,根据Langmuir和Freundlich方程分析平衡等温线数据。
材料和试剂
通过将1.5984g Pb(NO 3)2(由BDH提供)溶解在蒸馏水中制备含有1mg铅cm -3的铅的储备溶液,并将该溶液完成至1L量瓶的标记。通过用蒸馏水进一步稀释来制备较低浓度的铅溶液。通过将0.1g固体物质溶解在最少量的蒸馏水中制备的PAR(2-吡啶基偶氮间苯二酚)溶液0.1%(w / v),然后转移到100ml容量瓶中并用蒸馏水完成标记。使用的所有其他化学品均为分析级。
吸附剂的制备
干水葫芦(DS和DL)的制备:从埃及曼苏拉的尼罗河延伸的运河收集植物水葫芦。除去植物的根,同时用水洗涤叶子和茎,然后用蒸馏水洗涤,并在pH 10的0.25M EDTA中浸泡过夜,以除去吸附在植物上的任何金属离子(茎和叶)并用蒸馏水洗涤多次并在110℃的烘箱中干燥48小时,然后将干燥的茎(DS)和叶子(DL)研磨并储存在干燥器中直至用于吸附实验。
化学活性碳茎(ACS)和叶(ACL)的制备:将干燥相浸渍至其重量的3倍。用浓H 3 PO 4在室温下保持2天。然后在110℃的烘箱中干燥48小时,然后置于马弗炉(在不锈钢反应器中)中,在没有空气的情况下以加热= 10K / min的速率逐渐加热样品至550-600° C然后在此温度下保持3小时。冷却至室温后,用蒸馏水彻底洗涤得到的活性炭,直至上清液的pH稳定在约(pH = 6)。之后,将样品在110℃下干燥24小时。最后,将由茎(ACS)和叶(ACL)制备的活性炭研磨并储存在干燥器中直至用于吸附实验。
活性炭茎(MACS)和叶(MACL)的修饰:通过用浓硝酸(从67%浓HNO 3中 1:1稀释)进行表面氧化来修饰活性炭(ACS和ACL )。修改程序如下。将已知体积的1:1稀释的硝酸在110℃下加热。将适量的ACS或ACL以1g AC至5ml硝酸溶液的比例加入沸腾的硝酸溶液中。将其处理3小时以增加官能团的形成,例如羧酸。用蒸馏水洗涤残余物质直至上清液的pH变得稳定在约(pH = 6)。然后将使用硝酸的改性活性炭在120℃下干燥24小时,然后研磨并储存在干燥器中直至用于吸附实验。
批量吸附实验
通过将0.025g DS,DL,ACS,ACL,MACS和MACL添加到25ml溶液中来研究吸附等温线,其中初始浓度Pb(II)为5至400mg / L. 溶液的初始pH值为5.将悬浮液摇动2小时后,通过测量相应的PAR(2-吡啶基偶氮间苯二酚)络合物(PAR-Pb)的吸收来分析剩余的Pb(II)浓度。采用Dagnall等人提出的方法的改进,在520nm处。[ 4 ]。具体地,将10ml缓冲溶液(硼酸盐缓冲液pH = 10)加入到金属溶液中,然后加入1ml PAR(0.1g / 100ml),然后用蒸馏水加至25ml。吸附剂除去的Pb 2+量q e 提取百分比%E可以使用以下公式计算:
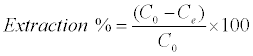 (1)
(1)
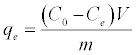 (2)
(2)
其中qe是吸附的Pb2 +的量(mg / g)。C o和C e分别是Pb 2+的初始和平衡液相浓度(mg / g)。V是溶液(L)的体积,m是所用吸附剂(g)的重量。
为了研究pH对Pb(II)吸附的影响,将0.025g吸附剂分散到含有250mg / L Pb(II)的25ml溶液中。使用0.01M HNO 3和0.01M NaOH 将溶液的初始pH值从1.5调节至6 。
通过使用含有约0.2g吸附剂的不同烧瓶在含有200mg / L Pb 2+的200ml溶液中进行动力学实验。在所需的时间间隔,从悬浮液中取出1ml等分试样,并如上所述通过分光光度法测定Pb 2+的浓度。
制备样品的表征
MACS,MACL,ACS,ACL,DS和DL的物理化学表征如下测定:使用烘箱干燥法测定水分含量,零电荷点(pH pzc),表面积由Brunauer Emmett和Teller的应用确定(BET)方程式为N 2在77k 的吸附 - 解吸等温线[ 5 ],如(表1)所示。通过电子显微镜检查的MACS,MACL,ACS,ACL,DS和DL的形态显示在图2中。所获得的SEM显微照片的检查清楚地表明不同吸附剂的多孔结构在放大率分别为1500x,3500x和1000x(DS和DL),(ACS和ACL)和(MACS和MACL)。类似样品的FT-IR光谱如图1所示。由于六方基团和吸附水的OH拉伸模式,所有样品在约(3373-3442cm -1)处显示宽带。由于脂肪族(CH),在(2849-2932 cm -1)处观察到肩部,并且对于所有样品都出现[ 6 ]。在1600 cm -1附近的带是由于芳香环中的C = C伸缩振动而观察到的样本。带(1711-1713 cm -1)对于MACL和MACS是由于层平面边缘上的羧基的拉伸振动[ 7 ]。出现在1580,1574,1240,1520,1608,1243,1530和1621cm -1的弱带是由于高度共轭的形成(C = O拉伸,羧基和羧酸酯部分的CO拉伸)[ 8 ]。
| 样品 | 水分含量 % | 表面pH值 | 表面积m 2 / g | 总孔容 | pH PZC |
|---|---|---|---|---|---|
| DS | 6.71 | 5.95 | 57.46 | 0.01 | 4.95 |
| DL | 5.1 | 6.13 | 71.83 | 0.03 | 4.80 |
| ACS | 3.88 | 4.50 | 864.52 | 0.52 | 4.05 |
| ACL | 2.64 | 4.10 | 493.78 | 0.31 | 4.05 |
| MACS | 9.13 | 3.60 | 381.22 | 0.43 | 3.38 |
| MACL | 7.89 | 4.00 | 365.22 | 0.29 | 3.36 |
表1:干燥的水葫芦(茎和叶),活性炭和改性活性炭(茎和叶)的特征。
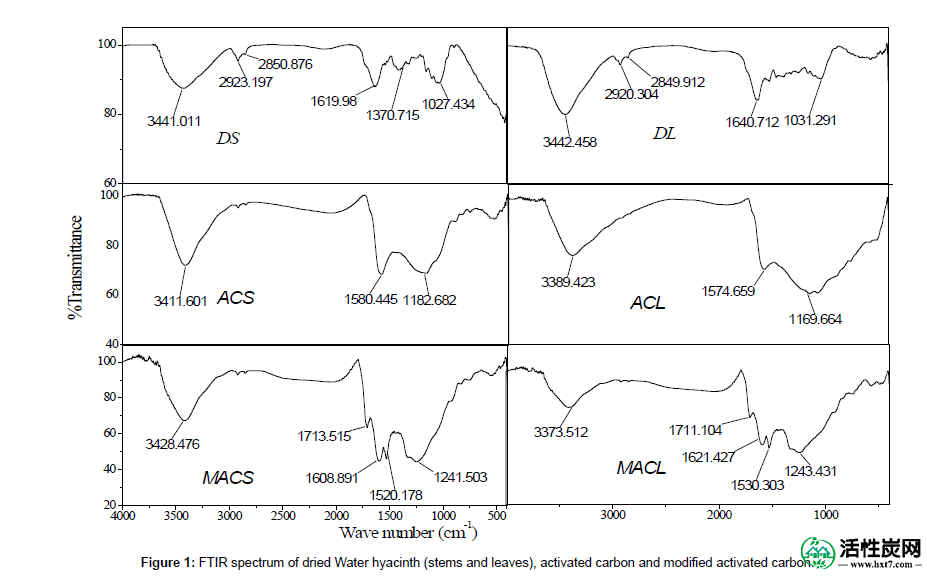
图1:干燥的水葫芦(茎和叶),活性炭和改性活性炭的FTIR光谱。

图2:(a)DS(b)DL(c)ACS(d)ACL(e)MACS(f)MACL的SEM照片。
吸附参数
pH的影响:为了优化pH值以获得最大的去除效率并避免Pb(II)的沉淀,在2至6的初始pH范围内进行吸附实验,如图3所示。。DS吸附量从21.04增加到102.50 mg / g,样品DL从17.10增加到68.04 mg / g,样品ACS从1.30增加到35.80 mg / g,样品ACL从0.6到32.30 mg / g在pH = 1时增加和5,分别。在低pH下,吸附剂的表面被水合氢离子包围,水合离子与金属离子竞争,这阻止金属离子接近吸附剂上的结合位点。随着pH增加,金属去除的增加可以基于表面位点的水合氢离子和金属物质之间的竞争减少来解释。在pH = 5.0时,(DS,DL,ACS和ACL)的吸附容量几乎达到最大值。因为铅的形态图显示在pH> 6.0时,[Pb(OH)] +,[Pb 3(OH)4 ] 等物种+,和[Pb(OH)2 ]将被产生[ 9 ]。为了保证真实地检测碳样品的吸附性能以及避免Pb(II)离子的沉淀,所有以下实验都在pH = 5.0下进行。
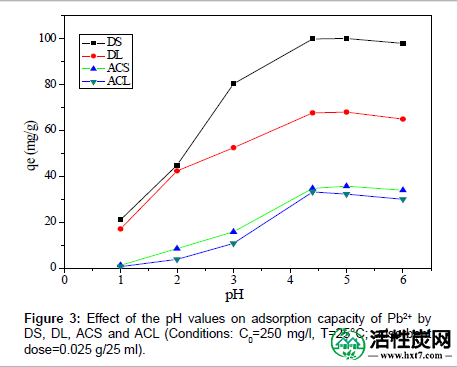
图3: DS值,DL,ACS和ACL的pH值对Pb2 +吸附容量的影响(条件:C0 = 250mg / l,T = 25℃;吸附剂剂量= 0.025g / 25ml)。
初始浓度对pb 2+摄取的影响
研究了初始浓度对吸附的影响,如图4和5所示。结果表明,随着初始浓度的增加,吸附容量增加。初始浓度可以提供克服液相和固相之间Pb(II)传质阻力的驱动力[ 10 ]。初始浓度较高,然后驱动力较高,因此吸附能力较高。
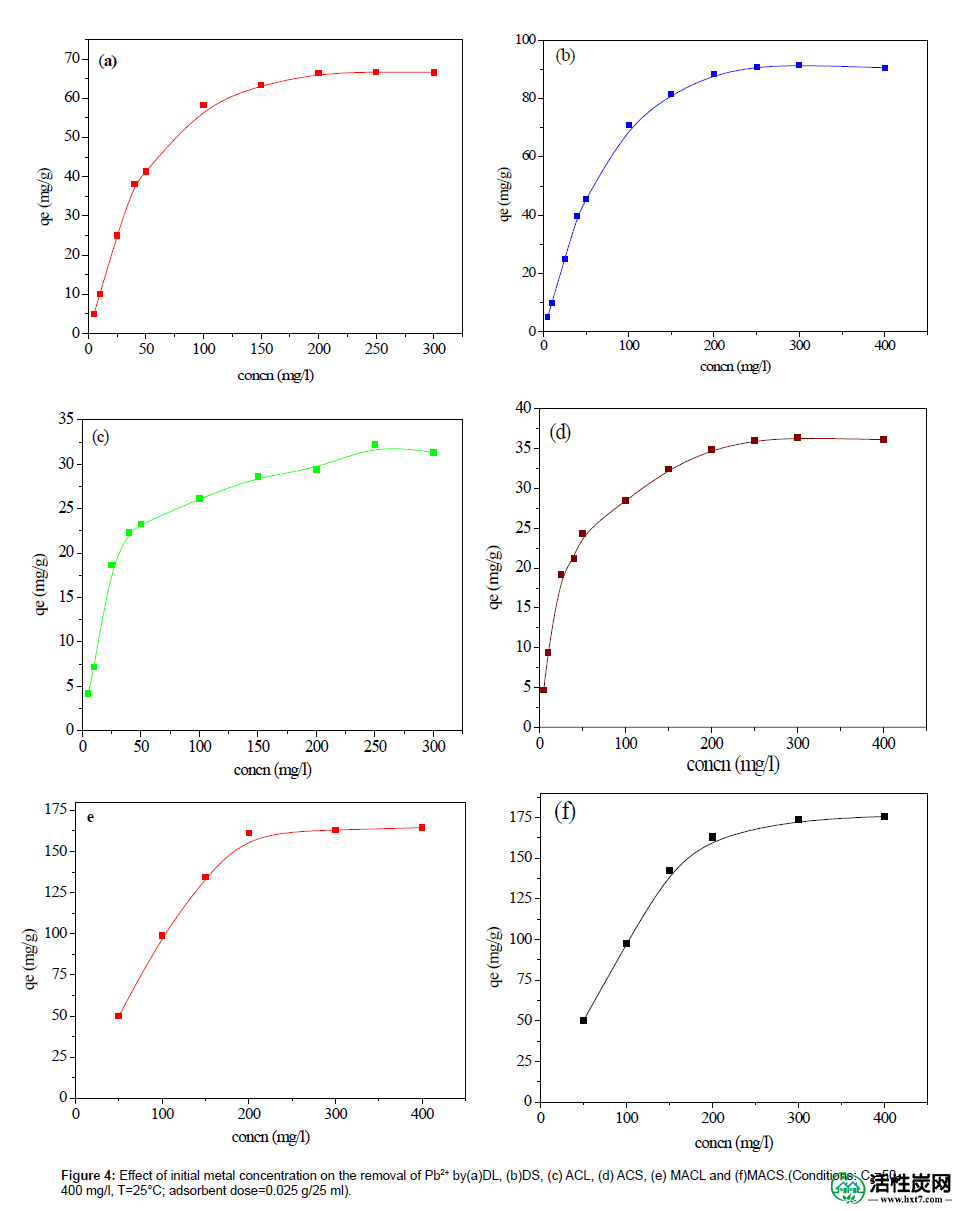
图4:初始金属浓度对去除Pb2 +的影响(a)DL,(b)DS,(c)ACL,(d)ACS,(e)MACL和(f)MACS。(条件:C 0 = 50-400mg / l,T = 25℃;吸附剂剂量= 0.025g / 25ml)。
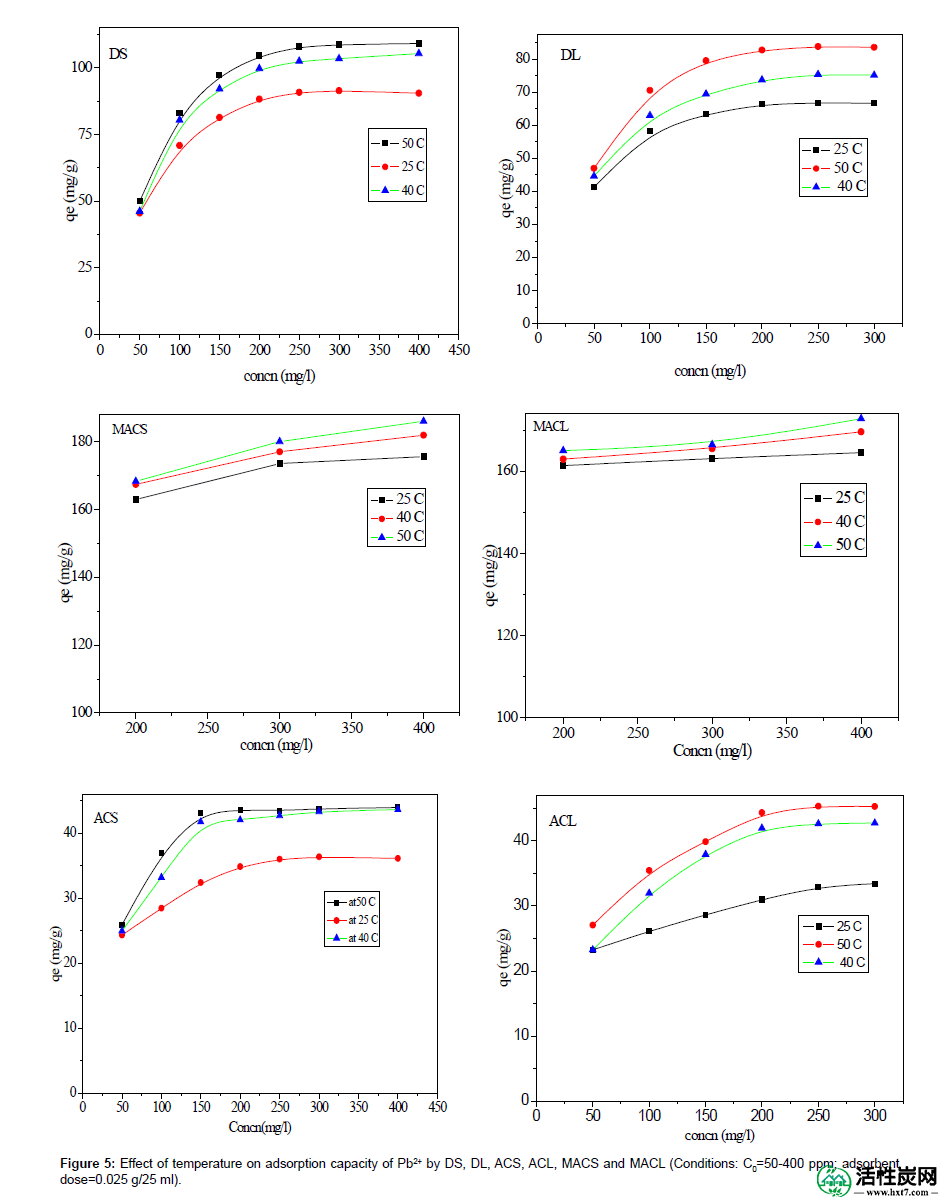
图5:温度对DS,DL,ACS,ACL,MACS和MACL对Pb2 +的吸附容量的影响(条件:C 0 = 50-400ppm;吸附剂剂量= 0.025g / 25ml)。
温度对吸附的影响
使用DS,DL,ACS,ACL,MACS和MACL在三种不同温度下研究溶液温度对Pb + 2去除的影响:298K,313K和323K。结果列于表2中,从表中可以明显看出,升高温度显着影响不同吸附剂从溶液中吸附的Pb2 +的量。吸附容量的增强可能是由于吸附质和吸附剂位点之间的化学相互作用或Pb 2+分子在吸附剂孔中的增加速率,这是由于在较高温度下溶液粘度降低和数量增加所致由于吸附剂表面活性位点边缘附近的一些内部键而产生的吸附位点[11,12 ]。
| 样品 | Q e(mg g -1) | ||
| 298 K. | 313 K. | 323 K. | |
| DS | 90.50 | 105.37 | 109.17 |
| DL | 66.60 | 75.14 | 83.54 |
| ACS | 36.00 | 43.00 | 44.00 |
| ACL | 33.40 | 42.72 | 45.25 |
| MACS | 175.63 | 181.96 | 186.07 |
| MACL | 164.56 | 169.62 | 172.79 |
表2:温度对Pb 2+的最大吸附容量的影响是DS,DL,ACS,ACL,MACS和MACL。
接触时间对吸附的影响
图6显示了接触时间对(a)DS和DL 去除Pb 2+的百分比的影响,(b)ACS和ACL,(C)MACS和MACL在25°C时使用1 g / L的吸附剂浓度在pH5时,Pb2 +的初始浓度为200ppm。很明显,Pb(II)的吸附量在吸附开始时迅速增加; 对于DS和DL ,相应的Pb 2+吸附剂的吸附容量超过65%发生在5分钟内,ACS和ACL在5分钟内发生超过88%,MACS和MACL在15分钟内发生约90%。MACS,MACL,ACS和ACL在60分钟后Pb 2+吸收几乎保持恒定,DS和DL在90分钟后因此可以认为90分钟是Pb(II)吸附的平衡时间。快的在初始阶段的吸附可能是由于较高的驱动力使金属离子快速转移到吸附剂颗粒的表面,以及未覆盖的表面区域和吸附剂上的活性位点的可用性。
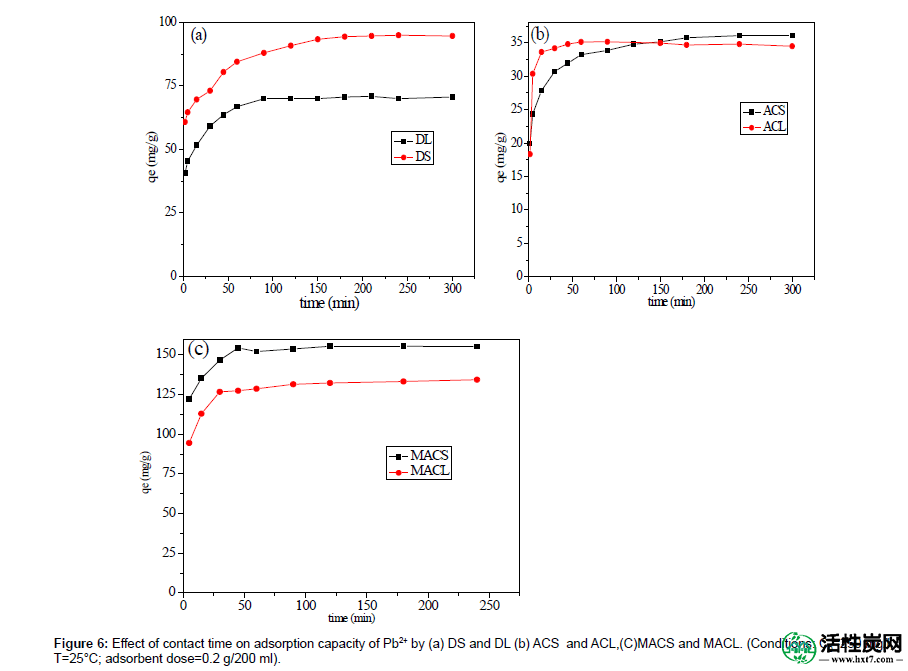
图6:接触时间对Pb2 +吸附容量的影响(a)DS和DL(b)ACS和ACL,(C)MACS和MACL。(条件:C 0= 250mg / l,T = 25℃;吸附剂剂量= 0.2g / 200ml)。
吸附剂用量的影响
DS,DL,ACS和ACL的量对Pb 2+去除率的影响如图7所示。可以清楚地看出,吸附剂剂量的增加有利于Pb 2+的去除。当吸附剂剂量从0.05增加到0.25 g时,DS,DL,ACS和ACL去除Pb 2+的百分比从48.40%增加到96.36%,从31.01%增加到95.63%,从17.9%增加到53.95%和从16.46%增加分别达到50.95%。吸附剂用量的吸附增加可归因于吸附剂表面积的增加和更多吸附位点的可用性。
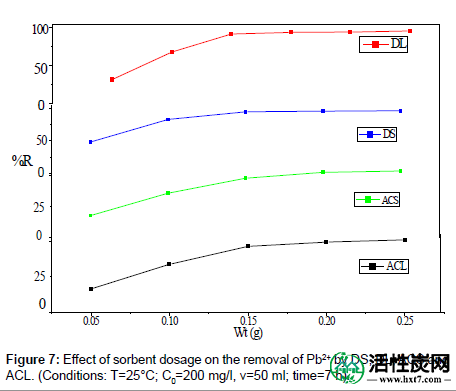
图7:吸附剂剂量对DS,DL,ACS和ACL去除Pb2 +的影响。(条件:T = 25℃; C 0 = 200mg / l,v = 50ml;时间= 7h)。
吸附等温线
吸附通常通过等温线描述,即吸附剂上吸附物的量作为其在恒定温度下的压力(如果是气体)或浓度(如果是液体)的函数。吸附等温线对于描述吸附物如何与吸附剂相互作用非常重要,因此它对优化吸附剂的使用非常重要。两种常见的等温线方程即,Langmuir和Freundlich模型中测试[ 13 - 15 ]。
Langmuir等温线假定具有均匀结合位点的表面具有等效的吸附能量,并且吸附物质之间没有相互作用。其数学形式如下:
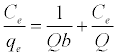 (3)
(3)
其中qe是平衡吸附量(mg g -1),C e是铅的平衡浓度(mg L -1),常数b与吸附能量(Lmg -1)有关,Q是Langmuir单层吸附容量(mg g -1)。Langmuir方程的基本特征可以用无量纲分离因子RL表示。
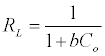 (4)
(4)
C 0是最高初始溶质浓度,b是朗缪尔吸附常数(L / mg),RL表示可逆的等温线类型(RL = 0),有利(0 <RL> 1),线性(RL = 1)或者不利(RL> 1)[ 16 ]。
Freundlich等温线是基于吸附位点和能量的指数分布的经验方程。它表示为:
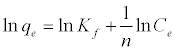 (5)
(5)
其中q e是平衡吸附量(mg g -1),C e是铅的平衡浓度(mg L -1),K f大致是吸附容量的指标,1 / n是吸附强度。ln q e与ln C e的线性图证实了Freundlich模型的有效性。
图8和9显示了Langmuir和Freundlich等温线在DS,DL,ACS,ACL,MACS和MACL上吸附Pb 2+的线性图。通过将Langmuir和Freundlich模型应用于实验数据获得的模型参数在表3和4中给出。可以发现,Langmuir模型得到的回归系数R2比Freundlich模型的回归系数R2更接近1,表明Langmuir等温线更符合DS,DL,ACS,ACL,MACS和MACL上Pb 2+的吸附。。另外,吸附Pb 2+的q max值根据Langmuir模型计算的不同吸附剂与实验数据完全相同。此外,获得的RL值在(0.000-0.086)的范围内,从而证实吸附是有利的过程。可以得出结论,单层Langmuir吸附等温线更适合解释Pb 2+在不同吸附剂上的吸附。
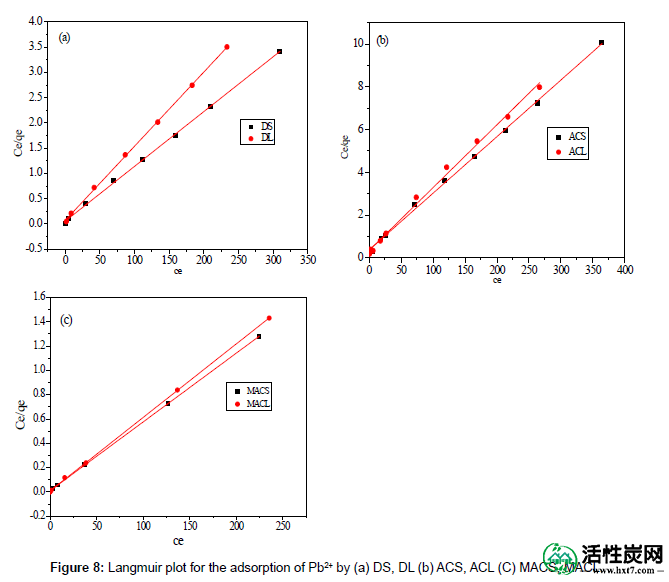
图8:通过(a)DS,DL(b)ACS,ACL(C)MACS,MACL 吸附Pb 2+的Langmuir图。
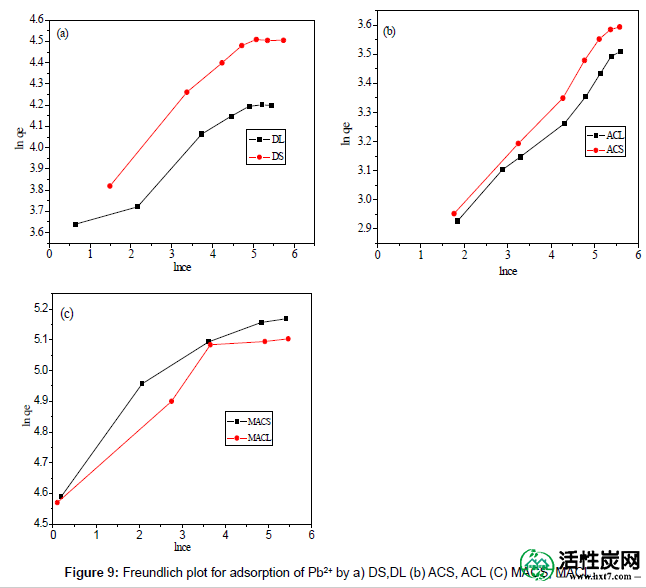
图9:通过a)DS,DL(b)ACS,ACL(C)MACS,MACL吸附Pb 2+的Freundlich图。
| 吸附剂 | Langmuir参数 | ||||
|---|---|---|---|---|---|
| R 2 | b(L / mg) | Q max,适合 | Q exp, | R L. | |
| MACS | 0.999 | 0.555 | 176.700 | 175.630 | 0.005 |
| MACL | 0.999 | 0.741 | 165.300 | 164.557 | 0.003 |
| ACS | 0.998 | 0.071 | 37.780 | 36.000 | 0.034 |
| ACL | 0.994 | 0.086 | 33.990 | 33.400 | 0.086 |
| DS | 0.999 | 0.199 | 92.170 | 90.500 | 0.012 |
| DL | 0.999 | 0.221 | 68.070 | 66.600 | 0.016 |
表3:通过DS,DL,ACS,ACL,MACS和MACL 吸附Pb 2+的langmuir等温线的参数。
| 吸附剂 | Freundlich参数 | ||
|---|---|---|---|
| R 2 | KF | 1 / n的 | |
| MACS | 0.773 | 97.710 | 0.121 |
| MACL | 0.894 | 101.510 | 0.099 |
| ACS | 0.992 | 13.900 | 0.175 |
| ACL | 0.987 | 14.040 | 0.153 |
| DS | 0.926 | 37.880 | 0.168 |
| DL | 0.948 | 33.860 | 0.132 |
表4:通过DS,DL,ACS,ACL,MACS和MACL 吸附Pb 2+的Freundlich等温线的参数。
吸附动力学
伪一阶方程和伪二阶方程:为了研究DS,DL,ACS,ACL,MACS和MACL 对Pb 2+吸附过程的控制机制,伪一阶和伪一阶引用二阶动力学模型来评估实验数据。伪一级动力学模型已被广泛用于预测金属吸附动力学。Lagergren [ 17 ] 建议吸附固/液体系。伪一级吸附模型的微分形式可表示为:
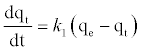 (6)
(6)
其中q e和q t(mg / gm)分别是在平衡和时间t吸附的铅的量,k 1是平衡常数(min -1)。等式(6)的积分和在t = 0时应用初始条件qt = 0,线性形式可以表示为[ 18 ]:
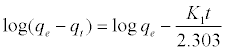 (7)
(7)
其中qe是时间t(mg / g)下Pb 2+的吸附吸收,k 1(min -1)是拟一级吸附的速率常数。log(q e -q t)与t的关系曲线应该是线性的; 从数据(图10)计算的参数k 1和R 2(相关系数)列于表5中。可以看出,伪一阶动力学模型的线性相关系数(R 2)很高。然而,实验q e值(q e,exp)与计算的q e之间存在很大差异值(Q E,CAL),其中所指示的准一级动力学模型拟合差为DS,DL,ACS,ACL,MACS和MACL的铅的吸附过程2+。伪二阶反应式的微分形式可以被写为[ 18,19 ]:
| 吸附剂代码 | q e exp。mg.g -1 | q ECAL。mg.g -1 | K1(min -1) | R 2 |
|---|---|---|---|---|
| MACS | 155.5 | 4.08 | 0.036 | 0.600 |
| MACL | 134.0 | 3.92 | 0.019 | 0.925 |
| ACS | 35.0 | 2.98 | 0.213 | 0.929 |
| ACL | 33.0 | 1.97 | 0.029 | 0.511 |
| DS | 92.0 | 3.53 | 0.018 | 0.993 |
| DL | 70.6 | 4.49 | 0.034 | 0.997 |
表5:通过DS,DL,ACS,ACL,MACS和MACL 吸附Pb 2+的一级模型的参数。
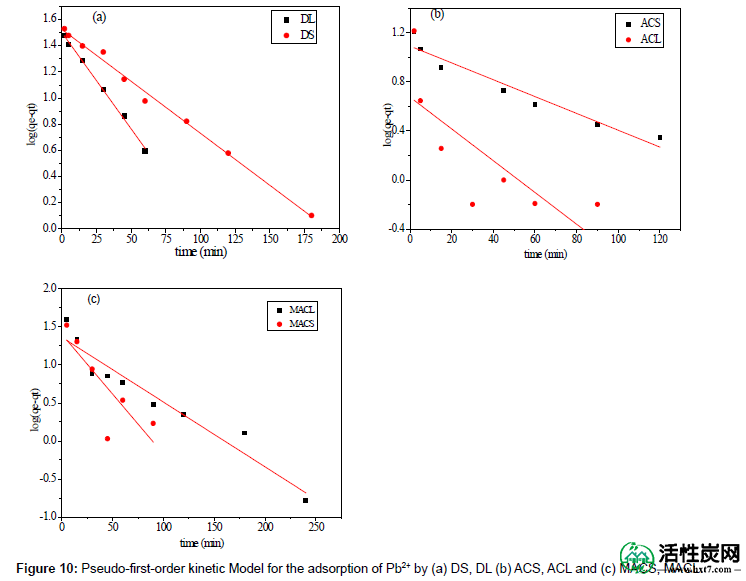
图10:通过(a)DS,DL(b)ACS,ACL和(c)MACS,MACL吸附Pb2 +的伪一级动力学模型。
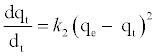 (8)
(8)
在考虑边界条件的积分后,该模型的线性化形式可表示为[ 18 ]
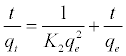 (9)
(9)
其中k 2(g mol -1 min -1)是假二阶吸附的速率常数。图11显示了对于DS,DL,ACS,ACL,MACS和MACL的Pb 2+的t / q与t的关系图。从表6可以看出,伪二阶动力学模型的R 2值均大于0.999,而且,伪二级动力学模型的q e,cal值均与q e,exp值一致。 。这表明DS,DL,ACS,ACL,MACS和MACL对Pb 2+的吸附过程可以通过伪二阶动力学模型很好地描述。这表明假二级吸附机制是主要的,因为吸附过程受化学吸附控制,化学吸附涉及通过溶剂和吸附物之间共享或交换电子的价力,因为既不是伪一级也不是二级。模型可以识别扩散机制,通过粒子内扩散模式进一步分析动力学结果,以阐明扩散机制。
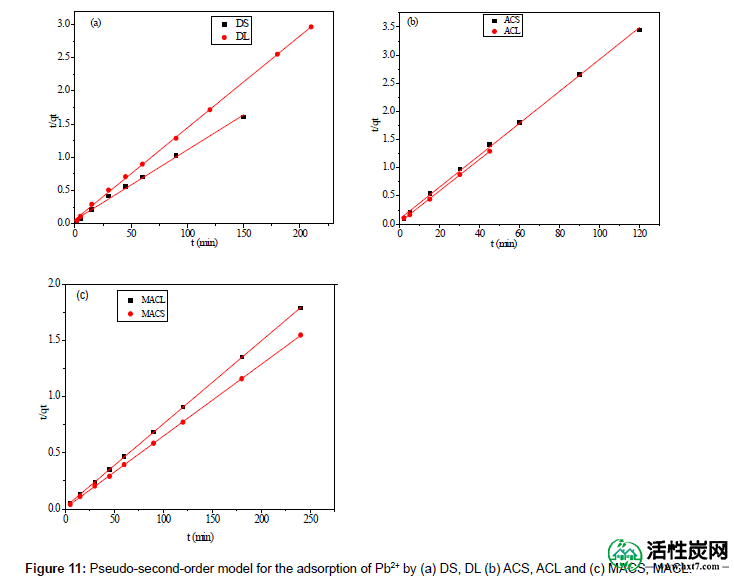
图11:通过(a)DS,DL(b)ACS,ACL和(c)MACS,MACL 吸附Pb 2+的伪二级模型。
| 吸附剂代码 | q e exp。mg.g -1 | q e cal。mg.g -1 | K 2克。mol -1 .min -1。 | R 2 |
|---|---|---|---|---|
| MACS | 155.5 | 156.49 | 0.041 | 0.999 |
| MACL | 134.0 | 135.50 | 0.027 | 0.999 |
| ACS | 35.0 | 35.34 | 0.009 | 0.998 |
| ACL | 33.0 | 35.84 | 0.002 | 0.999 |
| DS | 92.0 | 94.69 | 0.020 | 0.996 |
| DL | 70.6 | 72.31 | 0.003 | 0.999 |
表6:通过DS,DL,ACS,ACL,MACS和MACL 吸附200ppm Pb 2+的二级动力学模型的参数。
颗粒内扩散模型:吸附是一个多步骤过程,包括将溶质分子从水相输送到吸附剂固体颗粒表面,然后溶质分子扩散到孔内部,这很可能是是一个缓慢的过程,因此,速率决定。粒子内扩散参数K d(mg.g -1 h -0.5)由下式[ 20 ] 定义:
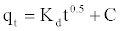 (10)
(10)
其中k d是颗粒内扩散速率常数(mg.g -1 h -0.5),C是常数。根据该模型,如果在吸附过程中涉及颗粒内扩散,则q t对t 0.5应该是线性的。根据等式(10),如果孔扩散是速率限制步骤,那么q t对t 0.5的曲线必须给出具有等于k d的斜率的直线,并且截距值C表示对外部的质量传递的阻力。液膜。
图12显示了通过DS,DL,ACS,ACL,MACS和MACL 吸附200 ppm Pb 2+的q t对t 0.5的曲线图,该图是多线性的,包含至少三个线性段,表明发生了三个步骤在吸附过程中。第一个更尖锐的部分是通过扩散通过边界层将Pb2 +从本体溶液输送到吸附剂外表面(膜扩散)。第二部分是Pb 2+从外表面扩散到吸附剂的孔中。第三部分是最终平衡阶段,其中Pb 2+ 被吸附在孔内表面的活性位点上,由于溶质浓度在溶液中越来越低,颗粒内扩散开始减慢。此外,曲线的线性部分没有通过原点,表明孔扩散不是控制吸附开始时总传质速率的步骤。
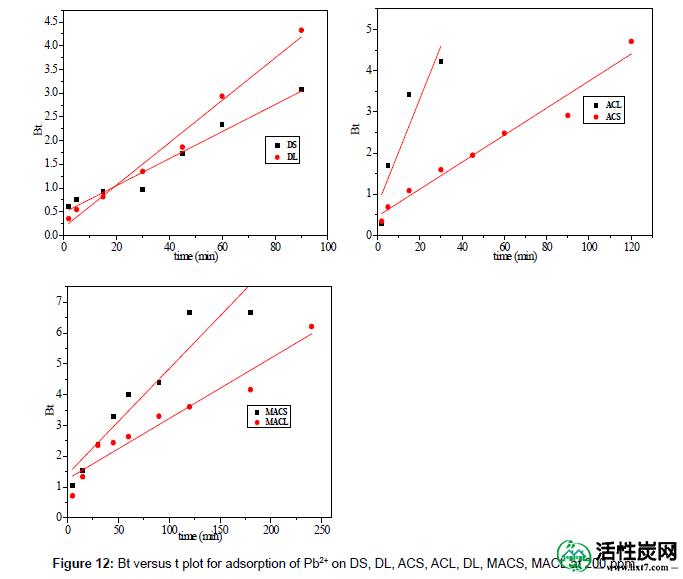
图12:在200ppm下DS,DL,ACS,ACL,DL,MACS,MACL上吸附Pb2 +的Bt对比t图。
在表7中,线性片段粒子内扩散模型的相关系数(R 2)在0.563和0.975之间,表明粒子内扩散不是唯一的速率控制步骤; 其他过程可以控制吸附速率。边界层效应可以控制第一线性段的时间段内的质量传递速率; 这一结论可以通过对博伊德模型数据的分析得到证实。
| 粒内扩散模型 | 博伊德模型 | ||||
|---|---|---|---|---|---|
| 吸附剂代码 | R 2 | Kp(mg g -1 min -0.5) | 截距 | 截距 | R 2 |
| MACS | 0.563 | 2.089 | 130.320 | 0.034 | 0.89 |
| MACL | 0.590 | 2.373 | 104.373 | 1.261 | 0.925 |
| ACS | 0.872 | 0.656 | 27.039 | 0.468 | 0.964 |
| ACL | 0.520 | 0.640 | 30.142 | 0.788 | 0.735 |
| DS | 0.954 | 2.874 | 58.700 | 0.479 | 0.958 |
| DL | 0.975 | 3.764 | 36.848 | 0.167 | 0.982 |
表7:通过DS,DL,MACS和MACL在200ppm下吸附Pb(II)的颗粒内扩散参数。
Boyd的模型表示为[ 21 ]:
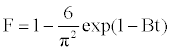 (11)
(11)
其中F是平衡的分数达到,在不同的时间,t和Bt是F的函数。
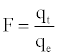 (12)
(12)
其中q t和q e分别是在时间t和平衡时的金属吸收(mmol g -1)。
方程。(18)可以重新排列为[ 22 ]
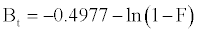 (13)
(13)
图13显示了B t的值由方程式计算。(13)并绘制时间t。该图的线性可以提供可用信息以区分颗粒内扩散和边界层效应(膜扩散)吸附速率。如果B t对t 的曲线是穿过原点的直线,那么吸附将适合层效应。该图仅在初始吸附期间是线性的并且不通过原点,表明外部质量传递是吸附开始时的限速过程,然后是颗粒内扩散。
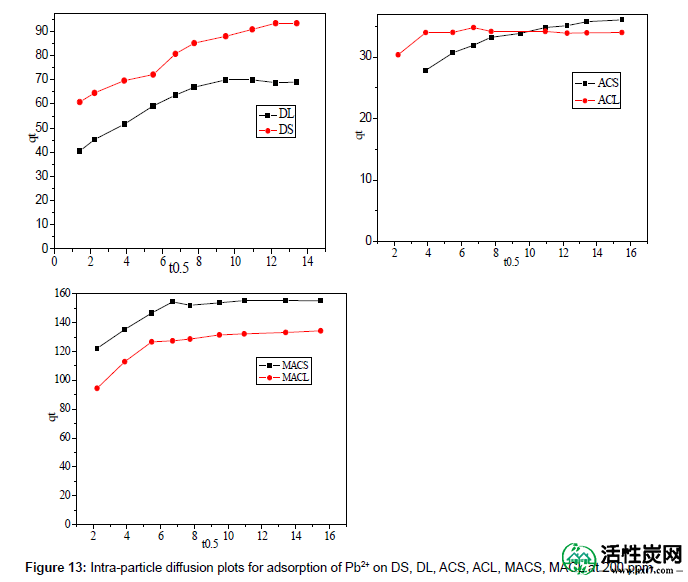
图13:在200ppm下吸附DS,DL,ACS,ACL,MACS,MACL上的Pb2 +的颗粒内扩散图。
热力学研究
从温度研究获得的数据用于热力学分析。使用以下方程[ 23 ] 确定热力学参数,例如标准自由能(ΔG°),焓(ΔH°)和熵(ΔS°)的变化:
范特霍夫方程
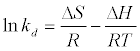 (14)
(14)
ΔG°=ΔH°-TΔS°(15)
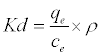 (16)
(16)
其中K d是吸附系数,ρ= 1000 g / L,使得尺寸Kd [ 24 ],ΔG°(J / mol)是吉布斯自由能的变化,ΔH°(J / mol)是Pb的焓变2+吸附,ΔS°(J / molK)是Pb 2+ 吸附的熵变,R是通用气体常数(8.314 J / mol K),T是绝对温度(K)。
通过绘制ln K d对1 / T的图(图14),可以分别从van't Hoff图的斜率和截距估计ΔH°和ΔS°的值。热力学参数在表8中给出。从表中可以清楚地看出,ΔG°的值对于DS,DL,ACS,ACL,MACS和MACL是负的。在各种温度下ΔG°的负值表明吸附过程的自发性质。ΔG°的值随温度升高而降低的事实表明自发效应的增加。对于所有吸附剂,ΔH°的正值表明吸附过程的吸热性质。此外,ΔS°的正值表明在DS,DL,ACS,ACL,MACS和MACL 吸附Pb 2+期间固/液界面的随机性增加。
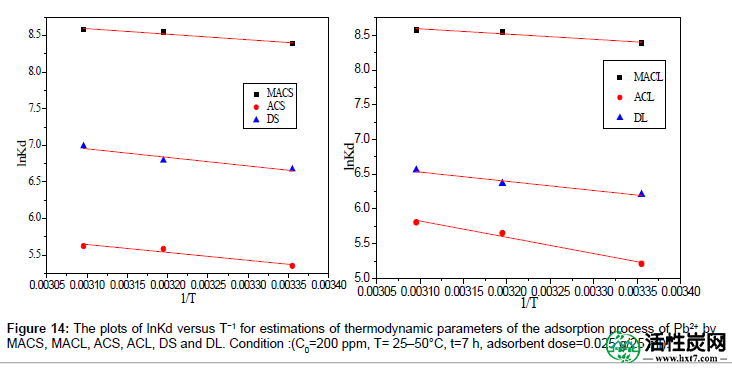
图14:通过MACS,MACL,ACS,ACL,DS和DL估算Pb2 +吸附过程的热力学参数的lnKd与T-1的关系图。条件:(C0 = 200ppm,T = 25-50℃,t = 7h,吸附剂剂量= 0.025g / 25ml)。
| AdsorbentCode | ΔH°(KJ / mol) | ΔS°(KJ / mol K) | ΔG°(KJ / mol) | ||
|---|---|---|---|---|---|
| 298 K. | 308 K. | 318 K. | |||
| MACS | 14.599 | 0.091 | -12.49 | -13.85 | -14.76 |
| MACL | 16.284 | 0.100 | -13.52 | -15.02 | -16.00 |
| ACS | 8.970 | 0.075 | -13.49 | -14.63 | - 15.38 |
| ACL | 11.190 | 0.109 | -21.29 | -22.93 | -24.02 |
| DS | 9.710 | 0.088 | -16.51 | -17.83 | -18.71 |
| DL | 10.990 | 0.088 | -15.35 | -16.67 | -17.56 |
表8:在不同温度下MACS,MACL,ACS,ACL,DS和DL 吸附Pb 2+的热力学参数。
解吸研究
为了实现实用和经济的吸附,要求有希望的吸附剂不仅具有高吸附容量而且具有再循环使用的再生能力。使用热活化来再生吸附剂可能需要高能量并且在每个循环中导致5-10%的吸附剂损失。因此,研究试图使用化学再生吸附物解吸[ 25]。通过破坏金属离子的配位并随后从活性炭表面释放到解吸介质中,使用HCl作为解吸剂解吸Pb。为了研究不同吸附剂的解吸能力,将0.025g不同的吸附剂引入到pH5的25ml 200ppm铅溶液中。当吸附达到平衡时,测量溶液的金属离子浓度,然后,收集负载铅的吸附剂并用25ml×M HCl处理以除去吸附的Pb2 +。与不同浓度的HCl解吸铅有关的结果示于表9和10中。结果表明,HCl浓度增加。解吸也增加但用0.6M HCl保持恒定。
| 吸附剂代码 | qe吸附 | qedesorped | %解吸 |
|---|---|---|---|
| MACS | 155.0 | 81.49 | 52.57 |
| MACL | 134.0 | 76.58 | 57.15 |
| ACS | 33.9 | 18.70 | 55.08 |
| ACL | 30.9 | 21.04 | 68.10 |
| DS | 88.2 | 50.00 | 56.70 |
| DL | 64.7 | 49.52 | 76.55 |
表9:吸附200ppm后使用0.3M HCl对铅的解吸效率。
| 吸附剂代码 | qe吸附 | qedesorped | %解吸 |
|---|---|---|---|
| MACS | 155.0 | 126.27 | 81.46 |
| MACL | 134.0 | 117.40 | 87.62 |
| ACS | 33.9 | 30.54 | 90.08 |
| ACL | 30.9 | 28.64 | 92.68 |
| DS | 88.2 | 74.84 | 84.85 |
| DL | 64.7 | 56.17 | 86.82 |
表10:吸附200ppm后使用0.6M HCl对铅的解吸效率。
吸附剂对Pb 2+吸附容量的比较
表11列出的铅的最大吸附容量的比较2+先前用于铅的吸附在这项研究中与各种吸附剂上获得的DS,DL,ACS,ACL,MACS和MACL 2+[ 26,27 ]。MACS和MACL具有比文献中报道的大多数其他吸附剂更高的吸附容量,表明它可能有可能从水溶液中除去Pb 2+。
| 吸附剂 | qe(mg / g) | 参考。 |
|---|---|---|
|
DS DL ACS ACL MACS MACL |
90.50 66.60 36.00 33.40 175.63 164.55 |
这项工作 |
| 菱铁矿壳聚糖 | 8.58 | [27] |
| 陨铁 | 12.43 | [26] |
| 稻壳灰 | 12.63 | |
| 高岭土 | 19.27 | |
| 数据有点碳 | 30.66 |
表11: Pb 2+对各种吸附剂的吸附容量的比较。
基于该结果,很明显,由于改性表面上羧基数量的增加,用硝酸改性水葫芦活性炭实现的铅去除值高于干水葫芦和活性炭。活性炭。该去除方法的主要优点包括(i)简单性,(ii)成本效益,(iii)快速性,和(iv)更高的有毒汞离子去除效率。根据本研究的实验结果,可以得出以下结论:发现吸附过程是pH依赖性的,Pb 2+的最大吸附容量是pH5。发现Pb 2的程度+随着初始浓度和接触时间的增加,吸附量增加,直至达到平衡。Pb 2+MACS,MACL,ACS和ACL在60分钟后和DS和DL在90分钟后几乎保持不变。基于伪一级,伪二级和粒子内扩散,对DS,DL,ACS,ACL,MACS和MACL进行铅吸附的动力学研究。数据表明,铅在所有吸附剂上的吸附动力学遵循不同铅浓度的拟二级模型。使用Langmuir和Freundlich等温线分析平衡数据,并确定每个等温线的特征参数。结果表明,Langmuir等温模型对实验数据有较好的相关性。热力学研究表明吸附过程是一个吸热过程。Pb 2+的解吸附 通过破坏金属离子的配位和随后从活性炭表面释放到解吸介质中,使用0.6M HCl作为解吸剂进行了研究。
(责任编辑:活性炭网)