发布日期:2018-11-17 08:38 来源:活性炭网 作者:活性炭网 浏览数:
开发了一种涉及由廉价,可重复使用的活性炭在水中促进的新型和高效好氧苄基氧化的一般策略。 该方法的应用已经在生物活性2-苯甲酰基苯并咪唑和2-苯甲酰基苯并恶唑衍生物的良性
苄基氧化在实验室和工业合成中都相当重要。氧化剂包括锰的大量VII,铬VI和我V传统上已经用于苄基氧化,但每个结果大量的不希望的废物1,2,3。分子氧是一种安全,廉价且环保的氧化剂。典型地,与O-苄基氧化2是极端的条件下,如高温或辐射下进行,因此形成自由基或单线态氧4,5。然而,大多数涉及温和的条件可以使用昂贵的和/或有毒的过渡金属,例如Pd,Ru和Rh组成的有氧氧化苄的6,7,8,9。
碳化学是有机合成和催化剂研究中最活跃和最有前途的研究领域之一。最近的报道已经表明纳米级碳催化剂在几个重要的反应和相关的化学工业过程中表现出色10,11,12,13,14。另一方面,活性炭(AC)广泛用作化学工业中的低成本吸附剂。一种新的有希望的方法已经使用AC / O报道2系统为苄醇或烷基芳烃(芴,呫吨和anthrones)到相应的羰基化合物的氧化15,16。值得注意的是使用非极性米在相对高温二甲苯在这些方法中,建议。
作为反应溶剂使用的水变为绿色化学一个有吸引力的研究领域17,18,19,20。尽管极大地促进了水有机氧化的领域而提出的,迄今已描述的由化学计量的高价碘或光催化在水中进行氧化苄只有几个例子21,22,23。在此,我们希望报告在水中活化的碳促进的好氧苄基氧化作为2-苯甲酰基苯并咪唑和2-苯甲酰基苯并唑的绿色合成方法。
在通过催化氢化预期制备5-甲基-2-(4-叠氮基苄基)苯并[d]咪唑以评估其生物活性期间,5-甲基-2-(4-硝基苄基)苯并[d]咪唑(1)无意中将10%Pd / C在乙醇中的混合物在空气中在室温下放置约12小时。大多数原料仍然未反应,但是,两种意想不到的产物,5-甲基-2-(4-硝基羟基苄基)苯并[d]咪唑(2)和5-甲基-2-(4-硝基苯甲酰基)苯并[d] 检测到咪唑(3)。使用2-(4-氯苄基)苯并[d]咪唑(4)作为底物和两种氧化产物5和6检查该反应。,获得(图1)。这些结果表明,2-苯甲酰基苯并[d]咪唑的苄基亚甲基可在Pd / C存在下在空气中氧化。
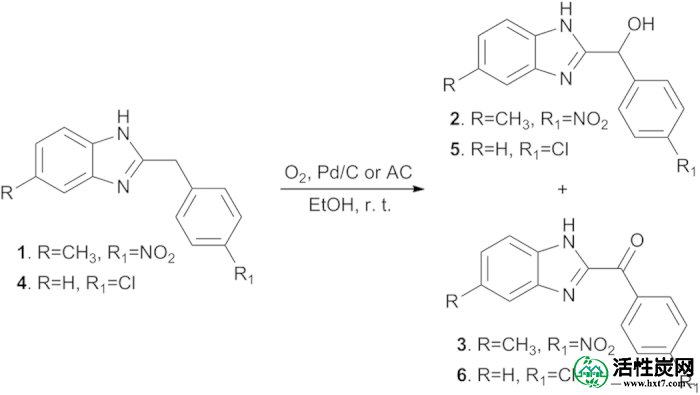
2-苄基苯并[d]咪唑的好氧苄基氧化。
为了研究Pd / C在该反应中的作用,化合物1和4分别在不存在Pd / C的乙醇中在空气中在室温下处理24小时,并且没有观察到氧化产物。然后使用各种Pd 0或Pd II物质进行反应,包括Pd黑,Pd [PPh 3] 4,Pd(OAc)2,PdCl 2和[Ph 3 P] 2 PdCl 2作为催化剂。但是,24小时后在反应混合物中没有检测到所需的产物。另一方面,Pd在4的氧化过程中从10%Pd / C浸出测量并且在反应混合物的相分离(Shimadzu,Kyoto,Japan,AA-7000,<1ppm检测限)24后未检测到浸出的钯物质。这些意想不到的结果促使我们检查活性炭在氧化中的有效性。
使用市售的AC代替Pd / C,重复反应并在6小时后清楚地获得苄基氧化产物。测试了三种类型的AC,分别得到了所需的产物,支持AC在这些反应中的有效性。结果表明,活性炭代替钯对2-苄基苯并[d]咪唑的好氧苄基氧化至关重要。
然后选择2-(4-氯苯甲酰基)苯并[d]咪唑(4)作为模型底物,以检查气氛,温度和溶剂对氧化产物(5和6)产率的影响。结果总结在表1中。正如所料,O 2下的氧化速率高于空气下的氧化速率(条目1和2)。温度从室温升至50℃导致产量增加(第3项)。通常,非极性米,在95℃或更高的二甲苯是在所报告的AC / O标准的反应条件2自由基氧化系统15,16。在我们的工作中,检查了各种有机溶剂,极性溶剂,特别是乙腈,比非极性溶剂显示出更多的改进(条目4-10)。为了优化环境特性并实现最小毒性,4的氧化在水中或在无溶剂条件下进行。尽管基质4和氧化产物在水中具有相对低的溶解度,但水上反应使得预期的产物平稳地进入(条目11)20。进一步研究了温度对这些水上反应的影响,并且将反应温度从50℃升高至85℃导致5和6的产率增加(条目12和13)。
| 条目 | 溶剂 | 自动取款机。 | 温度(°C) | 收率b 5 | (%)6 |
|---|---|---|---|---|---|
| 1 | 乙醇 | 空气 | RT | 5.2 c | 5.6 c |
| 2 | 乙醇 | RT | 7.9 c | 6.3 c | |
| 3 | 乙醇 | 50 | 8.3 | 5.9 | |
| 4 | 甲醇 | 50 | 11.1 | 1.4 | |
| 五 | 乙腈 | 50 | 12.0 | 6.1 | |
| 6 | 丙酮 | 50 | 7.1 | 8.2 | |
| 7 | 乙酸乙酯 | 50 | 11.2 | 7.9 | |
| 8 | THF | O 2 | 50 | 5.4 | 5.5 |
| 9 | 甲苯 | 50 | <1 | 5.3 | |
| 10 | 间二甲苯 | 50 | <1 | 3.4 | |
| 11 | H 2 O. | 50 | 6.7 | 4.2 | |
| 12 | H 2 O. | 70 | 11.4 | 8.4 | |
| 13 | H 2 O. | 85 | 31.6 | 29.5 | |
| 14 | 无溶剂 | 85 | 8.5 | 12.7 |
一个反应条件:4(2毫摩尔),AC III(阿拉丁公司,60mg)和溶剂(5mL)中。
b产量基于HLPC分析。
c分离产量12小时。
应该注意的是,反应管内的氧气压力也会影响产率。当在氧气氛下进行4的模式反应而没有密封时,反应速度低于密封条件下的反应速度,并且在24小时时最终产率6仅为约60%。
在反应优化期间,使用三种类型的AC,I,II和III以及石墨粉IV来检查表面积和Fe含量对产率的影响。如所示表2,II和III具有更大的表面积比我,表现出更高的活性。虽然III含有比II低得多的Fe ,但它们显示出几乎相同的反应性(条目1-3)。相反,使用IV与三种AC相比,表面积更小但Fe含量更高,反应后没有产生氧化产物(条目8)。因此,我们认为AC的表面积在反应中比Fe起着更重要的作用。氧化产物的产率也受AC量的影响。AC III的量从40mg / mmol降低至30mg / mmol而不影响5和6的产率,并且当使用20,10或5mg / mmol AC时(条目3-7),产率显着降低。
| 条目 | 类型 | 表面积(m 2 / g) | 铁(ppm) | 量(毫克/毫摩尔4) | 收率b 5 | (%)6 |
|---|---|---|---|---|---|---|
| 1 | 一世 | 600 | 2×10 5 | 三十 | 6.2 | 4.5 |
| 2 | II | 1100 | 5×10 5 | 三十 | 22.1 | 32.5 |
| 3 | III | 1100 | 0.02 | 三十 | 31.6 | 29.5 |
| 4 | III | 1100 | 0.02 | 40 | 28.2 | 32.1 |
| 五 | III | 1100 | 0.02 | 20 | 26.4 | 25.0 |
| 6 | III | 1100 | 0.02 | 10 | 9.8 | 21.5 |
| 7 | III | 1100 | 0.02 | 五 | 5.9 | 10.1 |
| 8 | IV | <50 | 5×10 6 | 三十 | <1 | <1 |
一基板4(2毫摩尔),AC(60mg的)和H 2 O(5mL)中,85℃,4小时。
b产量基于HLPC分析。
图2显示了时间对反应的影响。基质 4逐渐消耗,直到第20小时检测不到 .5小时的量增加到31.6%,然后小时4慢慢减少到小于1%。另一方面,产品 6从一开始就一直增加并达到最后98.8%。将反应时间延长至26小时不会提高反应产率。
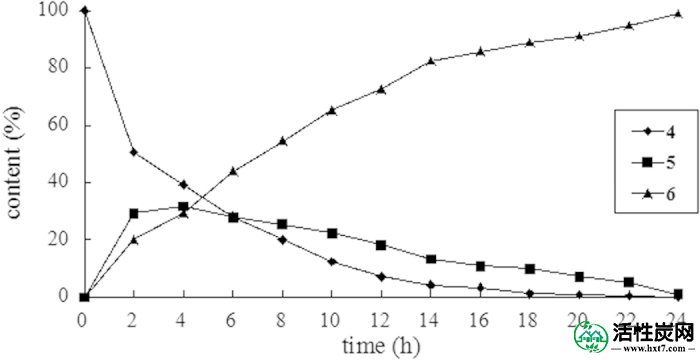
使用AC III的基板4,产品5和6的时间过程。通过HPLC分析确定产率。
观察结果表明,在好氧氧化过程中产生了5,它可以转化为相应的羰基化合物(6)。值得注意的是,在将烷基芳烃氧化成AC / O 2体系中相应的羰基化合物之前,从未记载苄醇(化合物5)。为了确认5至6的氧化转化率,通过在乙醇中用NaBH 4还原6制备的化合物5在O 2下在H 2 O 中用AC III处理。在85℃下保持12小时,以几乎定量的产率得到6。
随后在上述条件下利用4的反应测试AC的再循环。在每个循环中,通过过滤分离AC III并用EtOAc洗涤,然后直接用于下一循环而无需进一步处理。第二反应产生优异的收率(85%),第三反应产率略低(81%)。
一般地,需氧氧化的带O的机构2涉及自由基或单线态氧4,5。为了评价在此氧化自由基物种的存在,1.5当量自由基清除剂2,6-二-叔丁基-4-甲基苯酚(BHT)或2,2,6,6-四甲基-1-哌啶的(TEMPO)将反应混合物加入水或水/乙腈(1/1,v / v)中。发现氧化不受影响。此外,当加入1.5当量的单线态氧猝灭剂(二氮杂双环辛烷,DABCO)或避光时,反应显示不受影响。
详细的机理需要进一步的研究,但是,根据我们有可用的数据和在羰位置涉及去质子化的碱介导的有氧氧化说明25,26,27,氧化的可能机制,提出图3。吸收在AC上的起始材料(a)可以假设以(b)形式存在,在苄基sp 2碳上具有富电中心。可以使用计算建模来评估苄基位置的电密度(图S1)。将AC上吸收的分子氧亲电加成到烯胺互变异构体b上形成中间体两性离子过氧化物(c),随后通过质子的分子内或分子间提取将其转化为氢过氧化物(d)。将一部分d脱水,得到2-苯甲酰基苯并[d]咪唑(e),而另一部分d转化为2-羟基苄基苯并[d]咪唑(f)。通过类似的方法,将仲苄醇f氧化成相应的羰基化合物e。
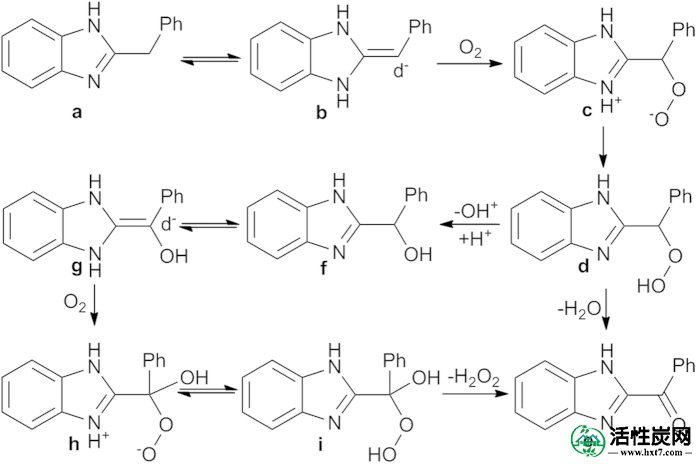
提出了水中AC对2-苄基苯并[δ]咪唑进行好氧苄基氧化反应的机理。
为了扩展该程序的范围并进一步理解氧化产率和苄基位置的电密度之间的关系,将优化的反应条件应用于许多2-苄基苯并咪唑,其是潜在CB 2激动剂的类似物28。如表3所示,在苯环上带有吸电子基团的2-苄基苯并[d]咪唑(条目4,8和12)通常比具有给电子基团的基质具有更高的收率(条目5,9和13) )。
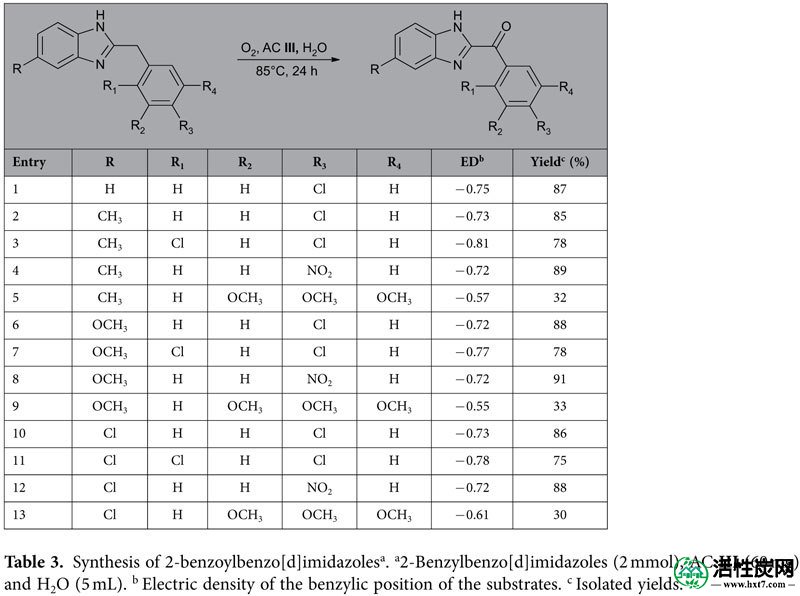
使用Jaguar 4.0软件利用B3LYP杂交密度功能方法进行底物苄基位置的计算电密度。表3显示氧化产率与苄型电密度密切相关。由于低电密度,带有三个OCH 3(条目5,9 和13)的基板通常具有较低的产率。对于在苄基位置具有较高电密度的条目3,7和11中的底物,反应被苯环的邻位上的氯基的空间位阻稍微阻挡。
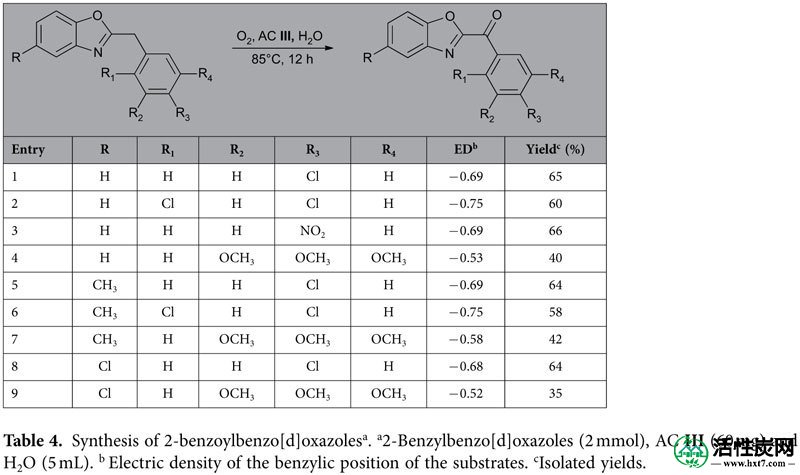
受上述结果的鼓舞,该方法用于合成2-苯甲酰基苯并[d]恶唑,它是脂肪酸酰胺水解酶抑制剂29的类似物。表4显示2-苄基苯并[d]恶唑是氧化过程的良好底物。取代基的电子和空间效应与2-苄基苯并[d]咪唑相似。由于低苄型电密度,带有三个OCH 3(条目4和13)的基板具有低产率。此外,我们认为,与表3中的苯并咪唑相比,苯并恶唑的相对较低的苄基电密度导致其较低的产率。
为了理解我们的方案相对于其他方案对2-苄基苯并咪唑的苄基氧化的效率,E因子(该方法的成本和环境影响)和每种方法的质量强度总结在支持信息的表S1中。比较氧化剂,溶剂和产率,可以清楚地看到现在的条件更有效,更清洁,并且相对更具可持续性。
总之,已经开发了由绿色溶剂水中的市售廉价,可重复使用的活性炭促进的好氧苄基氧化。它导致环境友好且有效的合成潜在生物活性分子的方法,包括2-苯甲酰基苯并咪唑和2-苯甲酰基苯并唑。在活性炭催化的好氧苄基氧化过程中,第一次发现了二级苄醇(5),它可以转化为相应的羰基化合物(6))在标准条件下。可重复使用的AC保持高效率,包括第3次运行而无需进一步处理。现有证据表明,这种氧化速率不受自由基清除剂,单线态氧猝灭剂和光照射的影响。初步研究表明,氧化机理可能涉及中间体氢过氧化物,并且最终羰基产物的一部分是通过仲苄醇中间体获得的。此外,氧化产率与使用Schrödinger软件计算的苄电密度密切相关。目前正在努力将该方法进一步应用于构建其他具有潜在价值的有机分子。
除非另有说明,否则所有材料均从市售来源获得,并且无需纯化即可使用。在GF254硅胶板上进行薄层色谱以监测反应,并在UV光下检查板。使用柱色谱(60Å,200-300目,青岛海洋化学或120Å,S-50mm,YMC Co.,Ltd。)或硅胶板(0.25mm层,青岛海洋化学)进行产物的纯化。 )用指定的溶剂。使用JASCO FT / IR-480 plus光谱仪获得IR光谱。1 H和13在Bruker ARX-300和Bruker AV-600光谱仪上以CDMS3溶液获得13 C NMR光谱,其中TMS作为内部参考。以四甲基硅烷的低场ppm和以Hz为单位的质子 - 质子偶合常数(J)报告化学位移。ESI-MS谱在Finigan LCQ Advantage MAX质谱仪上进行。
将底物(2mmol)和活性炭III(60mg)在水(5mL)中的混合物置于密封管(100mL)中。用分子氧吹扫系统并密封。将反应混合物加热至85℃并搅拌24小时。完成后,将反应混合物冷却至室温并过滤。浓缩滤液后,通过硅胶柱色谱分离产物,并通过MS,1 H-NMR和13 C-NMR分析。