发布日期:2018-11-16 10:53 来源:活性炭网 作者:活性炭网 浏览数:
AIMS 描述艾司西酞普兰在过量服用中的药代动力学和药效学(PKPD)及其对QT延长的影响,包括单剂量活性炭(SDAC)的有效性。 方法 数据集包括78次艾司西酞普兰过量事件(中位剂量,
艾司西酞普兰是新型选择性5-羟色胺再摄取抑制剂(SSRIs)和外消旋西酞普兰的S-对映体之一。艾司西酞普兰在抗抑郁药市场中的份额越来越大,重要的是确定它是否与过量服用西酞普兰有相似的毒性。艾司西酞普兰过量服用的报告表明,临床上最重要的影响之一是QT间期延长以及相关的尖端扭转型室性心动过速(TdP)[ 1 ]。然而,尚不清楚QT延长的风险在何种剂量具有临床意义。
定义过量服用药物的药代动力学(PK)和药代动力学 - 药效学(PKPD)对于了解剂量 - 浓度效应关系以及诸如去污等干预措施是否会影响这种关系非常重要。这已经针对有限数量的药物[ 2 - 6并且它表明去污对过量服用的不同药物有不同的影响,并且这并不总是转化为临床上重要的影响。药物过量管理的核心是基于所服用的药物,剂量和潜在毒性的风险评估。因此,建立过量服用量与毒性之间关系的PKPD模型可用于制定过量服用药物风险评估的临床指南[ 7 ]。
我们之前已经开发了基于西酞普兰过量服用PKPD的西酞普兰临床指南。这些指南确定了QT延长风险的剂量以及应该监测患者的时间以及去污的可能益处[ 8 ]。尽管依他普仑在过量服用时可能与西酞普兰相似,但在治疗剂量下它具有比其R-对映体更高的清除率[ 9 ]。此外,依他普仑对QT间期的影响可能与R-对映体不同,使得TdP的风险与西酞普兰的风险不同。
本研究旨在通过QT列线图[ 10 ]作为TdP风险指标,研究过量服用依他普仑的PKPD以及剂量与异常QT之间的关系。此外,该研究将确定SDAC是否对依他普仑的吸收和清除有益,以及这是否降低了QT异常的风险。这将为制定艾司西酞普兰过量治疗指南提供依据。
所有艾司西酞普兰过量给药三级毒理学单位的报告都被招募到该研究中。毒理学单位接受约30万人口的主要转诊,并提供24小时随叫随到的毒理学服务。该研究得到了当地人类研究伦理委员会的批准。所有患者均获得参与研究,收集血液样本和记录多个心电图(ECG)的书面知情同意书。根据临床毒理学家的说法,患者的治疗,包括使用去污。单剂量活性炭(SDAC; 50g,无添加剂)是本研究中唯一的去污方式。
在2003年10月至2008年9月期间,68名患者接受了78次escitalopram过量的临床数据。在来自29名患者的34次过量事件中可获得血浆浓度,并且在摄取后1.5至47.5小时采集总共104个样品,每次中位数为3个样品(范围1至9)。来自68名患者的77个演示文稿共有232个ECG可用,并且在报告的过量时间后1至54小时之间,在依他普仑过量(中位数为2,每个患者,范围1至8)之后记录了182个。剩余的50个心电图来自77例患者中的18例,这些患者来自另一种过量服用非心脏毒性药物的患者,或患者未服用过量服用时的入院时间。
病人的人口统计,治疗用途和依他普仑的剂量,使用由公知的患者以诱导CYP2C19,CYP2D6和CYP3A4的其它治疗药物,报告的剂量,用药历史的真实性,在提供共摄取药物和SDAC施用表1为PK分析中包括34次过量。在报告的中位剂量350mg(范围70至450mg)和摄入后中位时间1.9h(范围1.8至2.5h)后,SDAC以6次过量给药。在SDAC给药之前没有采集血液样品。
29例患者中34例艾司西酞普兰过量的特征可获得血浆浓度 - 时间数据
| 中位数(范围) | 患者人数 | 事件数量 | |
|---|---|---|---|
| 年龄(岁) | 27(16-51) | ||
| 男性/女性 | 5/24 | 5/29 | |
| 报告过量(mg) | 135(10-450) | ||
| Escitalopram处方 | 10(5-40)* | 22(76%)† | 26(76%) |
| 处方剂量(mg) | |||
| 准确度等级 | |||
| 0 | 3 | ||
| 1 | 12 | ||
| 2 | 15 | ||
| 3 | 4 | ||
| 共同摄入的药物 | 29 † | ||
| 2C19,2D6或3A4基板 | 11 | ||
| 2C19,2D6或3A4抑制剂 | 4 ‡ | ||
| 治疗性CYP3A4诱导剂 | 1 § | 1 § | |
| 活性炭 | 6(21%) | 6(18%) | |
| 艾司西酞普兰浓度 | 12-520微克升-1 |
表2包括用于PKPD分析的78个呈现的数据,尽管在一个患有药物浓度 - 时间数据的患者中没有ECG。数据包括人口统计学,报告的剂量,已知影响QT间期和SDAC给药的共同摄取药物。报告的中位剂量为280 mg(范围70-560 mg)后,在77次中有12次给予SDAC,而未给予SDAC的患者为130 mg(范围10-440 mg)。过量服用和SDAC给药之间的中位时间为1.7小时(范围1-2.6小时)。大多数ECG是在SDAC给药后服用的。五十八名患者在治疗上使用依他普仑。
在有可获得心电图数据的68名患者中,escitalopram过量服用77次的特征
| 中位数(范围) | 患者人数 | 事件数量 | |
|---|---|---|---|
| 年龄(岁) | 31(15-59) | ||
| 男性/女性 | 16/52 | 62分之16 | |
| 报告过量(mg) | 140(10-560) | ||
| 共同摄取的药物对QT有影响 | 3(4%) | 3(4%) | |
| 施用活性炭 | 12(18%) | 12(15%) | |
| 绝对QT间隔(ms) | 400(280-650) | ||
| RR间隔(ms) | 770(350-1580) |
依那西普仑的摄入剂量是根据(i)患者病史或来自重要他人的病史,(ii)片剂计数和(iii)任何其他可用信息(例如救护车记录)来估计的。通过评估历史的“真实性”,包括剂量的不确定性,如前所述[ 2]。Veracity按5分类分级评分:0优秀历史(回忆具有支持信息的片剂的确切数量,例如空包),1个良好的历史(使用一些支持信息获得的片剂的良好估计),2个不太可靠的历史(较少)由于镇静共同摄入者可获得的剂量的可靠估计但能够在入院时给出历史记录),3历史不佳(由于镇静共同摄入者导致过量或无过量服用)或4例非常差的病史(完全不可靠的病史,没有支持信息) )。本研究仅使用0至3类(表1))。对于准确度为0的过量服用,假定精确剂量。在准确度等级为1,2或3的过量事件中,允许增加添加剂和比例误差分量来改变剂量的不确定性。添加剂组分与片剂大小有关(例如10mg的倍数)。
从患者病史中获取过量服用的时间,并且在此时间内可能的范围由最早可能的摄取时间(例如与家庭成员的接触)和最近可能的摄取时间(例如救护车呼叫时间)提供。这用于解释时间的不确定性,如前所述[ 2 ]。在这项研究中,范围从5分钟到4小时不等。
通过高效液相色谱定量艾司西酞普兰。标准曲线(范围45-335微克升-1)具有大于0.999的相关系数。剂量标准化血浆浓度 - 时间曲线如图1所示。测得的浓度范围为12至520微克升-1。没有浓度低于1μgl - 1的定量限[ 11 ]。
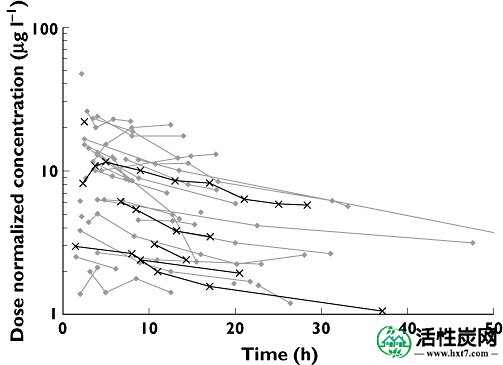
观察到剂量标准化浓度(至20mg的平均治疗剂量)与报告的给药时间。来自相同剂量事件的样品相连。符号表示患者是否未接受SDAC(•)或SDAC(×)治疗
所有QT间期均使用先前描述的方法在12导联ECG中手动测量[ 12 ]。从Q波的开始直到T波返回基线的点测量QT间期。在六个导联(三个胸部和三个导联导联)中测量QT间期并计算中值间隔。RR间期是从一个复合物中的R波到下一个复合物测量的,在导联II中至少六个循环。中值RR间期用于分析。
首先进行PK分析以建立数据的最佳PK模型,然后为PKPD模型保留相同的PK模型结构。作为34个场合与血浆浓度-时间数据[先前所述进行一个完全贝叶斯群体PK分析2,4,5 ]。使用三阶段分层模型将WinBUGS 1.4.3用于药代动力学数据建模。基于浓度 - 时间数据(图1)和西酞普兰过量药代动力学[ 2 ]的目视检查,假设没有滞后时间和一阶消除的一阶吸收。研究了加性,比例和组合残差模型。
先前的清除手段(CL),分布容积(V d)和吸收速率常数(K a)是从健康志愿者[ 9 ] 的先前药代动力学研究中引出的,使用反向分析技术[ 13 ]。弱先验用于受试者之间的变异性(BSV),因为只有一项先前的PK研究可用。对于所有服用依他普仑治疗的患者,使用如前所述的外推减法(ESM)和浓度 - 时间法(CTM)估计基线浓度[ 14 ]。通过结合准确性和modtime i,k来研究剂量和剂量时间的不确定性在模型中[ 2 ]。变量modtime i,k表示从针对第i个体的第k次的标称剂量时间的执行剂量时间的模型估计的时间差。
在评估基线浓度和给药不确定性后评估协变量,包括年龄,性别,共同摄入的药物,影响CYP2C19,CYP2D6或CYP3A4的治疗药物以及SDAC的影响。在过量患者中实际上难以获得患者体重并且不能包括在内。最初通过视觉检查评估表型协变量的影响,并且如果似乎存在影响,则协变量包括在模型中。SDAC的效果通过一个名为f CL-charc的因子改变个体间隙来评估,并且通过f F-charc因子吸收个体分数来评估SDAC的效果。。如果患者未给予SDAC,则该因子固定为1.如果差异大于20%,则认为其具有临床意义。
同时估计所有PK和PD参数,并且包括所有78个时间。最终的PKPD模型基于先前对西酞普兰的人口PKPD分析,之前已对此进行了详细描述[ 3 ]。假设心率依赖性具有等式1中所示的功率关系,并且允许每个个体具有单独的心率校正的QT间期(QT c,i),其中αi索引到第i个体。
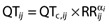
这里我们表示第i个患者对于RR ij和QT c,ij的第j次测量。预测的艾司西酞普兰浓度C或效应室中的浓度(C e)用于使用等式2从基线QT c,j 0 驱动变化QT c,ij。虽然我们展示了依他普仑的效应室浓度模型,但这也是模型开发的一部分。以前用西酞普兰建模[ 3 ]发现了一个线性函数,提供了QT c,ij的最佳描述。
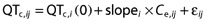
假设误差项εij是正态分布的。假设参数之间的主题差异是对数正态分布的。
PK参数的先验分布与PK模型相同。先前已经详细描述了用于QT间期的PD分析的先验的引发,并且假定西酞普兰的PKPD分析的先前分布适用于依他普仑[ 3 ]。QT间期来自先前对服用非心脏毒性药物过量的患者的研究[ 10 ]。假定所有参数进行日志正态分布,QT C,Ĵ 0与423方差0.0004的平均,斜率我具有零平均值(无影响)和3.57方差,α 我用的0.333和方差的平均0.09,最后从效果室消除速率常数(假设k eo)的平均值为1,方差为0.676。
可用于PD参数的唯一协变量是性别,年龄和共同摄入的药物。只有三次共同摄入影响QT间期的药物,因此不予考虑。通过对QT c的不同值进行建模来评估性别的影响,根据西酞普兰PKPD,允许每种性别和年龄的j 0影响QT c,i 0 [ 3 ]。
WinBUGS首先用于为患有浓度 - 时间数据的患者建立PK数据模型。然后同时建模完整数据集的PK和PD数据,WinBUGS估算了那些仅进行PD测量的患者的缺失浓度 - 时间数据。使用马尔可夫链蒙特卡罗(MCMC)模拟方法生成后验平均值和可信区间(CrI)。后验分布的CrI是在“老化”期后覆盖95%的MCMC样品的间隔。最初使用两个链进行建模,并在老化后进行10 000次迭代。假设老化已完成4000次迭代。最终模型运行了20万次迭代,保持每10 个样本。
在WinBUGS中提供的Gelman-Rubin诊断用于检查是否实现了收敛。对于PK和PKPD分析模型,选择决策是基于偏差信息准则(DIC)的减少,BSV在参数中的后验均值,残差误差幅度和协变量包含的估计效应的大小。 ,如SDAC。混合物模型,用于关键建模步骤或当先前标准是不一致的,如前所述[ 2,4,5]。在这种方法中,两个竞争模型同时适用于数据,并且特定模型的偏好由混合参数的后验分布给出,该参数表示每个模型的相对贡献[ 15 ]。
进行灵敏度分析,通过将先验精度降低10倍,并将BSV参数的Wishart分布自由度从11降低到9来评估先验对PK模型对后验分布的影响。类似地,在PKPD分析中,通过将标准偏差加倍来减少所有先前的精确度(因此精确度降低了4)。ω矩阵的Wishart分布的自由度减少了。
使用来自最终模型的参数的后验分布的平均值作为参数的点估计,在MATLAB(版本2010b,The MathWorks,Natick,MA)中对最终模型进行编码。如果QT,RR对高于Fossa [ 16 ] 定义的'云'的上限,则假设QT间期是异常的并且与发生TdP的风险增加相关,这相当于QT,HR对是高于QT列线图[ 10 ]。对于50 日在我们的762ms研究中观察到的RR间期的百分位数,'阈值'QT间期被确定为447ms。使用最终模型参数5000 QT,模拟指定协变量组(30岁女性)的RR间隔,他们在治疗上服用依他普仑并且服用剂量为定义的5,10,20,30和40倍每日剂量10毫克。根据这些模拟值,计算具有异常QT的患者的比例。使用和不使用SDAC进行模拟。在这个例子中,我们从后验分布的点估计模拟,以减少计算负担。Yano 等人的工作证据。[ 17在形成预测分布时,基于来自完全后验的模拟与来自点估计的模拟的推断没有显示出差异。
使用具有和不具有SDAC的结果,将瞬时危险估计为在时间t处具有预测的QT间期高于447ms 的患者的分数。然后将累积危险度计算为0至96小时的瞬时积分。然后计算与施用SDAC相关的累积危害的相对减少。
最佳结构PK模型是没有滞后时间的单室一阶输入模型。基于DIC的减少选择组合误差模型。使用CT方法治疗依西酞普兰的患者包括基线浓度改善了模型。包含准确性改善了模型,但除基线浓度外还包括modtime并未改善模型。
施用SDAC使吸收的部分减少31%,并且效果大于20%的后验概率为0.76。SDAC对清除没有影响。年龄,性别和共同摄入抑制CYP2C19,CYP2D6或CYP3A4的药物与任何参数之间没有明确的关系,因此不包括这些协变量。因此,最终的PK模型具有组合的残余误差模型并且包括基线浓度,基于准确性的剂量不确定,并且SDAC作为共同影响吸收的分数(f F-charc)。
剂量与CL或V d之间无相关性。降低先验精度并不影响平均CL和V d的估计值(分别为-5.8%和+ 1.9%)。K a的估计值从5.97增加到52 450,表明该数据包含的信息非常少。个别场合的中位半衰期为34小时(四分位距[IQR] 28-38小时)。在给予SDAC的中位数为0.018(IQR 0.16-0.036)的患者中,针对剂量调整的曲线下的个体预测面积(AUC i,k /剂量i,k)降低,而患者中0.036(IQR 0.027-0.042)给出SDAC(图2)。对于给予SDAC且中位数为40.6 lh -1(IQR为26.4-47 lh -1)且未给予SDAC的患者为27.7 lh -1(IQR 24.6-40.4 lh -1)的个体预测CL不同。
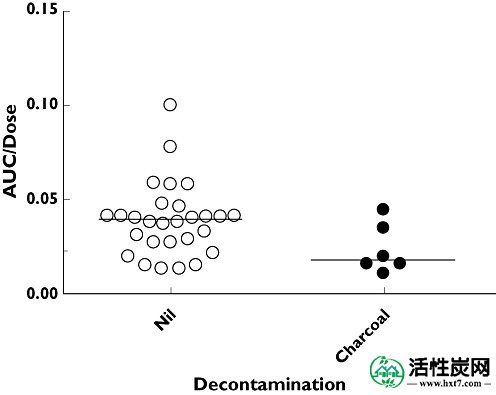
未接受SDAC(○)的患者与接受SDAC的患者的曲线下个体预测剂量标准化面积(AUC k /剂量)估计值的比较(•); 中位数用水平线表示
最终PKPD模型的相同,西酞普兰和包含个体心脏速率校正因子,α 我,线性浓度-效应关系(等式2),一个作用室模型和QT的年龄和性别特异性值C,Ĵ 0.加性误差模型用于QT间期数据。该模型很好地描述了数据,最终参数包含在表3中。从视觉上和用Gelman-Rubin诊断图(图S1和S2)看,MCMC过程似乎有很好的收敛性。年龄或性别对QT c,j 0的影响不大。观察到的CL / F值,V d / F,K a和基线浓度与PK分析相当(表3)。该数据包含关于所有参数的信息,所述参数基于后验装置从先前值移位(数据未示出)。
最终药代动力学 - 药效学模型的估计参数分布的平均值(95%CrI)
| 人口平均值(95%CrI *) | BSV(CV%)† | |
|---|---|---|
| CL / F(lh -1) | 33.5(20.1,50.3) | 74.4 |
| V d / F(l) | 1285(950,1715) | 63.2 |
| K a(h -1) | 8.0(1.1,36) | 111.4 |
| 基线浓度(mg l -1) | 0.014(0.003,0.045) | 46.3 |
| QT c,j 0 men(ms)‡ | 424(411,436) | 6.2 § |
| QT c,j 0女(ms)‡ | 423(414,432) | 6.2 § |
| α | 0.353(0.306,0.402) | 29.2 |
| t eq(h) | 1.01(0.05,5.6) | - |
| 斜率[ms /(mg l -1)] | 87(27,164) | 87.4 |
| C p上的比例残差(mg l -1) | 0.237(0.191,0.291) | - |
| C p上的附加残留误差(mg l -1) | 0.002(0,0.006) | - |
| QT上的比例残差(ms) | 16.6(14.8,18.6) | - |
对于具有典型PK和PD参数的个体,预计在过量服用后8.5小时对QT的最大影响与过量服用后0.7小时的峰值浓度相比(图3A)。对于药物浓度每增加1mg l -1,估计QT间期延长87ms(即斜率,表3)。该模型还预测了SDAC对QT间期的显着影响,如图3B所示,典型个体。
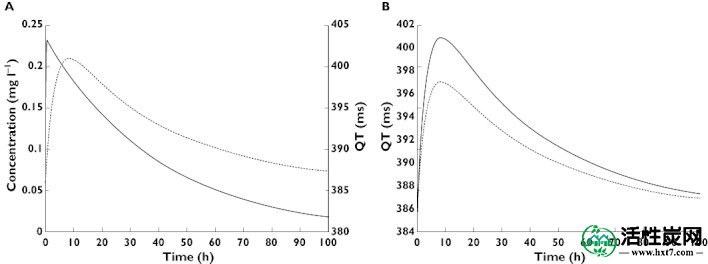
模拟血浆浓度( - )和QT间期( - - - )与患者的时间相比,典型的PK和PD参数为没有SDAC的艾司西酞普兰过量(A)。模拟QT间隔与没有( - )和( - - - )SDAC(B)的时间。对于两个组,剂量为300mg并且RR间隔为770ms(HR = 78bpm)
图4显示了依他普仑过量服用后QT值异常的患者比例,其中有和没有SDAC的中位RR值为762 ms(79次/分钟 -1)。SDAC的施用减少了具有异常QT的患者的比例(图4),并且在施用SDAC后过量200mg的异常QT的累积危害的相对降低约为35%(图5)。
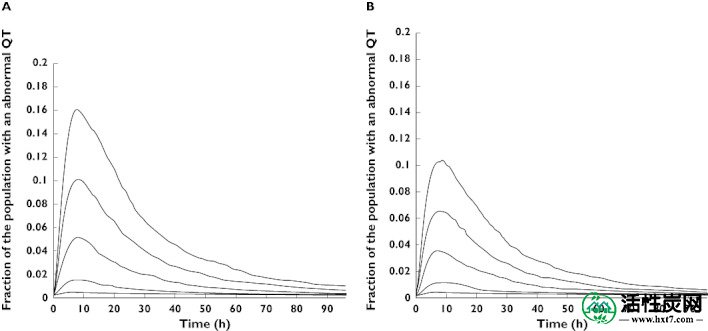
QT异常(QT> 447 ms,RR = 762 ms)的患者比例与50 mg至400 mg剂量时间的关系曲线。A)显示没有SDAC的患者比例和B)SDAC患者的比例。模拟了5000名患者,并假设30岁的女性在治疗上服用依他普仑
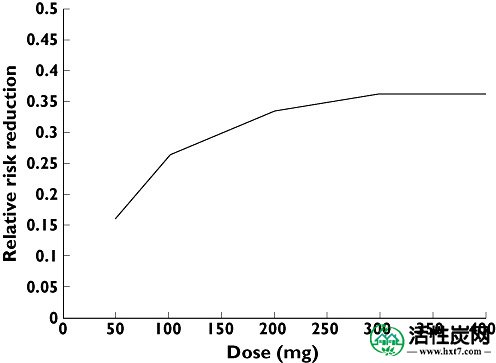
对于剂量范围为50 mg至400 mg的SDAC,QT间期异常(≥447ms,RR = 762 ms)累积危险相对减少的情节图
我们开发了过量服用依他普仑的人群PK和PKPD模型,以确定剂量 - 暴露 - 效应关系。在过量的药物以前PKPD研究,包括关于剂量和浓度基线不确定性信息的类似改进了模型,并报告剂量药物暴露[可靠措施7,18 ]。SDAC降低了吸收的分数,这在给予SDAC的个体患者AUC的减少中看到(图2)。这转化为SDAC发生异常QT的患者比例降低,服用200 mg或更多的患者相对风险降低35%。
我们无法证明SDAC对依他普仑药代动力学模型中清除的影响,考虑到SDAC对西酞普兰过量的清除具有临床重要影响,这是令人惊讶的。虽然依他普仑比R-对映体代谢更快,但这不足以解释木炭对清除的影响,因为依他普仑的半衰期仍为34小时。更可能的原因是对依他普仑过量服用的PK研究较小,34例中只有6例被给予SDAC。该模型不太能够提供严格的间隙估计,因此可以检测有和没有SDAC的间隙之间的差异。这在图6中示出显示了有或没有木炭的患者的清除率,比较了西酞普兰与依他普仑的预测个体清除率。
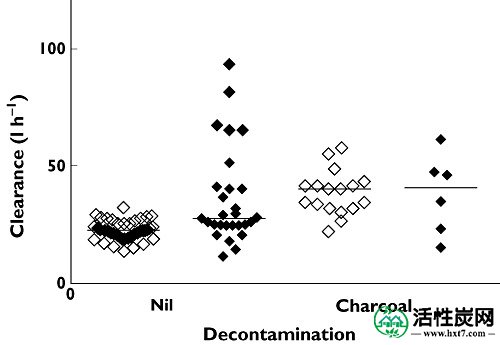
预测西酞普兰(灰线)的有或没有木炭的个体间隙值,与含有和不含木炭的依他普仑(黑点)的值相比较。使用先前公布的西酞普兰PKPD模型预测西酞普兰的清除值[ 2 ]。Escitalopram(♦); 西酞普兰(◊)
该研究增加了从药物代谢动力学研究的越来越多的证据所报告的剂量是药物暴露在过量的患者的有用的量度[ 2,4,5 ]。尽管报告的剂量存在不确定性,但在剂量上包含准确性改善了模型。这意味着报告的剂量是异常QT的有用预测因子,随着剂量增加,患者发生异常QT的比例增加。此外,对于200mg或更多的剂量,SDAC具有显着影响,异常QT发生的相对风险降低为0.35。因此,患者摄入的剂量的仔细历史对于风险评估和在某些情况下,例如依他普仑,SDAC的使用是至关重要的。
基于我们之前对西酞普兰过量服用的研究,其中大于10%的QT异常患者的剂量被认为具有临床重要性[ 8 ],可以建议SDAC用于摄入超过300 mg的依他普仑过量剂来自图4(上图)。同样,摄入超过300毫克未给予SDAC的患者或摄入超过400毫克且给予SDAC的患者应监测12小时或直至QT,HR对低于诺模图线。这些用于SDAC和监测的剂量截止值大致相当于为西酞普兰过量开发的先前剂量截止值[ 8 ]。
不能在PK和PKPD模型中包括表型协变量是该研究的限制,并且可能是由于数据集的大小。与过量患者的先前人群PK研究类似,实际上不可能在大多数患者中记录体重,因此在协变量分析中不能包括体重。虽然包含体重或瘦体重作为协变量可能会降低CL和V d的BSV ,但这可能没有改善该模型用于未来预测的有效性,因为在过量患者中很少测量体重。
另一个问题是虽然女性的QT间期通常较高并且随着年龄的增长而增加,但在我们的PKPD模型中没有发现。男性和女性的平均QT c,i(0)略高于女性,男性和女性最年轻和最年轻的个体之间至少有5%的差异。这可能是由于研究中的数量较少,但QT间期的这种关系已经在药物诱导的QT间期延长的其他研究中看到[ 19 ]。
像这样的完全贝叶斯分析有时会被批评为在先前的分布中包含主观信息。在这项研究中,我们使用来自文献[引发先验信息先前开发的客观方法2,13 ]。不幸的是,之前没有对依他普仑的人口分析。我们可用于引发先前分布的唯一信息是对健康志愿者进行治疗剂量的单一PK研究[ 20 ]。因此,我们只能在V d和CL 上包含信息丰富的先验,并且在参数上使用信息量较弱,生物学上合理的先验BSV(根据Friberg 等 [ 2]])。当我们在灵敏度分析中放松先验时,CL和V d的估计值最小化,表明数据(而不是先验)是模型最重要的信息来源。然而,当我们放松先验时,K a的估计值发生了显着变化。这可能是吸收阶段血液样本数量有限的结果。因此难以以有意义的方式解释K a的估计值。过量患者CL和V d的估计值与依他普仑治疗使用的PK研究相似[ 20]。似乎过量服用依他普仑的PK与治疗用途相似。
艾司西酞普兰过量的PKPD被很好地描述。报告的剂量与发生异常QT的患者比例之间存在明确的关系。SDAC降低了吸收的分数,从而导致QT异常风险显着降低。对于大于300mg的摄入剂量施用SDAC似乎是有益的。