发布日期:2018-11-13 09:39 来源:活性炭网 作者:活性炭网 浏览数:
描述了活性炭的氯甲基化。 发现氯甲基化产生表面积为1310m 2 / g 的碳衍生物, 并且孔结构没有显着变化。 发现该产物 每克材料 含有~1.5毫摩尔-CH 2 Cl基团,类似于原始Merrifield树脂合成
活性炭在世界范围内被广泛使用,作为吸附剂材料,用于各种分离和纯化需求。还修饰了活性炭以增强其对某些目标物种的亲和力。例如,活性炭已经用硫浸渍以增强其对Hg(1)的亲和力。该改性相当于碳主体内部的简单嵌入/沉淀,但是它在工业中已经发现了重要的应用和用途。重要的是认识到活性炭也可以通过针对芳族主链的化学反应进行化学修饰,例如亲电子芳族取代。例如,活性炭已经硝化(2,3)。这些-NO 2可以将基团还原形成-NH 2基团,然后可以将其用于酰胺偶联反应,从而允许引入多种配体和/或官能团。我们一直有兴趣更详细地探索这个一般领域,开发用于化学选择性分离的活性炭化学改性的其他方法。
在聚合物领域,单一最通用的合成子之一是氯甲基化聚苯乙烯,又名“Merrifield's树脂”(4)。在这些可溶胀性聚合物的苄氯很容易移动,促进肽,离子交换树脂,和催化剂载体(合成5 - 7)。Merrifield最初合成中使用的氯甲基化反应包括ClCl 2 -O-CH 3与交联聚苯乙烯的SnCl 4催化反应,得到每克树脂含有约1.89毫摩尔-CH 2 Cl 的产物(4(目前可获得的该聚合物的商业版本含有1.0至4.5毫摩尔Cl / g,取决于等级(8))。氯甲基化反应可以通过几种方式进行,最常见的是用甲醛,ZnCl 2和HCl 处理芳烃(9)。相应的苄醇是中间体,然后通过HCl将其转化为苄基氯(如图1所示)。交联/聚合(即Ar-CH 2 -Ar)可以是在溶液中具有自由移动的底物的竞争过程。
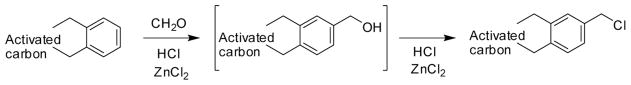
概述活性炭氯甲基化的通用示意图。
活性炭的刚性纳米多孔结构以及其优异的化学和热稳定性得到了广泛认可(10)。我们有兴趣将这种氯甲基化化学应用于活性炭骨架,以创造一种有用的合成子,可以很容易地进行各种化学分离。对于我们最初的实验,我们希望制作一个高表面积支撑装饰基于硫的功能,以便我们可以将其用作我们正在进行的重金属吸附剂研究的一部分(11)。烷基卤可以通过多种方式转化为相应的硫醇,但最广泛使用的策略是用含硫亲核试剂(例如硫代硫酸根阴离子,硫脲,硫代乙酸酯等)取代卤化物,然后裂解。产生硫醇的加合物(见图2)。该手稿总结了用共价锚定的硫醇基团修饰的新型纳米多孔碳基吸附剂材料的合成,并证明了其对重金属分离的效果。
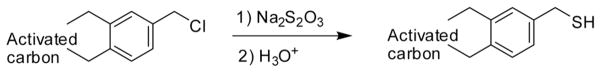
显示将硫醇结合到活性炭主链上的一般示意图。
活性炭(Darco KB-B,100目)购自Aldrich。测定该材料的表面积与质量比为1483m 2 / g,孔体积为1.53cc / g。所有其他试剂均购自Aldrich并按原样使用。
采用有机合成方法的变体(12)。一个三颈500毫升圆底烧瓶装有一个大的磁力搅拌棒,一个橡胶隔膜,一个短路冷凝器连接到一个带有硅油鼓泡器和惰性气体供应的气体歧管,和一个玻璃分散管连接到一个无水HCl罐。首先向烧瓶中加入10.0g活性炭和0.50g(3.7mmol)氯化锌,最后加入250mL 1:1浓盐酸和乙酸的混合物。将混合物在27℃下搅拌直至所有氯化锌溶解,然后在氩气氛下将温度降至0℃并在该温度下在冰浴中保持接下来的3小时。混合物在0℃后,停止氩气流,剧烈鼓泡通入悬浮液,然后加入38.0克(0.47摩尔)37%水溶液。一次性加入甲醛。继续HCl流动4小时,然后将溶液温热至27℃并再搅拌6小时。在玻璃料上收集氯甲基化活性炭,用两份100mL水洗涤,然后用三份100mL甲醇洗涤。将滤饼破碎并转移到敞开的聚乙烯容器中。将粉末在50℃和0.25atm下进一步干燥另外36小时。最终干燥的产物重11.75g。将滤饼破碎并转移到敞开的聚乙烯容器中。将粉末在50℃和0.25atm下进一步干燥另外36小时。最终干燥的产物重11.75g。将滤饼破碎并转移到敞开的聚乙烯容器中。将粉末在50℃和0.25atm下进一步干燥另外36小时。最终干燥的产物重11.75g。
氯甲基化材料的表面积为1310m 2 / g(与适度的质量增加一致),孔体积为1.30cc / g。孔结构没有可辨别的变化,表明氯甲基化化学没有阻塞或显着降低孔结构。
该材料的元素分析显示氯含量为5.21%,相当于约1.46毫摩尔/克。在鉴定-CH 2 Cl基团的新条带方面,氯甲基化材料的FTIR分析是不确定的。
将2.3865g氯甲基化活性炭悬浮在60mL甲醇中。将硫代硫酸钠(8.6g,35mmol)溶解在60mL蒸馏水中。将硫代硫酸钠溶液加入到500mL圆底烧瓶中的氯甲基化活性炭悬浮液中。将该混合物在氮气下搅拌并加热至回流总共12小时。通过真空过滤收集产物,用蒸馏水大量洗涤,然后用甲醇洗涤。然后将产物风干数天(回收1.549g)。
BET表面积分析显示表面积与质量比为1179m 2 / g,与氯甲基化活性炭原料的孔径分布没有可辨别的差异。再一次,没有证据表明活性炭的孔结构受损。
该材料的元素分析显示氯含量为0.15%,表明Cl的有效置换。发现S含量为4.2%,与硫代硫酸根阴离子整合到产品中一致。这相当于每克吸附剂1.3毫摩尔S,或0.65毫摩尔硫代硫酸盐/克。鉴于该产品以1.46毫摩尔-CH 2 Cl开始,这表明~45%转化为Bunte盐。在鉴定硫代硫酸盐基团的新谱带方面,氯甲基化物质的FTIR分析是不确定的(已知Bunte盐在~1215cm -1,~1050cm -1和~650cm -1(13)处具有特征谱带)。
将2.50g上述制备的氯甲基化活性炭样品悬浮在60mL甲醇中。首先将硫代硫酸钠(8.60g; 34.7mmol)溶解在60mL反渗透(RO)水中,然后加入到含有活性炭的反应容器中。将混合物回流2小时并在0.45μm尼龙过滤器上温热收集,洗涤2×100mL RO水,并风干。将粗品Bunte盐重新悬浮在100mL 3.0N HCl中,并将混合物在密封的Mason罐中于80℃保持12小时(14)。将悬浮液搅拌1小时并再回到80℃的温度另外1小时,然后通过中等玻璃料过滤。收集的AC-CH 2用2×100mL份的RO水洗涤-SH,然后用100mL甲醇洗涤。将洗涤过的物质在0.75atm下真空干燥。在25℃下18小时,得到1.78g材料。产物的元素分析显示S含量为1.88%。这相当于每克吸附剂0.59毫摩尔硫醇。考虑到中间体硫代硫酸盐具有0.65毫摩尔/克的功能密度,该结果表明水解反应干净地进行并且产率> 90%。BET表面积分析显示表面积与质量比为1244m 2/ g,孔体积为1.29cc / g。来自氯甲基化活性炭原料的孔径分布没有可辨别的差异。硫醇 - 甲基化物质的FTIR分析在确定-CH 2 -SH基团的新谱带方面尚无定论(~2550 cm -1处的硫醇S-H拉伸通常非常弱,通常未被检测到(15)) 。
对于分配系数(K d)测量,过滤的河水(来自哥伦比亚河,里奇兰,华盛顿州)加入了金属离子(Co 2 +,Cu 2 +,As 3 +,Ag +,Cd 2 +,Hg 2+),Tl +和Pb 2+)各自获得100μg/ L. 使用0.1M HNO 3将溶液pH调节至所需值和0.1M NaOH。温育30分钟后,将其在20mL聚丙烯小瓶中等分至4.9mL体积中。然后在溶液中加入0.1mL固体吸附剂和去离子蒸馏(DI)水的悬浮液,液体固体比率(L / S,以mL / g为单位),为100.这导致最终的L / S 5,000。对照以相同的方式进行,但没有固体吸附剂。然后将样品在轨道振荡器上以160rpm摇动2小时。2小时后,通过0.45-μm注射器尼龙膜过滤器过滤除去溶液,滤液保持在2体积%HNO 3中。在金属分析之前。使用电感耦合等离子体质谱仪(ICP-MS,Agilent 7500ce,Agilent Technologies,CA)分析对照(无吸附剂)和测试溶液(与吸附剂材料接触后)中的浓度。所有批次实验一式三份进行,并报告平均值。K d(以mL / g为单位)只是固相和液体上清液相之间的质量加权分配系数,如下所示:
其中C o和C f是通过ICP-MS测定的目标物质溶液中的初始和最终浓度,V是以mL计的溶液体积,M是吸附剂的克质量。
以与K d相同的方式测量吸附剂对金属离子的吸附容量,但仅使用单一元素并且其浓度在溶液中变化直至获得最大吸附容量。这通过使用大量过量的金属离子与吸附剂材料上的结合位点的数量(例如,L / S为0.1至4mg / L的金属离子为100,000)来实现。
以与平衡研究相同的方式进行金属吸附的动力学,除了取出1mL充分混合的等分试样并在0,1,2,5,10,30,60分钟,4,7和7过滤。 24小时,初始样品体积增加至100mL,以使L / S的变化最小化。
发现活性炭的氯甲基化顺利进行。起始活性炭的比表面积为1483m 2 / g。发现氯甲基化产物的比表面积为1310m 2 / g。如果材料的绝对表面积保持不变,则可以预期表面积与质量比下降,因为系统已经获得质量(在每个取代位点失去H +和-CH 2 Cl基团的增加)。在氯甲基化反应中观察到适度的质量增加(~17%),如果绝对表面积固定,则预测的表面积与质量比为1223m 2。/G。虽然协议并不完美,但这一观察结果支持了氯甲基化反应不会显着影响碳基质表面积的结论。与此一致,观察到孔体积从1.53cc / g略微下降至1.30cc / g。观察到的等温线(参见图3)和产物的孔径分布(参见图4)表明在这些条件下氯甲基化反应期间没有发生活性炭的显着交联或孔堵塞。该材料的氯化物含量(~1.46毫摩尔/克)表明在这些条件下该材料的氯甲基化程度与原始的Merrifield合成相似(4)。这种氯甲基化活性炭可以被认为是Merrifield树脂的类似物,不同之处在于它具有刚性,开放的纳米多孔结构。虽然Merrifield的树脂是可溶胀的,但这种氯甲基化活性炭不是,虽然Merrifield树脂的大部分使用都涉及“外部”功能(例如,在肽合成中),但这种氯甲基化活性炭的大部分功能都是内部的(可能是证明对基于尺寸的分离有用)。另一个关键差异是活性炭主链与聚苯乙烯主链的稳定性; 在热稳定性和化学稳定性方面,活性炭与聚苯乙烯相比具有明显的优势。预计氯甲基化活性炭可用于各种应用,
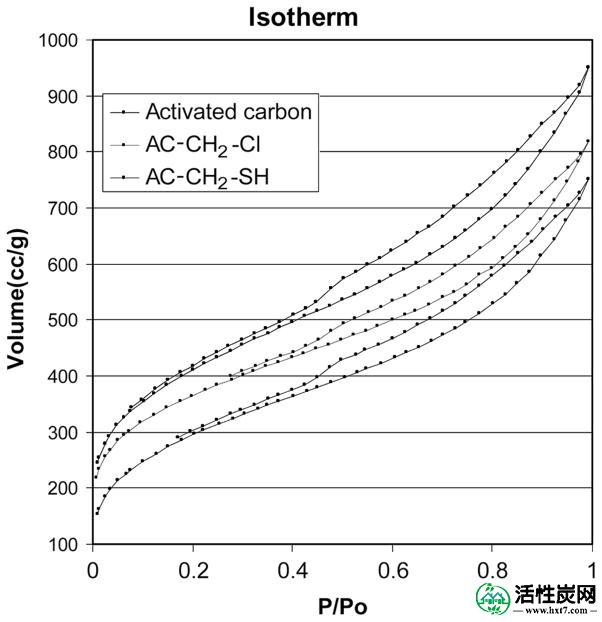
活性炭(Darco KB-B; Aldrich;顶部),氯甲基化活性炭(AC-CH 2 Cl;中间)和硫醇 - 甲基化活性炭(AC-CH 2 -SH;底部)的吸附等温线。
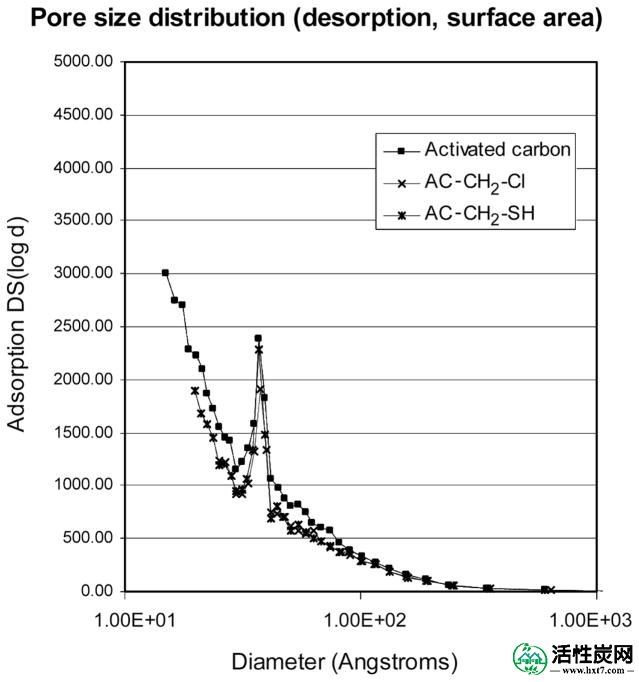
活性炭(Darco KB-B; Aldrich;顶部),氯甲基化活性炭(AC-CH 2 Cl)和硫醇 - 甲基化活性炭(AC-CH 2 -SH)的孔径分布。
尝试使用磷酸作为溶剂进行类似的氯甲基化反应,并且该产物的Cl含量和表面积都低得多。
毫不奇怪,苄基氯与硫代硫酸根阴离子的S N 2置换以合理的产率进行,得到相应的Bunte盐。起始的氯甲基化活性炭含有1.46毫摩尔/克Cl,而硫代硫酸盐仅含有0.65毫摩尔/克硫代硫酸盐。硫代硫酸盐产物的元素分析显示仅有0.15%的Cl,表明已经消耗了> 97%的苄基氯。由于仅约45%的苄基氯被转化为相应的硫代硫酸盐,其余的必须在一些其他竞争过程中消耗(在回流的甲醇水溶液中溶剂分解)。
与氯甲基化步骤相反,硫代硫酸根阴离子对氯离子的置换不会对碳主链产生任何化学变化,仅在氯甲基侧基上。因此,预测基质本身应该几乎没有形态变化似乎是合理的。氯甲基化活性炭的比表面积为1310m 2 / g,用硫代硫酸盐处理后的产物的比表面积为1179m 2 / g。如果在该反应过程中材料的绝对表面积保持不变,则可以预期表面积与质量比会随着较重的硫代硫酸钠部分(NaS 2)的氯离子(原子量为35.5克/摩尔)的位移而下降。O 3,MW = 135.2克/摩尔),因为系统的质量会增加。对于~1.5mmol / g的~50%转化率,这将预测约1250m 2 / g 的比表面积(忽略-CH 2 Cl基团的另一半的命运)。再次,虽然拟合不精确,但趋势是正确的方向,并且它支持这样的结论:在该置换反应期间碳骨架的形态没有显着变化。
已知硫代硫酸盐在酸性条件下干净且定量地裂解成相应的硫醇(14)。因此,将一批粗硫代硫酸化活性炭用3M HCl在80℃下水解过夜。这样可以干净且高产地生成相应的硫醇。发现硫醇的比表面积为1244m 2 / g,孔体积为1.29cc / g,硫含量为1.88%(相当于每克吸附剂0.59mmol的硫醇)。吸附等温线和孔尺寸分布支持这样的结论,有硫代水解期间的孔结构没有显著变化(参见图3和AND44)。
为了评估这种新的硫醇 - 甲基化活性炭(我们将其缩写为AC-CH 2 -SH)的化学效用,我们在一系列pH条件下对各种金属阳离子进行了一系列吸附实验。结果总结在表1中。
使用硫醇化活性炭(AC-CH 2 -SH)的重金属吸附实验。所有实验一式三份进行并取平均值
| 吸附剂 | 最终的pH值 |
平均K d(mL / g吸附剂)
|
|||||||
|---|---|---|---|---|---|---|---|---|---|
| 钴(II) | 铜(II) | 作为(III) | 银(I) | 镉(II) | 汞(II) | 铊(I) | 铅(II) | ||
| SH-SAMMS | 0.11 | 170 | 180 | 27000 | 2600000 | 65 | 1500000 | 29 | 31 |
| 2.01 | 0 | 74000 | 7100 | 3300000 | 0 | 1400000 | 15 | 22 | |
| 4.13 | 23 | 210000 | 1000 | 2800000 | 310 | 1500000 | 140 | 250 | |
| 6.19 | 170 | 140000 | 5800 | 1100000 | 4400000 | 810000 | 150 | 630000 | |
| 7.35 | 650 | 250000 | 16000 | 640000 | 1600000 | 650000 | 400 | 2700000 | |
| 8.31 | 870 | 280000 | 18000 | 440000 | 1100000 | 550000 | 340 | 190万 | |
| AC-CH 2SH | 0.17 | 280 | 260 | 180 | 1700 | 0 | 1600000 | 96 | 91 |
| 2.02 | 160 | 260 | 78 | 1400 | 83 | 1100000 | 19 | 120 | |
| 4.31 | 120 | 2100 | 0 | 5800 | 270 | 1800000 | 110 | 1500 | |
| 6.37 | 1100 | 55000 | 160 | 62000 | 1400 | 2200000 | 560 | 86000 | |
| 7.33 | 1900 | 100000 | 0 | 340000 | 5000 | 610万 | 1500 | 120000 | |
| 8.49 | 2100 | 88000 | 0 | 410000 | 4300 | 20000000 | 1700 | 110000 | |
| 活性炭 | 2.12 | 0 | 55 | 0 | 220 | 0 | 2600 | 73 | 170 |
| 4.22 | 110 | 5400 | 0 | 820 | 170 | 4800 | 250 | 6600 | |
| 7.61 | 1300 | 53000 | 23 | 3400 | 2900 | 9700 | 1800 | 67000 | |
初始金属浓度= 100ppb,L / S = 5000,在pH调节的过滤河水中。
为了便于比较,平行组实验,还进行了介孔载体上使用的硫醇终止自组装膜(巯基SAMMS ®)(16)看骨干的性质对在什么样的影响(如果有的话)这些硫醇吸附剂的性能。还用未改性的活性炭进行了一系列对照实验。
第一种趋势从这些数据中明显的是,无论是AC-CH 2 -SH和硫醇SAMMS ®吸附剂系统是在宽的pH范围内的捕获汞(我们的主要目标)是非常有效的。在大多数情况下,在AC-CH 2 -SH有汞,银,镉和相对于SAMMS铜更低的亲和力®。这大概是由于这样的事实,硫醇基团在SAMMS的有组织的单层环境的密实填充®允许多个金属配体相互作用,并因此更大的结合亲和力(17)。在AC-CH 2 -SH中没有这样的顺序,并且结合亲和力更可能是与金属阳离子相互作用的分离的硫醇基团的反映。
对T1(I)的低结合亲和力是令人惊讶的。Tl(I)几乎与Hg(18)一样“软” ,并且预计几乎与Hg 的AC-CH 2 -SH 的硫醇基团强烈结合。然而,从表1中的数据可以看出,观察到非常少的T1(I)结合。对此的一种可能解释是As(III)(即亚砷酸)与T1(I)阳离子的相互作用。已知亚砷酸与“软”路易斯酸(例如,Pd(19))配位,这为该假设提供了一些信任。为什么As(III)在这些其他金属阳离子存在下选择性地结合T1(I)目前尚不清楚。
作为与巯基SAMMS观察®,重金属结合亲和力,发现增加随着pH增加,尤其是对汞(我们的主要目标),提示也许这吸附剂可以强碱性条件下,其中二氧化硅或聚合物-下找到应用重金属捕获基于吸附剂可能不稳定。重要的是要认识到,虽然这种活性炭已经用巯基修饰,但已经存在的其他“本土”功能并未被“擦除”(即羧酸,酚类,内酯等)(20)))。一旦pH值高于约6,增加的金属与pH增加的结合对于Hg,Cu,Ag和Pb尤其显着,这与酚-OH基团的pKa大致相关,因此可能是由于酚的去质子化。以及随后的酚盐阴离子与金属阳离子的相互作用。使用来自AC实验的数据作为参考,很明显这种酚盐机制不是金属结合的主要驱动因素,这表明在这些碱性条件下硫醇盐和酚盐配体之间可能存在某种配体协同作用。
为了探测Hg吸附的动力学,使用1,000ppb的Hg(II)溶液在标称pH5下进行动力学实验。结果总结在图5中。该实验以液/固比为1,000进行。从数据中可以看出,使用AC-CH 2 -SH 的Hg吸附动力学非常快,在不到30分钟内将Hg浓度降至~0.04ppb。虽然这比通常使用的汞吸附剂(例如,GT-73(显著快16,21),或硫浸渍的活性炭(22)),它是显着高于硫醇SAMMS慢®,这实现在类似的结果在类似条件下仅需2-3分钟(16,21)。
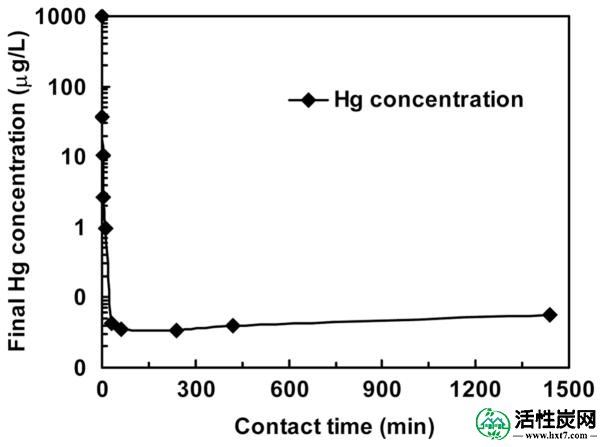
AC-CH 2 -SH在pH~5下吸附Hg的动力学(溶液/固体比= 1,000)。
进行一系列实验以确定AC-CH 2 -SH 的Hg结合能力。这些实验以溶液/固体比为100,000,标称pH为5.5进行。从图6中总结的结果可以看出,数据显示Langmuirian行为,并显示出每克吸附剂约33mg Hg的结合能力。这比每克吸附剂的> 600毫克汞已被观察到与硫醇SAMMS容量小得多®(21)。
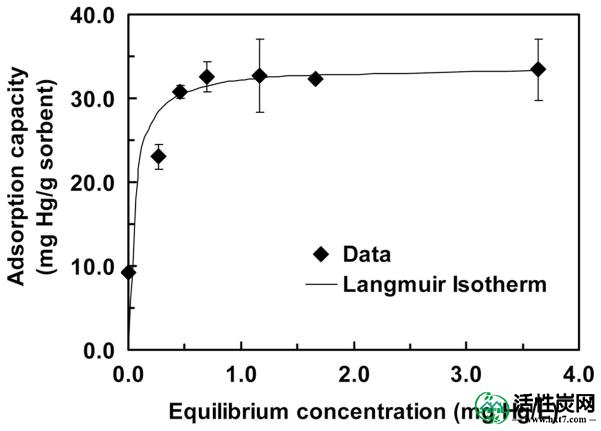
在pH为~5.5时,Hg对AC-CH 2 -SH的吸收容量等温线。
AC-CH 2 -SH 的Hg结合能力是观察到的官能化水平的一小部分(每克吸附剂0.165毫摩尔汞,与每克吸附剂0.59毫摩尔硫醇相比)。假设1:1的结合化学计量,这相当于硫醇负载的约28%,表明溶液携带的金属离子不易接近大部分硫醇官能团。类似的观察已用其它官能团(前面提到的2,3)。活性炭通常具有大量的微孔性,并且可能很多功能性锚定在这些微孔内,使其在动力学上不可接近。另一种可能的解释是多个硫醇/金属相互作用(例如,2:1或3:1结合化学计量)。之前已在人口密集,更高度有序的系统中观察到这种情况(17),但在这种更无序的系统中不太可能,功能密度稍低。
已知Hg(II)与活性炭的结合取决于活性炭的氧化水平,随着碳吸附剂(23)的氧化增加,Hg结合能力下降。报告的臭氧化活性炭的Hg(II)结合能力略低于我们在此报告的结果(例如,10-20 mg / g(23)),而其他“未掺杂的”活性炭相似(~25 mg / g(23))),据报道其他人具有更高的Hg结合能力(例如,154mg / g(24))。已经提出的是,汞活性炭结合是由于从碳主链(的富电子部分所产生的氧化还原机构23,24,26因此,活性炭经受的处理可能是至关重要的。从表1中总结的结果可以明显看出该机制在我们的研究中所起的有限作用- 未修饰的活性炭对AC-CH 2 -SH的Hg(II)具有一小部分亲和力。这种特定的活性炭具有12.7%的氧含量,使其在上述讨论的情况下被相当高度氧化,因此是氧化还原结合机理的不良配偶体。因此,我们得出结论,AC-CH 2 -SH主要通过硫醇基团通过共价Hg-S键结合Hg。
如果-CH 2 SH基团的很大一部分确实处于动力学不可接近的微孔中,那么就提出了如何改进这种化学反应的问题。显然,较大的孔隙碳是有利的。一个有趣的可能性是使用模板化的中孔碳作为底物来进行氯甲基化反应,因为这将允许先验地确定孔径。该策略的成功可能取决于碳中孔中暴露的“边缘”的数量。由于这种化学反应基于亲电子芳香取代,因此在孔壁上必须存在芳香族C-H键(即芳环的“边缘”),因此-CH 2可以安装Cl组。对于模板化的中孔碳,这反过来表明所选择的碳化条件可能在该方法的成功或失败中起关键作用,因为孔壁的石墨化程度将对C-H的数量产生重大影响。留在孔壁上的粘合剂。
氯甲基化活性炭易于由廉价,易得的材料制成。观察到的氯甲基化水平与Merrifield树脂的原始合成中报道的相似。氯甲基化反应似乎对活性炭的表面积或孔结构没有任何负面影响。苄基Cl易于被亲核试剂置换,使得易于获得可用于化学分离的化学修饰的活性炭。我们已经利用它来制造用硫醇基团修饰的活性炭,并表明它可用作重金属吸附剂。AC-CH 2发现-SH快速,有效并且能够将Hg浓度降低至远低于ppb水平(例如,0.04ppb)并且通过强共价Hg-S键结合Hg。AC-CH 2 -SH 的Hg吸附动力学比目前使用的常规吸附剂(例如,GT-73或硫浸渍的活性炭)观察到的快得多。活性炭骨架为AC-CH 2 -SH吸附剂提供了优异的化学和热稳定性,并且已经显示出在碱性条件下增强吸附剂对重金属的亲和力。使用AC-CH 2 -SH的Hg结合容量测量表明,大部分硫醇基团可能处于动力学不可接近的微孔中。
AC-CH 2 SH是不是一个强大的汞吸附剂如巯基SAMMS ®。巯基SAMMS ®不仅显示显著更快的吸附动力学,而且还高得多的汞结合能力。然而,AC-CH 2 -SH可能在基于二氧化硅的吸附剂不适合的条件下(例如,强碱性条件)证明是有用的。正在进行这些和相关材料的进一步研究。