发布日期:2018-11-12 09:34 来源:活性炭网 作者:活性炭网 浏览数:
使用BET模型中的表面积测定,Boehm滴定,TPR,DRX和浸入量热法,在处理之前和之后对结构化和化学表征活性炭。 通过气相色谱测定吸附容量和硫化合物去除的动力学。 已确定丙硫醇保留
含有硫醇基团(-SH)的化合物具有高度气味和挥发性,即使空气中少量此类物质,例如CH 3SH(最小气味阈值:约5ppm),也会使我们感到不舒服。-SH物种的从空气中除去是很重要的我们的舒适度,和活性炭被广泛地用作最有效的吸附剂之一[ 1 - 3]。通常,活性炭对有机化合物的吸附很大程度上受到孔径,分布,形态和表面性质等特性的影响。丙硫醇被物理或化学吸附在活性炭上。由于丙硫醇分子具有平均尺寸,因此认为活性炭的表面性质和孔特性在其吸附中起重要作用。在另一方面,已经报道,甲硫醇到二甲基二硫化物的氧化在含有官能团的活性炭的表面,如在干/湿空气[羧基4 - 6 ]。此外,还有一些关于表面改性活性炭上硫醇的吸附/氧化的报道[ 7- 9 ]。然而,很少有报道讨论丙烷硫醇在活性炭上的真实吸附。
参照活性炭的表面改性,引入羧基和氨基的,和官能团游离-活性炭的制备方法,已经报道了10 - 17 ]。通过HNO引入羧基到活性炭的表面3或H 2个 ö 2处理已经研究[ 10 - 13 ]。引入氨基基团已通过各种方法,例如,减少由HNO形成的硝基进行3 / H 2 SO 4 [混合物14 - 16 ],和治疗与气态氨[ 17]。另一方面,大多数官能团通常在Ar或N 2下进行热处理时消失。氧化铜吸附剂通常与噻吩硫化合物(例如丙硫醇)非常不反应,而相反,它们容易与硫醇反应并吸附硫醇(也称为硫醇)。众所周知,Cu基吸附剂的效率低于基于Ni的吸附剂,并且经常观察到硫从这种类型的保护床中泄漏。然而,硫醇以与氧化铜非常不同的方式起作用,因为发生不可逆的氧化还原反应,在两步过程中将硫醇和Cu 2+转化为硫醇铜(I)[ 18 ]:
在第一步中,在硫醇和CuO之间发生还原/氧化,形成二硫化物和氧化铜(I)。当硫醇与表面氧化铜(I)反应形成硫醇铜(I)时,反应继续进行。根据以下反应,在铜金属表面和硫醇之间发生类似的化学反应,其中铜金属用作释放H 2的还原剂:
众所周知,硫醇会自组装成硬币金属表面上严格排列的单层(通常称为SAM),尤其是金,银和铜[ 18 ]。由于所得表面的独特性质,包括对电化学和其他反应的稳定化和钝化,已经对这些SAM进行了深入研究并引起了极大的兴趣。虽然铜/硫醇化学的大部分研究都局限于SAM的形成和性质,但已经证明多层可以形成独立的层状结构(图1)[ 10 - 21]]。在该研究中发现,在适当的条件下,这些类型的层状化合物可以在升高的温度和压力下以及在烃溶剂存在下在硫保护床中形成。人们早就知道Cu 2+和硫醇的氧化还原化学,事实上,自20世纪初以来,基于这种化学作用,已经使用了一种使汽油变甜的方法[ 22 ]。
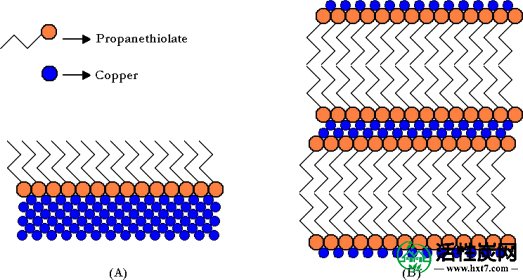
简单表示(A)铜金属表面上丙硫醇的自组装单层(SAM),和(B)铜(I)丙硫醇盐的自组装多层。
在所谓的“Perco”工艺中,将氯化铜(II)置于带有汽油的空气渗滤床中,并且恶臭的硫醇转化为较少攻击性的二硫化物。在这种情况下,根据以下反应,在该过程中不消耗Cu 2+,因为来自空气渗滤的氧气将部分还原的Cu +再氧化回Cu 2+。
Perco甜味工艺:
注意,在Perco脱硫过程中,绝不允许铜形成稳定的硫醇铜(I)化合物。最后,使用混合的水相和有机相进行常规合成硫醇铜(I),例如由丙硫醇制成的硫醇盐,其中水相含有Cu 2+盐,有机相含有硫醇。这些程序各不相同,之前已有报道[ 20 ],但一般程序仅说明了合成硫醇铜(I)硫酸盐晶体的常用方法。在本工作中显示的是,这些层状材料也可以在与炼油厂中硫捕集床中使用的条件类似的条件下形成。
在此背景下,在这项工作中,我们研究了通过酸处理对不同时间和浓度的活性炭的表面改性以及通过用铜浸渍对从水溶液中吸附丙硫醇的影响。还进行了动力学反应的研究,并根据结果和文献综述进行了研究; 我们解释了铜在丙硫醇分解中的作用。
为了研究对活性炭表面结构性质的影响,确定了N 2在77 K 下的吸附 - 解吸等温线,如图2所示。
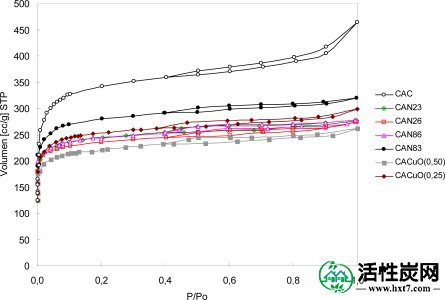
N 2吸附等温线在77 K.
根据IUPAC分类,等温线为I型。在活性炭的吸附 - 解吸等温线中N 2的主要消耗发生在相对低的相对压力(<0.2)并且在高相对压力下达到平台。这些结果表明通过各种处理获得的活性炭是微孔的。在用酸处理的活性炭的情况下,吸附的N 2的量随着HNO 3浓度的增加而降低,如用CuO处理的那些,可能是因为该处理在活性炭中产生高度堵塞的孔。关于CAN83,其面积有所减少,但与其他碳没有相同的幅度。在用HNO 3处理的情况下 在8小时内,活性炭的表面积仍然相当大。
通过用前体水溶液(硝酸铜,Cu(NO 3)2 ·3H 2 O)浸渍预处理的CAC制备的CuO / CAC催化剂表现出表面积减小,但微量体积和中孔的数量级与合成的其他多孔材料的数量级相同。
基于N 2吸附 - 解吸等温线的活性炭的孔特征示于表1中。
表面积(S BET)和来自N 2吸附等温线的总孔体积(V t)在77K。
| 碳 | S BET(m 2 / g) | V t(cm 3 / g) | V mic(cm 3 / g) | V meso(cm 3 / g) |
|---|---|---|---|---|
| CAC | 1449 | 0.66 | 0.43 | 0.23 |
| CAN23 | 884 | 0.39 | 0.33 | 0.06 |
| CAN26 | 855 | 0.39 | 0.32 | 0.07 |
| CAN83 | 1039 | 0.46 | 0.37 | 0.09 |
| CAN86 | 875 | 0.36 | 0.33 | 0.03 |
| CACuO(0.50) | 872 | 0.41 | 0.34 | 0.07 |
| CACuO(0.25) | 992 | 0.36 | 0.30 | 0.06 |
CAC是高度微孔的并且具有高于1400m 2 / g的BET表面积。在酸处理的活性炭的情况下,在用HNO 3溶液处理后BET表面积减小。假设活性炭的多孔结构部分地被HNO 3溶液的强氧化作用破坏并且未检测到微孔。表1报告了通过BET方法计算的表面积,总体积以及每种活性炭的中孔和微孔体积。
通过滴定法[ 13 ] 估算的活性炭上的酸性基团数如表2所示。用HNO 3溶液处理碳表面导致该表面上的氧化基团(酸性和碱性)的量增加。与在该工作中获得的其他活性炭相比,在CAC上发现更多数量的氧化基团,其显示了文献中报道的氧化剂HNO 3的作用。
Boehm滴定结果和AC的表面化学。
| AC | 羧酸盐* | 内酯* | 酚类* | AC | 含氧总量* | 总酸度* | 总碱度* |
|---|---|---|---|---|---|---|---|
| CAC | 2.14 | 2.37 | 83.2 | CACuO(0.25) | 281 | 281 | 86.8 |
| CAN23 | 61.3 | 65.7 | 108.5 | CACuO(0.5) | 282 | 279 | 60.3 |
| CAN26 | 62.4 | 60.8 | 133.7 | CAN26 | 301 | 256 | 14.2 |
| CAN83 | 63.5 | 118.6 | 140.6 | CAN86 | 328 | 315 | 5.82 |
| CAN86 | 65.1 | 120.4 | 142.3 | CAN83 | 330 | 320 | 2.26 |
| CACuO(0.25) | 3.51 | 140 | 135 | CAN83 | 164 | 163 | 24.0 |
| CACuO(0.5) | 32.9 | 234 | 13.7 | CAC | 88 | 87 | 56.9 |
表2显示,在活性炭中,由HNO 3处理产生的氧化基团的量随时间增加,并且在用铜离子处理后观察到类似的行为,因为氧化基团的量也增加。沉积在碳表面上的铜的量更大,并且可以预期这些离子在丙硫醇分解中的相应增强的催化效果。
如表2所示,每种活性炭样品中氧化基团的数量减少。在所有情况下,用硝酸改性的活性炭的碱度小于CAC中的碱度。用硝酸铜改性的活性炭显示出更高的酸性,因为铜与碱具有更高的亲和力,消耗更多摩尔的氢氧化钠。随着氧化基团数量的增加,总酸度增加。
关于活性炭在水和丙硫醇中的浸渍焓的结果示于表3中。表面化学是影响浸入测试液体中的碳产生的热量的最大变量之一[ 13]。对于CACuO(0.25)和CACuO(0.5),获得了丙烷硫醇中活性炭的浸渍焓的高值。改性的活性炭没有显示出显着的相互作用,因为当碳浸入丙二醇时产生的热效应很低; 在不增加活化剂浓度或改性持续时间的情况下,样品的焓增加。考虑到吸附剂 - 吸附质相互作用的焓值的数量级,这可以被认为是一种物理学[ 18 ]。
活性炭在水和丙硫醇中的浸入焓。
| 碳 | -ΔH IMM水 | -ΔH IMM丙硫醇 |
|---|---|---|
| CAC | 25.55 | 35.21 |
| CAN23 | 23.10 | 31.72 |
| CAN26 | 10.82 | 38.70 |
| CAN83 | 23.89 | 33.22 |
| CAN86 | 18.03 | 64.40 |
| CANCu(0.5) | 10.94 | 1133.4 |
| CANCuO(0.25) | 25.58 | 138.47 |
这是因为在这种情况下存在化学物质的相互作用,当比较焓值之间的焓值之间的数量级时,丙硫醇值与水相比更高。此外,我们看到不同处理对活性炭的影响,其可以通过浸没微量量热法来表征。
图3显示了载体催化剂CACCu(0.25)和CACCu(0.5)的XRD图谱。氧化铜的XRD图谱在2θ的35.7°和38.55°的角度处具有峰值; 这些反射角表明氧化铜颗粒在活性炭上的形成和存在,与文献[ 13]一致。图2显示了CACuO(0.25)和CACuO(0.50)的这些峰。
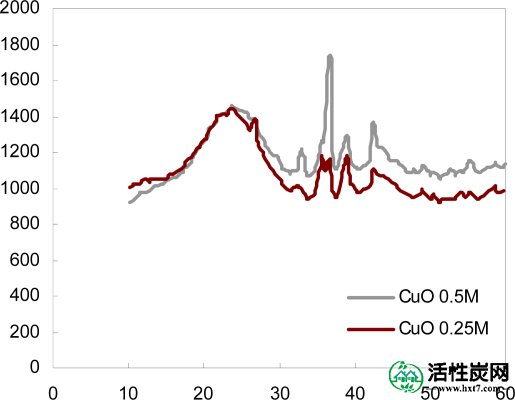
用氧化铜浸渍的活性炭的X射线衍射。
通过粉末X射线衍射分析废吸附材料,发现铜(I)丙硫醇盐晶体的优选取向具有非常强的反射(图2)。在顶部吸附和丙硫醇分解之前和之后,在CACCu(0.5)中测量最强的强度,表明形成了相对大的晶体。参考文献[ 20 ] 中显示了其他硫醇盐晶体的类似衍射图,但似乎强度要低得多,证实了己烷溶液中Cu 2+和丙硫醇之间的氧化还原化学。
基于布拉格衍射定律和晶体的峰位置,层状铜(I)丙硫醇盐晶体的层间距为35.7°和38.55°,这与文献中报道的值非常接近。
因此,结论是在这个过程中使用了大量的铜。如已经显示的,铜颗粒的分散增强了硫吸附的总容量。根据上述观察结果并将这些数据与引言中所述的化学机理进行比较,图4说明了根据Turbeville的提议,使用活性炭 - 铜作为催化剂吸附 - 分解硫醇的主要机理。等。[24]。
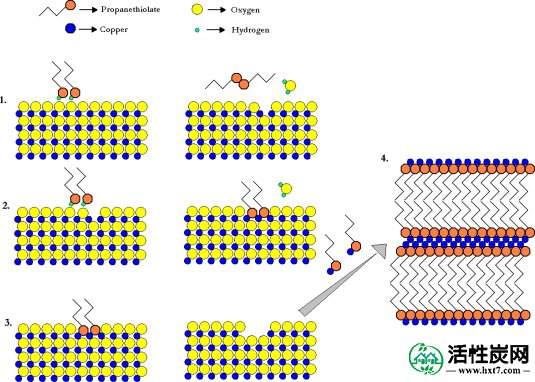
提出的反应机理发生在CACCu和丙硫醇之间在298K和1巴下形成铜(I)丙硫醇盐晶体。(1)还原/氧化形成二硫化物和Cu 2 O.(2)置换以在CuO表面上形成丙烯硫醇的自组装单层。(3)溶解铜(I)丙硫醇盐以暴露材料的新鲜表面。(4)自组装的多层铜(I)丙硫醇盐的结晶。
提供图5是为了说明在这些条件下将硫醇吸附到含铜吸附剂上的所提出的主要机理。首先,众所周知的氧化还原化学发生在CuO和硫醇之间,导致表面上的二硫化物和Cu 2 O位点。接着进行Cu 2 O与硫醇的置换反应,在这种情况下,在表面上形成丁硫醇铜(I)。应该注意的是,此时,SAM已经有效地形成在表面上。事实上,CuO的表面上形成SAM已经报道发生[ 2, 9]。由于铜(I)丙硫醇盐晶体与吸附剂材料分开形成,因此表面物质必须溶解到进料液体流中并迁移到另一部位结晶。因此,该机理在揭示材料中的大量CuO方面非常有效,使其可用于参与硫醇的吸附。
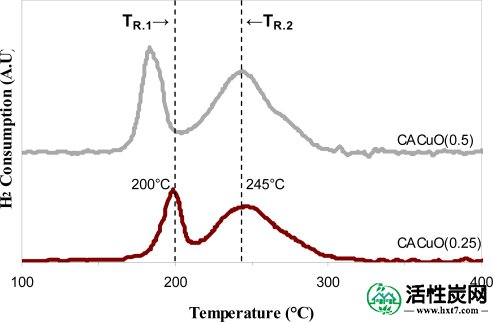
程序升温减少。
通过H 2流中的TPR测量评估合成催化剂的还原性,结果显示在图5中。主要反应在150至300℃的温度范围内显示出两个峰。这些峰被解释为对应于CuO的逐步还原[ 15 ]。较低温度下的峰值对应于Cu 2+向Cu +的还原,而相对高温下的峰值对应于Cu +向Cu 0的还原[ 17 ]。在CACCu(0.5)的情况下,在较低温度(185℃,TR 1)下观察到第一个峰)而不是CACCuO(0.50)催化剂(197℃),因为氧化含量的变化促进了在较低温度范围内的氢消耗。类似地,引入更多氧化基团引起第一和第二峰向更低温度的转变。这些峰值位移表明,在CACuO(0.25)和CANCu(0.50)催化剂中,CuO向Cu的还原更容易发生,因为酸和碱性基团的发展增加了氧迁移并允许CuO释放的氧更活跃地迁移到催化剂表面。
图5显示具有最高Cu量的活性炭是CACuO(0.5),其显示出比用0.25M硝酸铜改性的活性炭更高的强度。
图6显示了丙烷硫醇在活性炭上的吸附随初始浓度的变化。
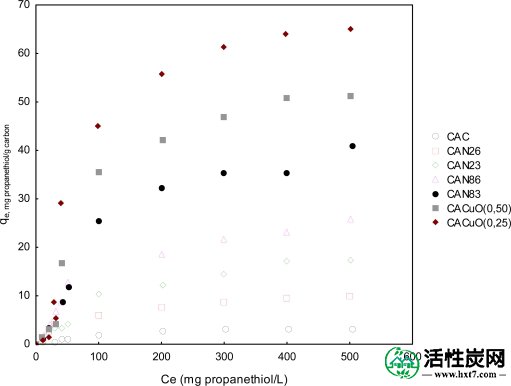
丙硫醇吸附等温线。
如图所示,吸附在原始活性炭(AC)上的丙硫醇的量随时间增加并达到平台。丙硫醇在酸 - 金属处理的活性炭的表面上物理吸附,例如通过分散力吸附。吸附在处理过的活性炭上的丙硫醇的量也随时间增加。在酸处理的活性炭的情况下,丙硫醇的吸附随着用于处理的HNO 3溶液的浓度而增加,比用铜处理的那些更多。因为活性炭上的酸性基团的数量随着HNO的浓度而增加。3溶液中,吸附的丙硫醇量必须受酸性基团的影响。关于羧基的影响,先前已经报道了在干燥和潮湿条件下通过空气中的氧气将甲硫醇氧化成二甲基二硫醚的催化作用,其值与该工作中获得的值一致。因此,认为其他因素,例如甲基硫醇的羧基和硫醇基之间的氢键而不是甲硫醇的氧化,在丙硫醇的吸附增加中起作用。
表4示出了将Freundlich模型的实验数据时所获得的吸附常数[ 8, 9 ]; 与其他样品相比,CAN86和CACuO(0.25)样品的K F值(分别为6.63和7.21)显示最高值,表明这些样品的吸附容量更高。当分析相关系数时,观察到它们落在0.993-0.879之间的范围内,表明高分散并且表明该模型没有充分描述丙烷硫醇从己烷溶液吸附到固体上。图7显示了Freundlich模型的虚线。
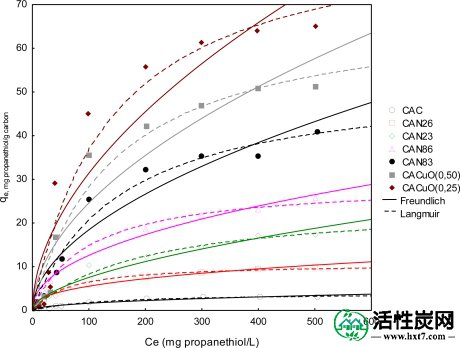
吸附等温线:Langmuir和Freundlich模型。
Freundlich模型常数。
| 碳 | K F(mg / g)(L / mg)1 / n | ñ | R 2 |
|---|---|---|---|
| CAC | 0.47 | 3.12 | 0.972 |
| CAN83 | 1.11 | 2.45 | 0.955 |
| CAN86 | 6.63 | 5.41 | 0.993 |
| CAN26 | 3.19 | 2.87 | 0.879 |
| CAN23 | 3.62 | 6.33 | 0.918 |
| CACuO(0.50) | 5.38 | 2.78 | 0.974 |
| CACuO(0.25) | 7.21 | 3.16 | 0.952 |
表5显示了实验数据的调整,以适应Langmuir模型[ 8, 9 ]。吸附常数和R 2显示出0.996-0.982的减小范围,这表明该模型更适合于在等温线中获得的实验数据。
Langmuir模型常数。
| 碳 | q m(mg / g) | K L(L / mg) | R 2 |
|---|---|---|---|
| CAC | 3.731 | 0.014 | 0.996 |
| CAN83 | 14.706 | 0.013 | 0.982 |
| CAN86 | 21.739 | 0.031 | 0.990 |
| CAN26 | 27.027 | 0.021 | 0.983 |
| CAN23 | 10.870 | 0.021 | 0.997 |
| CACuO(0.50) | 40.000 | 0.066 | 0.997 |
| CACuO(0.25) | 43.478 | 0.085 | 0.995 |
对于浸渍有铜的活性炭样品,发现的最大吸附量的较高值与浸渍焓的结果一致; K L常数值表明丙二硫醇在这些样品中的高吸附性。对于通过表面氧化改性的样品,CAN26显示出最高的吸附值,即用6M硝酸溶液改性的样品,因此显示了表面化学对丙硫醇吸附的影响。图7显示了这个模型与实线的拟合; 发现该模型更适合,因此充分描述了丙硫醇在活性炭上的吸附。
两个动力学模型进行了研究,所述伪第一和伪二阶[ 8,9,14 ]。图8显示了在活性炭表面上作为时间吸附的溶质所获得的实验结果,其在约800分钟后变得饱和。CACuO(0.25)样品对丙硫醇的吸附能力最高,原始活性炭最低(36%)。
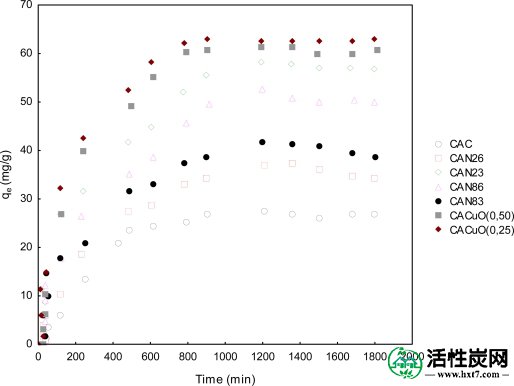
去除丙硫醇的动力学。
表6显示了合成的每种活性炭样品在平衡时吸附的丙硫醇的量,使用伪一级模型,恒定动力学和相关因子R 2在0.982-0.963之间。这些值表明实验数据的分散。
伪一级反应的常数动力学。
| 碳 | q e(mg / g) | k 1(min -1) | R 2 |
|---|---|---|---|
| CAC | 28.50 | 0.003 | 0.982 |
| CAN23 | 35.59 | 0.003 | 0.984 |
| CAN26 | 40.29 | 0.003 | 0.963 |
| CAN83 | 48.47 | 0.002 | 0.971 |
| CAN86 | 54.27 | 0.002 | 0.982 |
| CACuO(0.50) | 57.86 | 0.004 | 0.975 |
| CACuO(0.25) | 58.15 | 0.003 | 0.982 |
伪二阶模型比CACuO更适合CAN。相关系数在0.997-0.983之间优于Freundlich模型。表7显示了平衡吸附的丙硫醇量,模型的速度常数和相关因子; 这些值取自模型的线性化。
伪二阶模型常数。
| 碳 | q e(mg / g) | k 2(g / mg.min) | R 2 |
|---|---|---|---|
| CAC | 33.33 | 0.00010353 | 0.997 |
| CAN23 | 41.67 | 9.7166E-05 | 0.983 |
| CAN26 | 47.62 | 8.7171E-05 | 0.986 |
| CAN83 | 62.50 | 5.9660E-05 | 0.988 |
| CAN86 | 66.67 | 6.3238E-05 | 0.993 |
| CACuO(0.50) | 66.67 | 0.00011943 | 0.997 |
| CACuO(0.25) | 71.43 | 0.00012785 | 0.995 |
通过与先前的动力学模型比较,可以确定丙硫醇去除到二速动力学的动力学,因为该模型以较小的分散度调整实验数据。
在约800℃下通过蒸汽物理活化由商业椰壳衍生的碳源制备的活性炭(CAC)用作本研究中的催化剂载体。在使用之前,AC支持物用浓度为3和6M的硝酸溶液预处理以进行化学改性。索氏提取设备用于该程序,并加入150mL含有20g活性炭的溶液并加热2-8小时。用热水洗涤活性炭,直至其在改性后达到6.5的恒定pH。酸处理的载体如下指定:(a)酸处理的活性炭(CAN23):用HNO 32M 处理CAC 2小时; (b)酸处理的活性炭(CAN26):CAC用HNO 3 2 M处理6小时; (c)酸处理的活性炭(CAN83):用HNO 3 8M 处理CAC 3小时; (d)酸处理的活性炭(CAN86):用HNO 38M 处理CAC 6小时。
通过用适当浓度(0.25M和0.5M)的前体(硝酸铜,Cu(NO 3)2 ·3H 2 O)的水溶液浸渍预处理的CAC来制备CuO / CAC催化剂。Cu负载量约为3%(重量)。在浸渍过程中,将溶液在70℃下加热并持续搅拌直至液体完全消除。然后,将催化剂在110℃下干燥2小时,随后在流动空气中在450℃下煅烧2小时。在450℃的煅烧步骤期间CAC负载的催化剂的近似重量损失为约20%。从初始载体量和Cu(NO 3)2 ·3H 2估算涂覆的CuO的初始量O.经铜处理的载体如下指定:(e)酸处理的活性炭(CACuO(0.25)):用0.25N的CuNO 3处理CAC ; (f)酸处理的活性炭(CACuO(0.5)):CAC用CuNO 3 0.5M 处理。
在体积系统(Autosorb-3B,Quantachrome)中测量77K下的N 2吸附等温线。对于吸附数据分析,使用Dubinin-Radushkevich方程(DR)。将活性炭样品(约0.100g)在Autosorb 3B(Quantachrome Co.)中在523K下脱气3小时。在该设备中在77K [ 5 ] 获得相应的吸附氮等温线。
活性炭的碱性和酸性位点通过Boehm使用0.1M HCl,NaHCO 3, Na 2 CO 3和NaOH溶液[ 6 ] 提出的滴定方法测定。在该方法中,将50mL溶液与玻璃烧瓶中的0.500g活性炭在298K的恒定温度下接触48小时。用相应的0.1M溶液滴定10mL样品。使用Trito Line Alpha Plus(SCHOTT Instruments,Woburn,MA,USA)进行滴定[ 4 ]。
活性炭的浸入焓的测定在水和丙硫醇中进行。使用局部结构的Calvet型热传导微量热计[ 23 ]来确定浸入热量。向细胞中加入8mL液体。将重约0.100g的活性炭样品置于玻璃安瓿内的量热单元中。当设备达到平衡温度时,玻璃安瓿被破坏; 记录并电气校准产生的热效应。
在使用该技术进行测量之前,将活性炭样品浸渍以获得细粉末。将粉末置于载体中以测量X射线光谱,数据以0.02°/ min的间隔从2至180°获得。使用Rigaku Mini Flex设备进行测量。
使活性炭样品达到每分钟50mL的氢气流量。逐渐升高温度,以确定发生还原的温度。使用具有He / H 2(10:90)混合物的MICROMERITICS 2720化学计量器。
用于获得平衡等温线的方法是分批式系统。活性炭称重千克的样品放置在250毫升丙硫醇在Ñ在锥形瓶中-己烷溶液(30-500 ppm)表示。搅拌溶液并保持恒温以达到平衡。1毫升每种样品的的等分试样通过气相色谱法,使用Shimadzu QP2010加GC-MS配备有火焰离子化检测器[分析9,10 ]。
进行实验以确定活性炭除去丙硫醇的动力学在室温和大气压下进行。将固体预先在炉中干燥至100℃,保持24小时,然后称重,将约1,000g各自置于150mL在己烷中的500ppm丙硫醇溶液中,并转移到锥形瓶中,然后将其密封,定期采样。通过气相色谱分析样品[ 9 ]。
当通过硝酸和Cu(NO 3)2改性时,商业AC的表面化学和结构性质发生变化不同浓度的溶液。如通过程序升温还原和X射线衍射所确定的,在AC表面上存在CuO对应于用铜盐浸渍。取决于活性炭表面上的氧化基团的量,丙二硫醇被改性的碳吸附。用0.25M硝酸铜溶液获得显示出最高丙硫醇保留的活性炭。已经证明,通过改变AC的化学和质地,丙硫醇吸附可以增加84%。对于由硝酸溶液改性的AC,最重要的因素是浓度。