发布日期:2018-11-14 09:58 来源:活性炭网 作者:活性炭网 浏览数:
生物滞留,也称为雨水花园,允许雨水通过土壤介质浸入地下,从而去除颗粒物和溶解的污染物,减少峰值流量。 尽管土壤有机质(SOM)在吸附许多污染物方面是有效的,但是已经提出
来自城市地区的地表径流是城市溪流洪水和侵蚀的主要原因,也是接收水体的主要污染源。生物滞留和雨水花园是绿色基础设施的例子,通过收集和储存水,帮助维持或恢复雨水的自然流动模式,使其渗透到地下,去除污染物,并为地下水位和天然溪流补给(欧盟委员会2013 ;美国环保局2014年 ; Waterbucket 2014)。生物滞留和雨水花园可以互换使用,但生物滞留倾向于用于具有更详细设计标准的大规模系统。这两个系统都是由景观中的浅层种植凹陷构成,允许来自不透水区域的地表径流通过介质(通常是原生土壤或工程土壤)浸入地下。这减少了峰值流量和流量,并促进了雨水中微粒和溶解污染物的去除(Davis等人2009 ; Grebel等人2013 ; LeFevre等人2014 ; Muthanna等人2007 ; Trowsdale和Simcock 2011)。Cu和Zn等金属在污染的雨水中以颗粒和溶解形式存在(Camponelli等。2010年 ; 莫里森等人。1990)。最近的研究表明,疏水性有机污染物,包括,例如,多环芳香烃(PAHs),也存在于胶体和雨水(溶解相布朗2002 ; Kalmykova等人2013 ; Kalmykova等人2014 ; Zgheib等人2011)。研究表明,除了颗粒沉降之外,吸附和生物降解是生物滞留和雨水园中主要的碳氢化合物去除机制,尽管挥发和植物吸收也是可能的途径(LeFevre等人2014 ; LeFevre等人2012a ; Zhang等人。2014)。鉴于吸附是有机污染物的主要去除过程,生物滞留介质的性能是必不可少的。目前,生物滞留和雨园的性能数据非常少,特别是与有机化合物的去除有关(Davis等人2009 ; DiBlasi等人2008 ; Grebel等人2013 ; LeFevre等人2012a ; Zhang等人) 。2014)。现有研究表明,这些系统可有效去除雨水中的有机污染物; 对于疏水性化合物,如石油烃和轻质多环芳烃,可预期进入负荷减少80-90%(DiBlasi等人,2008 ; Hong等人,2006 ; LeFevre等人。2012a)。
为了进一步加强雨水中污染物的去除,已经提出用生物炭,粉煤灰和水处理残留物修改生物滞留介质(O'Neill和Davis,2012 ; Tian等,2014 ; Zhang等,2008)). However, studies on media amendment to enhance the removal of organic pollutants are to date very limited. The hypothesis is that media amended with efficient adsorbents exhibit limited pollutant migration, and delayed saturation and loss of sorption capacity compared to non-amended media. This would lead to lower media replacement frequency, hence lower costs of maintenance. Contaminated soils amended with activated carbon and biochar exhibit reduced mobility and bioaccumulation of metals (e.g. As, Cd, Pb and Zn) and organic compounds (e.g. PAHs and the herbicide atrazine) compared to non-amended soils (Beesley and Marmiroli 2011; Bian et al. 2014; Jakob et al. 2012; Wang et al. 2014; Ulrich et al. 2015)。在之前的研究中(Björklund和Li 2017),我们已经证明,生活污水污泥产生的活性炭是一种有效的吸附剂,用于去除疏水性有机化合物(HOCs),如PAHs,邻苯二甲酸盐和烷基酚。
尽管活性炭对于从水中去除HOC非常有效,但是雨水中溶解的有机物(DOM)的存在可能通过竞争吸附剂表面上的吸附位点和大DOM分子阻塞孔而对HOC吸附产生负面影响(Kilduff等)人。1996年,李等人。2003 ; Pelekani和Snoeyink 1999年 ; Quinlivan等人。2005)。在先前的污水污泥基活性炭(SBAC)测试中,由于HOC的水溶性低和SBAC的高吸附能力,批次吸附测试被认为是无效的,导致碳的低饱和度以及HOC和DOM之间的竞争很小。在连续流动系统,如柱的研究中,吸附剂最初只部分地加载了肝卵圆细胞和DOM,但更多的肝卵圆细胞和DOM不断进入系统,可能导致吸附网站竞争(Li等2003)。因此,必须在柱研究中测试SBAC,其中HOC和DOM的连续流入可能影响吸附剂的性能。
本研究的目的是研究与未经修正的培养基相比,用SBAC修正的土壤生物滞留培养基是否会提高雨水中经常检测到的HOC的去除效率。本研究的范围仅限于溶解HOCs的吸附; 除去颗粒结合污染物。该研究的目的是(i)比较批量吸附试验中生物滞留介质中SBAC和土壤有机质(SOM)的吸附能力; (ii)使用柱试验比较生物滞留培养基中添加和不添加SBAC的HOCs的去除情况; (iii)确定HOCs从污染的生物滞留介质中的解吸附。这些目标基于以下假设:(i)土壤中的有机物质,通常为0-5%w / w在生物滞留媒介(Fassman等人,2013 ; Rouhi和Schwartz,2007)中,通常可有效捕获HOC和其他污染物(Chefetz等,2000 ; Chiou等,1983)。然而,由于SBAC的大表面积(约700 m 2 / g [Björklund和Li 2017 ])和微孔性(适用于HOC吸附),假设吸附到SBAC上高于SOM (Smith等人2009))。(ii)由于SBAC的高吸附能力(Björklund和Li 2017),未经修正的培养基将在SBAC修正培养基之前达到HOC的突破; (iii)HOCs对土壤的吸附是可逆的,吸附的污染物可能会因例如土壤性质的变化和与胶体物质的共同运输而解吸(Badea等人,2013 ; Durjava等人,2007)。
筛选研究表明,PAHs,邻苯二甲酸盐和烷基酚在城市径流中普遍存在,并且经常在超过欧洲和加拿大水质标准的浓度下检测到(Björklund等人2009 ;Björklund等人2011 ; Bressy等人2012 ; Clara等人)人2010 ; Zgheib等人2011)。本研究中包括的特定有机化合物如下:三种PAH(芴,蒽和芘;分别为2.5,3和4个芳环); 两种烷基酚(4-非苯酚和4- 叔辛基苯酚); 和两种邻苯二甲酸酯(邻苯二甲酸二丁酯和邻苯二甲酸二(2-乙基己基)酯)。化合物的选择的物理-化学性质列于表表1 1。
首字母缩略词,CAS识别号和所选有机化合物的物理化学性质
| 化学名称(缩写) | CAS编号 | MW(g / mol) | 水溶性a(mg / l) | 记录K owb | K oc b |
|---|---|---|---|---|---|
| 多环芳烃 | |||||
| 芴(FL) | 86-73-7 | 166 | 1.8 | 4.02 | 4241 |
| 蒽(ANT) | 120-12-7 | 178 | 1.3 | 4.35 | 7274 |
| 芘(PYR) | 129-00-0 | 202 | 7.7×10 -2 | 4.93 | 17180 |
| 酚类 | |||||
| 4- 叔丁基苯酚(OP) | 140-66-9 | 206 | 19 | 4.12 | 10,290 |
| 4-壬基酚(NP) | 84852-15-3 | 220 | 5.4 | 4.48 | 18970 |
| 邻苯二甲酸盐 | |||||
| 邻苯二甲酸二丁酯(DBP) | 84-74-2 | 278 | 9.9 | 4.57 | 1919年 |
| 邻苯二甲酸二(2-乙基己基)酯(DEHP) | 117-81-7 | 391 | 2.5×10 -3 | 7.50 | 99470 |
一个 DEFRA 2008 ; 欧洲央行2002年,2004年,2008年 ; 麦凯等人。2006年
b记录来自KOWWIN™(v1.68)的K ow值和来自EPI Suite™的KOCWIN™的K oc(US EPA 2012)
该媒介是从一个雨水花园采样的,该花园接收来自屋顶的径流和来自草地区域的次要地表径流。雨水花园在抽样时已经运作了1。5年。使用干净的桶和铲子从表面下方约50-300mm处取样。该培养基,以下称为土壤,是以Cascade Ecomedia名称销售的工程化土壤,由Cascade Envirotech(Aldergrove,BC,Canada)开发。在用于我们的实验之前,将该土壤储存在4℃的黑暗中。在筛分的土壤(<2 mm)中,几乎90%的土壤颗粒≤250μm,pH = 4.3,颗粒密度= 2.54 g / cm 3,灼烧损失= 3.75%(更多细节见补充材料和Björklund和李2016)。浸出试验(Björklund和Li 2016)显示所研究的HOC中没有一种以可检测的量从土壤中释放出来。
在Gong(2013)和Björklund和Li(2017)中详细描述了SBAC的生产和材料的特性。碳源是来自生活污水处理试验工厂的干燥污泥。将污泥浸泡在活化剂ZnCl 2中,并在T final = 500℃下通过热解碳化。将最终的碳产物研磨并用HCl和蒸馏水洗涤,最后干燥(105℃)并储存在琥珀色玻璃瓶中。活性炭的pH,表面积和灰分含量分别为3.4,700m 2 / g和9%(Björklund和Li 2017)。
4-壬基苯酚(85%含量的标准对位,芴,蒽,芘,邻苯二甲酸二丁酯,二(2-乙基己基)邻苯二甲酸酯,苊-d -异构体)10,苯酚- d 6,苯甲酸苄酯和菲d 10和腐殖酸(HAs)购自Sigma-Aldrich,并且Fluka提供4- 叔辛基苯酚。在从Caledon Laboratories Ltd.获得的甲苯中制备有机化合物的储备标准溶液(终浓度约5000ng /μL),并且在Fisher Scientific的丙酮中制备掺加水样品的工作标准(最终浓度约100ng /μL) 。Acenaphthene-d 10苯甲酸苄酯和苯甲酸苄酯用作替代标准,而苯酚-d 6和菲-d 10用作内标。在甲苯中制备分析物的内标和校准标准品。将所有溶液储存在-18℃的琥珀色玻璃瓶中直至使用。
在Björklund和Li(2015)中详细描述了水中HOC的液 - 液萃取(LLE )。简而言之,用3×25mL二氯甲烷(DCM,来自Fisher Scientific)同时提取HOC,用N 2蒸发至干,并用甲苯重构提取物。从“ 污染土壤中的HOC负荷的测定 ”部分中描述了从土壤中提取HOC。
在GC-MS分析之前,将内标物(苯酚-d 6和菲-d 10)加入到提取物和校准溶液中。使用GC-MS的分析程序对于水和土壤样品都是类似的,并且在Björklund和Li(2015)中有详细描述。使用气相色谱保留时间和至少三种离子的质谱图谱鉴定化合物。为了定量,为所有目标化合物制备六点校准曲线。对于来自柱试验的水和土壤样品,来自批次吸附试验(参见“ SBAC和SOM的批量吸附试验”部分)的样品的浓度范围分别为2.5-150和2.5-50μg/ L(参见“ 列测试 “和”分别测定污染土壤 “ HOC ”中的HOC负荷。
为了比较SBAC和SOM的吸附容量,进行了批量吸附测试。该测试与之前关于HOCs的BAC吸附(Björklund和Li 2017)的研究类似地进行,以获得可比较的结果。超纯水(用来自Millipore一个协同UV的Milli-Q系统纯化)的一百五十毫升与七个肝卵圆细胞(表的混合物掺加(表1)1)至终浓度为100μg/ L的各化合物。将15毫克SBAC或SOM与HOC溶液在端对端转筒中接触24小时。在SOM样品中,使用对应于15mg OM的土壤质量(衍生自测定的有机物含量,参见补充材料)。通过以2000× g离心除去固相持续10分钟 提取液相并通过GC-MS分析(参见“ 水样中有机化合物的提取和分析”部分)。所有样品一式两份制成。对于所有批次,按照相同的程序制备基质空白和基质加标,以分别确定污染和分析物的损失。
在连续流动试验中使用三个柱:两个用0.5%(w / w)SBAC修正土壤的柱子和一个带有未修正土壤的对照柱子。所选的修正剂量已被其他研究人员使用,例如Tian等。(2014年)。为了确保均匀的材料,将土壤过筛以除去标称尺寸> 2mm的颗粒和长植物纤维。在雨水渗透期间吸附到介质上并且是动力学过程,因此取决于中等污染物接触时间,即渗透速率。典型的生物截留和雨水花园渗透速度是50-200毫米/小时(一般接近100毫米/小时)和干土壤堆积密度是0.8-2.0克/厘米3(通常为1.5g / cm 3)(大温哥华污水和排水区2012 ; KWL 2012 ; Rouhi和Schwartz 2007)。根据圆柱形芯方法(D7263 [ASTM 2009 ])和根据D2216(ASTM 2010)的水分含量测定土壤堆积密度。使用比重瓶法和容量瓶方法测定的颗粒密度(比重)(D854 [ASTM 2014 ])。所有参数均在一式三份样品上测定。
所有柱组件均为不锈钢。柱的内部尺寸如下:直径114毫米,高51毫米。列的详细描述和示意图可在Li(2011年)中找到)。在使用之前,柱装置的所有组分用洗涤剂和水洗涤,然后用丙酮冲洗。选择高宽比<1是因为增加柱的宽度可以降低优先和侧壁流动的可能性,这在高高宽比高的柱子中容易发生,导致固体材料与合成材料之间的接触较差雨水。为了进一步防止侧壁泄漏,柱的内壁涂有一层薄的膨润土浆液(水分含量~200%)。在柱的顶部和底部使用多孔石头以防止优先流动。通过在超纯水中在室温下超声处理1小时来清洁石头,然后煮沸30分钟以去除气穴。根据D698(ASTM2012)。柱中产生的堆积密度为1.22g / cm 3,在生物滞留和雨水园中观察到的密度范围内,但在下端。从体积和颗粒密度(2.54g / cm 3),平均孔体积估计为227cm 3(Budhu 2007)。将SBAC均匀地铺展在填充土壤层的顶部(即最靠近出口)两列中。
柱子在恒定的向上水流下操作,这通常导致比向下流动的柱子浸出更均匀的流动。该系统用合成雨水喂养:自来水中加入腐殖酸原料至最终溶解有机碳(DOC)浓度约为20 mg / L,并加入HOCs的工作标准,最终浓度为50μg / L七个HOC中的每一个。合成雨水每天两次在三个串联的加压不锈钢容器中制备,总体积为20L(由于实际原因不能使用重力流)。系统的流速由三个并联的蠕动泵控制,使用Teflon管连接到不锈钢容器和柱的入口。每个泵设定为6.4 mL / min,导致渗透率为44.7毫米/小时。该速率略低于设计建议(50 mm / h),但由不锈钢容器的总体积决定。在柱的出口处也使用特氟隆管来排出流出的水。每隔12小时(对应于每20个孔体积)在35分钟内将流出的水样品收集在琥珀色玻璃瓶中,每个样品对应于一个孔体积。将样品在4℃的冷室中储存不超过4天,直至提取和GC-MS分析。对于所有批次,制备基质加标和空白,并与柱洗脱液样品一起分析。在28天(对应于1000孔体积)的连续流动后终止实验。但是由不锈钢容器的总体积决定。在柱的出口处也使用特氟隆管来排出流出的水。每隔12小时(对应于每20个孔体积)在35分钟内将流出的水样品收集在琥珀色玻璃瓶中,每个样品对应于一个孔体积。将样品在4℃的冷室中储存不超过4天,直至提取和GC-MS分析。对于所有批次,制备基质加标和空白,并与柱洗脱液样品一起分析。在28天(对应于1000孔体积)的连续流动后终止实验。但是由不锈钢容器的总体积决定。在柱的出口处也使用特氟隆管来排出流出的水。每隔12小时(对应于每20个孔体积)在35分钟内将流出的水样品收集在琥珀色玻璃瓶中,每个样品对应于一个孔体积。将样品在4℃的冷室中储存不超过4天,直至提取和GC-MS分析。对于所有批次,制备基质加标和空白,并与柱洗脱液样品一起分析。在28天(对应于1000孔体积)的连续流动后终止实验。每隔12小时(对应于每20个孔体积)在35分钟内将流出的水样品收集在琥珀色玻璃瓶中,每个样品对应于一个孔体积。将样品在4℃的冷室中储存不超过4天,直至提取和GC-MS分析。对于所有批次,制备基质加标和空白,并与柱洗脱液样品一起分析。在28天(对应于1000孔体积)的连续流动后终止实验。每隔12小时(对应于每20个孔体积)在35分钟内将流出的水样品收集在琥珀色玻璃瓶中,每个样品对应于一个孔体积。将样品在4℃的冷室中储存不超过4天,直至提取和GC-MS分析。对于所有批次,制备基质加标和空白,并与柱洗脱液样品一起分析。在28天(对应于1000孔体积)的连续流动后终止实验。
使用Lachat Instrument IL 500 TOC分析仪,使用GC-MS(参见“ 水样中有机化合物的提取和分析 ”部分)和DOC 分析来自柱研究的洗脱液样品的HOC。该仪器后来被Dohrmann Phoenix 8000,UV-过硫酸盐TOC分析仪取代(参见“ 溶解有机物对吸附能力的影响 ”部分)。
在完成柱研究后,将来自对照柱的土壤分成三层同样厚(17mm)的层。在水分含量分析之前将这些单独的部分彻底混合(每层的三份)。根据ISO / TS 21268-2标准方法(国际标准化组织2007)确定从每层中可浸出的HOC的解吸附。搅拌24小时后,将样品(每层的一式三份)沉降10分钟,以2000× g离心10分钟,并通过934-AH玻璃纤维过滤器(Whatman)过滤。使用“ 水样中有机化合物的提取和分析 ”部分中描述的LLE方法从土壤洗脱液中提取HOC 。
土壤中HOCs的吸附负荷是在对照柱土壤各层的一式三份样品上测定的(参见“ 污染土壤中HOCs的解吸 ”部分)。将每层中HOC的浓度(μg/ g)乘以每层中已知的干土质量(g),以达到对照柱土壤中的总HOC负荷(mg)。从土壤中提取HOCs是基于Hollender等人提出的方法。(2003)和宋等人。(2002)。向大约2g潮湿的土壤中加入1.0mL替代标准品(ace -1-d 10在丙酮中加入苯甲酸苄酯,然后向小瓶中加入5mL丙酮和25mL DCM。手动摇动样品1分钟并排气以释放潜在的过量气体。然后将样品置于超声浴(40℃,VWR Scientific Products,Aquasonic,50 HT型,35kHz)中2小时并每10分钟倒置一次。将萃取物通过1.5g无水Na 2 SO 4(置于VWR的烘焙玻璃纤维滤器中,1.6μm孔径)过滤,使用旋转蒸发器蒸发至几毫升,然后用温和的N 2流完全干燥。。用1.00mL甲苯和内标物(菲-d 10和苯酚-d 6)重构提取物)在通过GC-MS分析之前(与水样相同的程序)。在未污染的土壤中,HOCs的背景浓度是在重复的非加标土壤样品上测定的。还使用相同的程序提取溶剂空白(无土壤)。
通过将所有HOC在丙酮中加入一式三份空白样品(未污染的土壤)(最终浓度为20μg/ g每种HOC)来测试提取效率。加入的样品在室温下干燥,然后加入替代物并开始提取程序。ace - d 10和苯甲酸苄酯的平均回收率分别为64%和112%。在加标样品中,HOC的回收率如下:芴47,蒽75,芘84,辛基苯酚86,壬基酚114,邻苯二甲酸二丁酯(DBP)102和邻苯二甲酸二(2-乙基己基)酯(DEHP)141%。ace- 10和芴的低回收率可能是由于它们具有较高的挥发性,而DEHP的高回收率可能是由污染问题引起的。
IBM SPSS Statistics 22程序用于执行统计分析,包括Pearson和Spearman的相关性以及Mann-Whitney U检验。Pearson的相关性表示两个变量之间的线性关系,需要正态分布的数据。Spearman的秩相关通过将每个变量转换为等级来工作,并且在数据不满足关于正态性和线性的假设时使用。因为使用分区系数K ow的对数,所以使用秩检验来测试涉及K ow的相关性。Mann-Whitney U.当数据不是正态分布时,test用于比较两个独立组之间的差异。使用Shapiro-Wilk测试测试正态性:如果p > 0.05,则数据分布与正态分布没有显着差异。
在批量测试中,平衡时的吸附容量q e(μg/ g)使用
其中C 0和C e分别是水相中HOC的初始和平衡浓度(μg/ L); V是溶液的体积(L); 和米是吸附剂(G)的重量。
柱研究的结果通常使用突破曲线报告:x轴上的时间(t)或孔体积(V)和y轴上的C / C 0的图,其中C是样品中的HOC浓度在特定时间或孔体积,C 0是初始HOC浓度(在该研究中为50μg/ L)。突破时间是任意设定的; 在目前的研究中,我们使用C / C 0 = 0.10,即在流出物中检测到10%的初始浓度。
这项研究背后的假设之一是修正案延长了介质的使用寿命,然后才发生饱和,污染物浸出变得不可接受。在这个例子中,我们使用芴来计算SBAC带来的增强吸附能力,与未经修正的土壤相比。
从柱流出物浓度和合成雨水的施加体积,计算对照和SBAC修正柱之间去除的芴负荷的差异。然后将柱中的SBAC和土壤质量按比例放大以匹配1m 2生物滞留或雨水中的SBAC和中质量。假定介质深度为0.5μm(Fassman等人2013 ; KWL 2012),即1米2生物截留或雨花园对应至0.5μm 3土壤。然后计算通过0.5%(w / w)SBAC修正至1m 2生物滞留(0.5m 3)去除的芴负荷。
在住宅区,由于不透水面的百分比较低,每平方米的生物滞留或雨水通常与流量较大的道路连接到较大的贡献流域。另一方面,住宅的污染物浓度通常低于交通繁忙的地区。因此模拟了两种情景:(1)生物滞留受到来自居民区的径流,其中芴浓度低(0.05μg/ L),径流系数ɸ= 0.35,生物滞留面积的面积为2%。流入生物滞留的不透水区域; (2)生物滞留从交通区域接收径流,其中芴浓度高(1μg/ L),ɸ= 0。8,生物滞留表面积的大小是排入生物滞留的不透水区域的10%。从StormTac数据库获得有关芴浓度,径流系数和不透水/透水面积的数据(2016),Tegelberg和Svensson(2013)以及Campbell等。(2013年),分别。在兰利,BC,加拿大(1375毫米)年降水量使用这些假设,一起,年径流量和相应的芴负荷排出到1m 2生物截留在住宅和业务区域估计。最终,将两种情景估算的年芴负荷与1 m 2生物滞留中去除的芴量进行比较,修正后用0.5%SBAC进行修正。
使用以下公式计算可以吸附到土壤中的HOC 的理论最大质量,m ads(mg):
其中K oc是土壤和水相之间的有机碳标准化分配系数; f oc是土壤有机质含量的质量分数(0.0375); 和米 土壤是在列中的土壤质量(g)。ķ OC是衍生自文献值ķ 流(表(表11)。
解吸系数K des(L / kg)是土壤相中残留的HOC含量与水溶液中解吸化合物的质量浓度之比,由
哪里
与SOM接触的HOC的吸附显着低于SBAC。在土壤的批量试验中,邻苯二甲酸酯DBP和DEHP的初始浓度(C 0)和最终浓度(C e)之间的差异仅为每升几微克,即非常低的吸附容量。土壤对壬基酚和辛基酚的吸附能力 分别比SBAC的容量(q e, SBAC≥900 )低5(q e,SOM =200μg/ g)和8(q e,SOM =120μg/ g)。两种烷基酚的μg/ g)(Björklund和Li 2016 )。所有HOCs在SOM上的平均吸附容量显着低于SBAC(Mann-Whitney U = 1.00,p = 0.003,双尾)。对于PAHs观察到使用土壤的最高去除率,去除了70%的芘,对应于q e,SOM =660μg/ g,而去除了约30%的芴和蒽,对应于q e,SOM = 270和200μg/ g。这些结果表明SOM具有吸附大量HOC的潜力,因为它具有吸附能力和丰度(≤5%w / w)在一些用作生物滞留介质的工程土壤中。实际上,SOM由非极性基团控制,例如脂族和芳族部分,它们是HOC的重要吸附位点(Kyoichi 1987)。然而,由于疏水位点丰富且表面积大,SBAC的吸附能力优于SOM(Björklund和Li 2017)。因此,如果修改为生物滞留和雨水土壤,SBAC有可能增加补充污染物的去除和储存。
对于不同的化合物,在非常不同的孔体积下达到突破(C / C 0 = 0.10)。通常,每组中最不疏水的化合物 - 芴,辛基酚和DBP(log K ow = 4.02-4.57) - 表现出较短的穿透时间,并且在流出物中观察到的浓度高于疏水性更强的化合物。这种趋势在芴,壬基酚和芘(图的穿透曲线所示(图1)。1)。硒,辛基酚和DBP的突破曲线见补充材料,图S2。芴的突破在200个孔体积(图达到(图1a),1a),之后出水浓度介于进水浓度的10%至30%(50μg/ L)之间。 在所有三个柱中,辛基酚在100个孔体积内达到C / C 0 = 0.10,这是所有测试化合物的最短穿透时间(图S2)。DBP的出水浓度变化很大; 在约180个孔体积后达到突破,并且 在孔体积450和650之间达到C / C 0 = 0.30-0.40,但随后稳定在C / C 0 = 0.05-0.20,对照柱的流出物浓度更高(图S2)。辛基酚显示出与孔隙体积450及以后的DBP相似的行为。DBP和辛基酚的流出物浓度的时间限制增加可取决于吸附达到其容量之前所需的平衡时间,如先前报道的,例如Ulrich等人。(2015年)。在实验过程中的整个过程中,突破(0.10)从未蒽(图达到(除外离群值)S2),芘和壬基酚(图(图1a,1 A,C),该邻苯二甲酸酯DEHP,其是研究最疏水的化合物(log K ow = 7.5),表现出不确定的结果。这可能是样品污染的结果,这通常在邻苯二甲酸酯中观察到,因为它们普遍存在于塑料材料中。另外,由于DEHP的低水溶性的(表(表1),1),这种物质可以附着到实验室器皿在水中,这是不均匀地分布在各列的表面或形成乳液,导致流入和流出的变化浓度(Julinová和斯拉维克2012)。因此,DEHP被排除在进一步的水数据分析之外。通常,所有三个柱中HOC 的平均C / C 0(所有孔体积)与化合物log K ow相关性良好 (斯皮尔曼的ρ = -0.638到-0.725)。
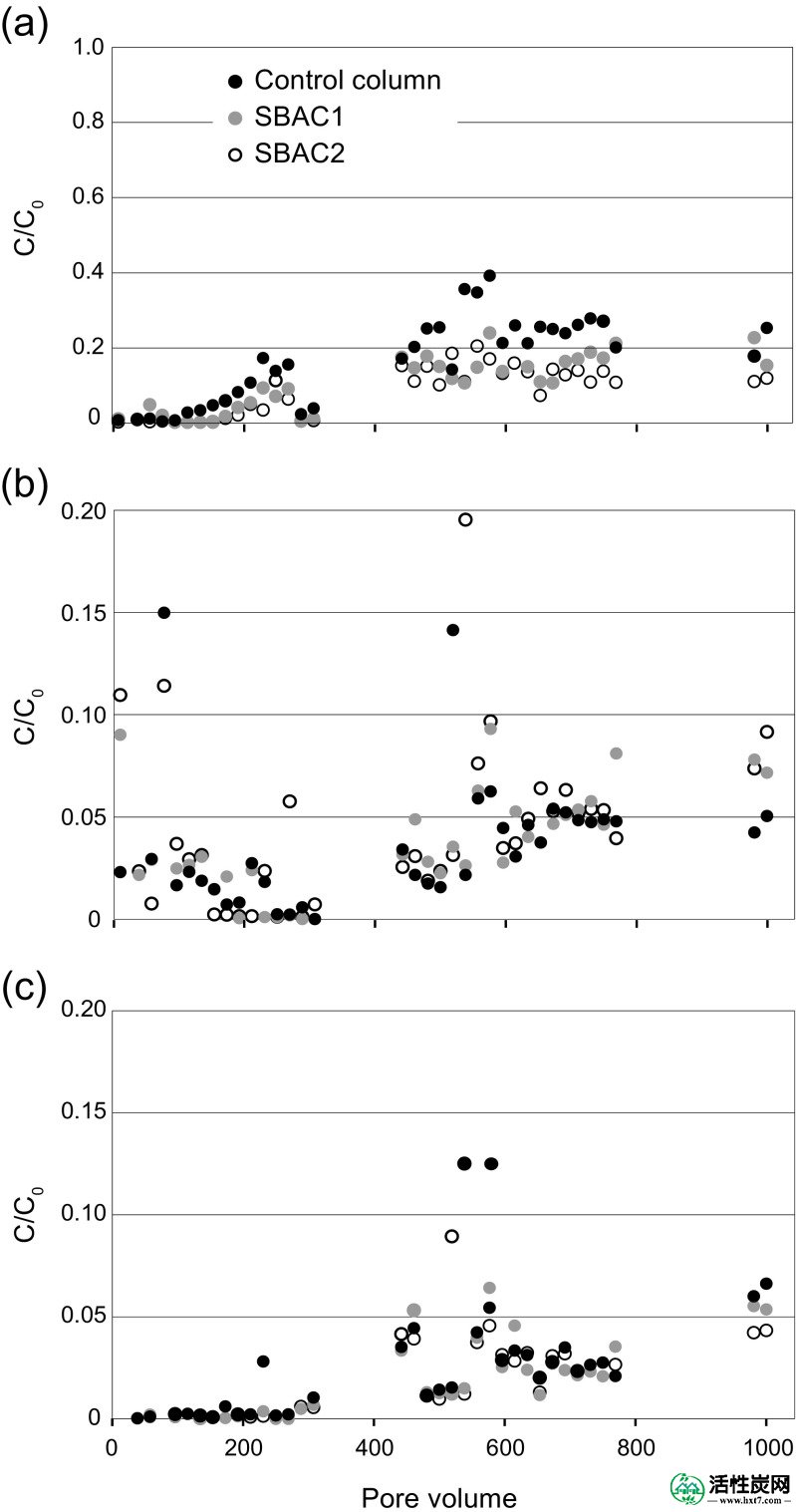
的穿透曲线一个芴(日志ķ 流量 = 4.02),b壬基苯酚(日志ķ 流量 = 4.48)和Ç芘(日志ķ 流量 = 4.93),表明流出物入口浓度比(ç / ç 0)作为的函数通过添加SBAC(0.5%w / w)的两个柱和对照柱的孔体积数。每个孔体积对应于227mL。注意y轴上的不同比例
在添加SBAC的两个柱之间,流出物浓度的差异没有统计学差异(Mann-Whitney U = 545-626,p = 0.140-0.804,双尾)。然而,对照柱中芴,辛基酚和蒽的流出物浓度显着高于SBAC的两个柱(Mann-Whitney U = 355-451,p = 0.001-0.027,双尾)。这些结果表明SBAC修改为生物滞留和雨水土壤可以增强溶解的HOC的去除和/或防止已经吸附的污染物的浸出。SBAC的修订似乎对去除中度疏水性HOC具有特别积极的作用(log K ow = 4.02-4.35)。这样做的原因观察可能是适度的疏水性化合物不表现出强吸附到SOM较高日志的化合物ķ 流,例如芘,这是在分批吸附试验所示(见“ SBAC和SOM的批次吸附试验 “ 部分)。高度疏水的化合物在很大程度上仅通过SOM去除,而疏水性较低的化合物在土壤床中更易移动,SBAC是进一步降低其流出物浓度的重要补充。
生物滞留和雨水花园通常设计为在24至72小时内排水,以防止介质中的饱和状况。床被排干以提供背靠背降雨事件的储存,适合植被的栖息地和湿干循环以促进不同的清除过程(Grebel等人2013 ; LeFevre等人2014年)。然而,在该研究中,使用连续流动系统,即饱和条件,以促进实验程序并促进介质与合成雨水之间的最佳接触。柱中的土壤可以被认为是“理想的填充”,并且假定水在土壤床上“理想地分布”(由于向上的水流,使用多孔岩石来均匀地分配进水和膨润土以防止优先流动)沿柱墙)。所有这些因素都有助于优化水和土壤之间的接触,即“最佳情况”。此外,通过使用连续流过介质,避免了由于干燥而形成的裂缝; 因此,避免了窜流。在运行生物滞留和雨水花园时,沿着植物根部和优先流动路径进行窜流是不可避免的,导致水和土壤之间或多或少有限的接触,从而限制污染物在土壤颗粒和SBAC上的吸附。另一方面,生物滞留和雨水园最常见的维护问题之一是由细沉积物和土壤压实引起的介质堵塞。植物根系在培养基中形成大孔是必不可少的,有助于保持渗透率,使土壤通气并最小化压实(Barrett等。2013)。
在先前的研究中,对于HOC混合物(Björklund和Li 2017),SBAC的最大吸附容量估计至少为85mg / g 。在目前的研究中,在实验过程中对每个柱施加的HOC负荷对应于每克SBAC约5.25mg HOC,即仅为预期最大吸附容量的6%。肝卵圆细胞到SBAC在列的相当低的吸附可以归因于从土壤床有机质浸出,主要是在该柱的实验(图的启动观察竞争(图2)。2)。土壤有机质含有大部分可溶性转化物质,称为腐殖质(Kyoichi 1987),包括疏水结构域(例如非极性脂族和芳族部分)和亲水性官能团(例如极性酚和羧基部分)。活性炭的非极性表面可以与腐殖质的非极性部分相互作用。先前的研究显示了腐殖质对活性炭的有效吸附(Daifullah等,2004 ; Kilduff等,1996)。我们假设合成雨水中的腐殖酸(20 mg DOC / L)和土壤中释放的SOM(≤80mgDOC / L)导致SBAC早期饱和,因此HOC吸附量低于先前研究的预期(Björklund和Li 2017)。遗憾的是,HOC和DOC流出物浓度无法相关,因为DOC仪器无法为某些批次运行提供正确的结果。当许多先前的样本已被丢弃或太旧而无法重新分析时,在实验的中途发现了这个问题。
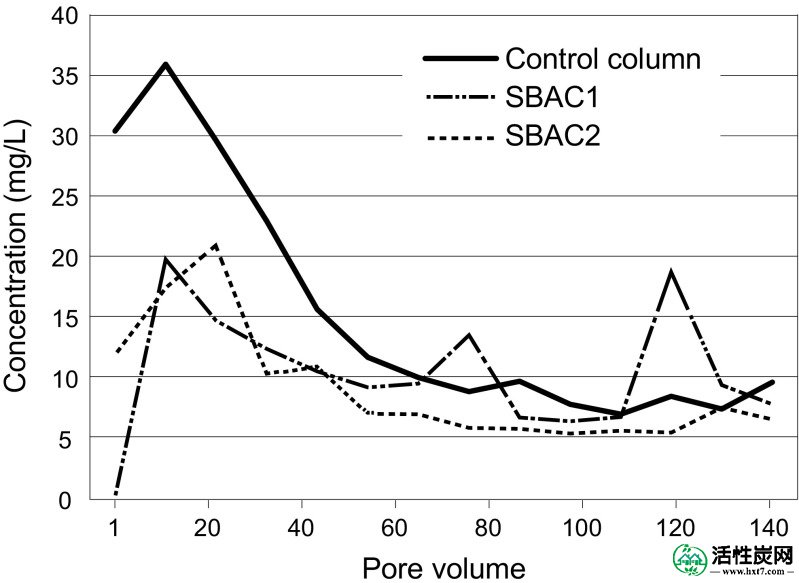
在实验的前140个孔体积(7天)中,在没有SBAC的情况下添加SBAC和对照柱的柱的流出水中的溶解有机碳浓度(DOC [mg / L])。每个孔体积对应于227mL。没有DOC添加到列中; 该图说明了从土壤中浸出的DOC
在使用HOC实验之后建立了另一个柱研究,以研究从土壤床中释放DOC(使用用于DOC分析的新仪器)。使用的装置和土壤与所述的柱试验完全相同(参见“ 柱试验 ”部分),除了将自来水(非合成雨水)送入塔中。图Figure22表明在实验开始时DOC的释放升高,并且从孔体积140稳定至<5mg / L直至实验结束(35天)。由于越来越少的可溶性有机物可用于从土壤中浸出,因此预计会有这种观察结果。随着时间的推移,DOC浸出的逐渐减少也在泥炭和堆肥的柱测试中观察到(Kalmykova等人2010 ; Mullane等人2015),而操作生物滞留和雨水花园接收新的DOC输入与雨水和退化植物。图Figure22显示了添加SBAC(≤20mg/ L)的两个色谱柱和不含SBAC(≤35mg / L)的对照色谱柱之间DOC流出物浓度的差异。与SBAC修正柱相比,对照柱的流出DOC最小,平均和最大浓度更高。这些结果表明,大部分释放的SOM被SBAC吸附,从而占据碳表面上的吸附位点并抑制HOC的吸附(Li等人,2003 ; Newcombe等人,2002)。先前的研究结果证实了这一假设,表明SBAC每克SBAC可以吸附至少20 mg DOC(以技术HA的形式)(Björklund和Li 2017)。
因为测试的HOC仅具有有限的极性(烷基酚和邻苯二甲酸酯),可以假设这些HOC与腐殖质物质相比非极性SBAC更强烈地结合。事实上,我们之前的研究表明,当SBAC上吸附位点的竞争成为一个因素时,疏水性在吸附过程中起着重要作用:SBAC比较低的log K ow(Björklund和李2017)。尽管SBAC可能有利于HOC的吸附,但丰富的腐殖质是强有力的竞争对手。然而,有机污染物的吸附可能发生在SBAC和SOM上,如批量测试所示。在列的有机污染物的另一种可能途径是结合腐殖物质吸附到SBAC表面,从而变得固定化(Wen等人。2013)。然而,这一假设尚未在当前的研究中进行过测试。
如所预期的,最高的浓度和肝卵圆细胞的最高负荷土壤层在最接近所述柱入口被发现(图(图3a3 a和b,分别地)。该浓度HOC显示很强的相关性为化合物登录ķ 流在入口和中间层(斯皮尔曼的ρ = 0.786和0.857,分别地),但仅中度相关在出口层(ρ = 0.536)。每个HOC的总负荷的大约40-70%被捕获在土壤的前17mm中,而在最靠近出口的层中发现5-27%的负荷。与大多数疏水化合物相比,疏水性较低的化合物在土壤中的迁移程度较高:在所有HOCs中,芴在最靠近出口的层中表现出最高负荷部分(27%),其次是DBP和蒽(20%) ),而芘在出口层中表现出最低部分(5%)。这一趋势解释了为什么出口层中的HOC浓度仅与log K ow中度相关。这些结果与DiBlasi等人在雨园中对PAHs进行的实地研究相比较。(2008年):大多数PAH保留似乎通过吸附和颗粒捕获在表层土壤层中发生。值得注意的是,当DiBlasi等人的雨水花园运行不到3年时。(2008)进行了他们的研究。同样,Dierkes和Geiger(1999)发现PAH浓度通常在路边土壤的上部10厘米中最高。但是,在某些地方,PAH浓度没有随着土壤深度(≤30cm)而降低。Murakami等人。(2008年用人工雨水进行了柱渗透研究,发现当土层厚度从20厘米增加到50厘米时,PAH去除效率从17%增加到56%,表明PAHs大量垂直迁移。此外,Strömvall等人。(2006年)在道路采样土壤中检测到浓度升高的半挥发性有机化合物和多环芳烃浓度分别达到1.0和1.5米。作者提出,土壤中这种意外的有机污染物垂直迁移可能是由于胶体促进的运输。在目前的研究中,技术腐殖酸形式的DOC与HOCs一起被添加到合成雨水中。在施用于土壤柱之前,HA和HOC之间的接触时间在0到12小时之间(每天两次制备成批的雨水)。这可能是小于所需的溶解肝卵圆细胞的时间与HA胶体平衡,以形成复合物的(van德Kreeke等人2010)。假设接触时间太短而不能形成与天然雨水相同程度的HA-HOC胶体(Brown 2002 ; Kalmykova等人,2013),在该列中低估了胶体促进的HOC 运输,即迁移。试验。目前的研究(图(图3),3),与来自Strömvall等人的结果一起。(2006)和Murakami等人。(2008年),表明HOCs通过中床(通常0.5米)的迁移可能发生在生物滞留或雨园的整个生命周期中。此外,对于溶解较少的疏水性有机污染物或附着在胶体上的HOC,可以预期更大的迁移,因为它们不会被土壤颗粒吸附或物理保留。
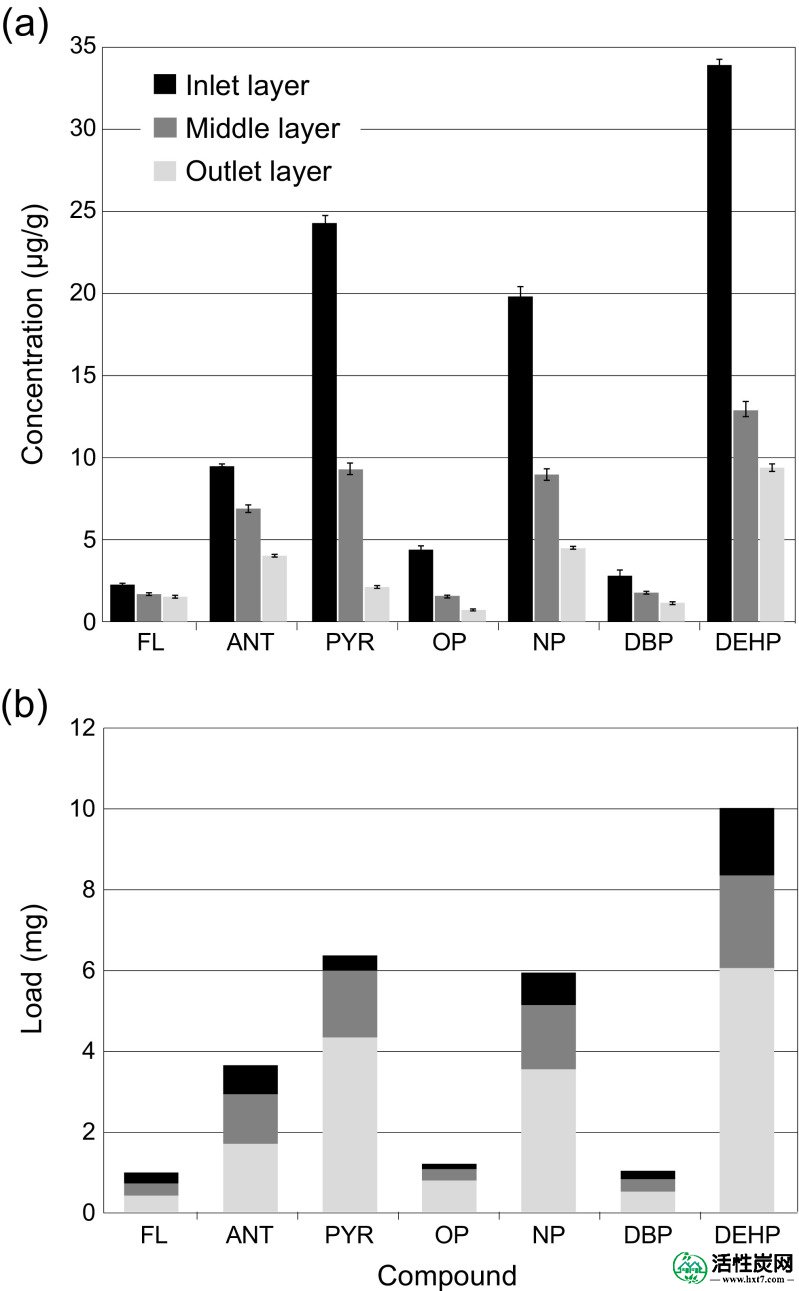
a三个分离的土壤层中的HOC 的浓度(μg/ g)和b载荷(mg)(入口层0-17mm;中间层18-34mm;和出口层35-51mm)。误差条表示每层中平均浓度的标准误差(在一式三份样品上测定)
既辛基苯酚和DBP在污染土壤表现出较低的负荷比从它们各自的日志预期ķ 流量值(图(图3b)。3 b)中。取决于各种物理 - 化学和空间特征,化合物基团(PAH,酚和邻苯二甲酸酯)可能以不同的强度吸附到SOM。但是,每组中的化合物太少,无法就此问题得出任何结论。各化合物的总负载土壤是负的平均浓度在列的流出水(斯皮尔曼相关ρ = -0.600至-0.771),条件是DEHP流出物的浓度被忽略。
肝卵圆细胞的质量吸附到土壤只占10〜50%的计算的理论最大质量的,米 广告(等式2),可被吸附到基于所述内容SOM(表土壤(表2)。2)。这表明在柱实验中土壤没有被HOC饱和,因此可以进一步吸附。此外,Ç / c ^ 0 = 1没有达到任何肝卵圆细胞(图的(图1,1,图S2),加强这一假说。理论剩余吸附能力(表(表2)2 )没有遵循疏水性或土壤中实际吸附质量的强烈趋势,这意味着吸附不能简单地通过SOM含量或化合物疏水性来解释。
土壤的实验测定和理论吸附能力; 在过滤和离心后测定污染土壤(所有三层)中HOC的解吸
| 实验确定与理论吸附 | 解吸 | ||||||
|---|---|---|---|---|---|---|---|
| 总吸附质量(mg)a | 理论最大吸附质量,m ads(mg) | 剩余理论吸附量(%) | 解吸质量(μg),在过滤的样品上测定 | 解吸百分比(吸附总质量的百分比) | 解吸质量(μg),在离心样品上测定 | 解吸百分比(吸附总质量的百分比) | |
| 芴 | 0.974 | 4.24 | 77 | 45.7 | 4.7 | 62.7 | 6.4 |
| 蒽 | 3.63 | 7.28 | 50 | 49.7 | 1.4 | 91.6 | 2.5 |
| 芘 | 6.35 | 17.2 | 63 | 74.9 | 1.2 | 222 | 3.5 |
| 辛基酚 | 1.19 | 10.3 | 88 | 50.2 | 4.2 | 89.3 | 7.5 |
| 壬基酚 | 5.92 | 19.0 | 69 | 112 | 1.9 | 246 | 4.2 |
| DBP | 1.02 | 2.10 | 52 | 20.8 | 2.0 | 35.0 | 3.4 |
| DEHP | 9.99 | 99.5 | 90 | 181 | 1.8 | 628 | 6.3 |
一个从图数据。图33 b
肝卵圆细胞的脱附负载,按照ISO / TS 21268-2标准方法,进行了比较在受污染的土壤柱的肝卵圆细胞总负荷,以确定脱附的(表的百分比(表2)。2)。一般而言,与土壤中有机污染物的许多其他解吸研究相比,HOCs的解吸百分比较低(1.2-4.7%),并且HOC对土壤的吸附不能被认为是可逆的(Delle Site 2001 ; OECD 2000)。解吸的负载(微克)是相关的,以在土壤肝卵圆细胞的总负载(皮尔森- [R = 0.702),即可用于解吸肝卵圆细胞的初始质量,并为化合物登录ķ 流(斯皮尔曼的ρ = 0.631)。
在当前的研究中,将解吸部分离心,然后过滤(1.5μm孔径),然后进行提取和分析(根据ISO / TS 21268-2)。为了比较,还分析了离心样品(未过滤的)的HOC浓度。离心(2000× g,10分钟)导致可沉降固体的分离。对于过滤和离心的样品,TOC(总有机碳)浓度分别为14.0和50.9mg / L. 在日志中的差ķ DES为离心,过滤样品之间肝卵圆细胞在图中示出图4。4。ķ 德 -值对DEHP低得多(即多个移动),比从化合物的日志预计ķ 流 ,特别是在离心样品中。通常,解吸HOC负载离心的样品中分别为27%(芴)至71%(DEHP)高于过滤样品中(表(表2):2):这意味着该最疏水的肝卵圆细胞的大部分被吸附颗粒>1.5μm(过滤器孔径)。Brown(2002)研究了PAHs在雨水颗粒,胶体和真正溶解相中的分配,并得出结论,与PAHs 的log K ow所预期的相反,胶体相的重要性因疏水性更强而降低化合物(log K ow > 4.5)因为颗粒相中的有机碳是更好的吸附剂。基于这一原理,我们认为DEHP和其他高疏水性HOC主要吸附在颗粒中的有机物质上,对于胶体的吸附对疏水性较低的HOC更为重要。这些结果表明,颗粒和/或胶体分离的截止值极大地影响了解吸试验的结果。
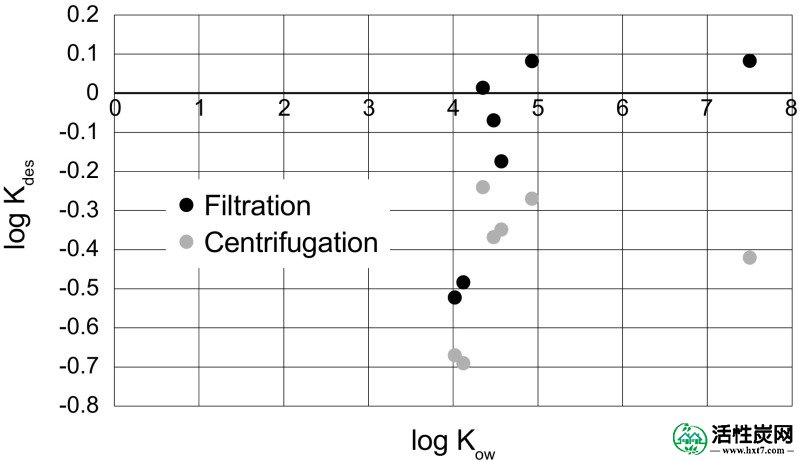
解析系数的对数log K des与所研究的七种有机化合物的疏水性log K ow有关。显示过滤(1.5μm孔径)和离心(2000× g,10分钟)洗脱液的关系
所述至少疏水性化合物芴和辛基酚表现出最低ķ DES(图(图4),4),即,在土壤中的大多数移动的化合物。这些数据支持先前提出的假设(参见“在柱测试中去除HOC”部分),疏水性较低的HOC对SOM的吸附较弱。因此,SBAC在色谱柱测试中对这些化合物的去除起着更大的作用。
生物滞留和雨园中有机污染物的主要去除过程,吸附和生物降解主要分别在潮湿和较长干旱时期进行(LeFevre等,2014 ; Murakami等,2008)。张等人。(2014年)表明干燥期需要超过至少10小时才能发生生物降解,而对于降解率低的化合物,可能需要数天到数周才能降解。因此,在连续流动柱中,促进了吸附,并且预期很少或没有生物降解。解吸数据表明,肝卵圆细胞被牢固地结合到SOM(表(表2),2),导致生物利用度低,因此生物降解的机会有限(LeFevre等人,2012b)。HOC的低解吸还导致吸附位点的再生有限以及其他污染物找到可用吸附位点的机会。
在种植的生物滞留和雨水花园中,从植物中释放的根系分泌物可能在从土壤中解吸HOCs中起作用。根分泌物含有的物质如有机酸,酚类化合物,多糖,和腐殖酸的化合物,其是公知的,以增加肝卵圆细胞的脱附等(Gao等人。2010 ;利费夫等人2013)。研究表明,植物根系分泌物可以有效地改变和增强PAHs萘,芘和菲从土壤中的解吸附,尽管不知道改变背后的机制是什么。然而,正如Grebel等人所强调的那样。(2013年),植物根系分泌物的相关性,以及相关的增强解吸和生物利用度与雨水污染物和条件的相关性尚不清楚。
例如,芴用于估算可添加到改良土壤中的SBAC的补充吸附能力(参见“使用SBAC评估增强污染物去除”部分)。通过添加0.5%(w / w)SBAC至1m 2生物滞留(0.5m 3土壤),除了通过土壤除去的负荷之外,可以除去几乎1g的芴。在模拟区域(萨里,BC,加拿大),假定生物截留的每平方米每年接收110和1200米3径流在交通和住宅区分别。假定此径流携带110毫克(流量)和60mg(住宅)芴至1m 2生物截留的。给定这些载荷,0.5%(w / w)SBAC对1 m 2(0.5 m 3)生物滞留的修正可以吸收与17年(住宅)和9年(交通)径流量的累积芴负荷一样多的芴。
在柱研究中使用的合成雨水是一种比天然雨水复杂得多的解决方案,天然雨水含有广泛的有机污染物; 油和油脂; Zn,Pb,Cu,Ni和Cd等金属; 营养成分; 有机和无机胶体; 和溶解的化合物,以及颗粒。预计颗粒及其结合的污染物将被困在生物滞留和雨园介质的最顶层(DiBlasi等人,2008 ; LeFevre等人,2014 ; Murakami等人,2008))。然而,许多溶解的污染物竞争SBAC上的吸附位点并导致介质饱和。这表明柱研究是“最佳情况”,对吸附位点的竞争较小,并且预计天然雨水的SBAC饱和时间会缩短。尽管基于SBAC增加的补充吸附能力的简化计算,结果表明SBAC可能在媒体饱和发生之前延长生物滞留或雨园的寿命,可能延长约10 - 20年。
批量吸附研究表明,SBAC对所选疏水性有机化合物的吸附能力显着高于土壤有机质:吸附SBAC的HOC质量比SOM高约5至8倍。假设这种差异取决于疏水性吸附位点的丰度,除了高表面积和SBAC的大微孔性之外。然而,柱试验表明,SBAC修正的土壤比非常疏水的化合物更有效地去除中等疏水性化合物,例如芴,辛基酚和蒽。解吸试验表明,HOC通常强烈地吸附在土壤颗粒上; 疏水性越高,对SOM的吸附越强。此外,更疏水的化合物对>1.5μm的颗粒表现出更强的吸附作用,而疏水性较低的化合物似乎附着在小颗粒和胶体上。这些结果都表明,疏水性较低的HOCs对SOM的吸附较弱,即通过土壤床迁移的风险较高,SBAC在柱试验中对这些化合物的去除起着较大的作用。添加量低至0.5%(w / w)SBAC可以在疏水性较低的化合物发生饱和之前将生物滞留介质的寿命延长大约10 - 20年。然而,HOC与有机胶体竞争SBAC吸附位点。柱测试显示,大部分释放的SOM被SBAC吸附,这可能导致SBAC吸附位点的早期饱和。此外,雨水中存在的有机胶体可能吸附HOC并促进其通过土壤床的运输。
未来的研究应该集中在HOCs通过中床的迁移,因为它决定了HOC浸出变得不可接受之前生物滞留和雨水花园的寿命。尽管在土壤床的第一(上)厘米中发现了最高的HOC浓度和负荷,但由于操作系统中污染物 - 土壤接触不良以及HOC通过胶体促进的运输,不能排除污染物通过床的迁移。土壤,被认为在天然雨水中具有重要意义,其中有机胶体和化合物有足够的时间来平衡和形成复合物。