发布日期:2018-11-13 09:45 来源:活性炭网 作者:活性炭网 浏览数:
从不同来源获得的商业活性炭(AC)样品:Norit E Supra USP,Norit B Test EUR和ML(Baracoa,Cuba)进行了研究。 对乙酰氨基酚的吸附,C o = 2500 mg / L,在pH 1.2的模拟胃液(SGF)中与活性炭接触,
活性炭(AC)可以作为解毒剂口服应用于不同的中毒。几项研究,无论是在体外和体内都表现出活性炭吸附大量的有毒化合物(Neuvonen&Olkkola容量1989 ; Alaspaa等人2000 ; Ho等人1989 ;池塘1986 ; McGoodwin&谢弗2000 ; Cooper等人。2005 ; Hoegberg等2003 ;莫迪等人1994年 ; Hoegberg等2002 ;埃尔- Kemary等人。2011)。所述1-15acetaminophen(N-乙酰基- 对-氨基苯酚)是一种具有镇痛作用的药物,没有临床上显着的抗炎特性。它通过抑制前列腺素合成起作用,细胞介质负责疼痛的发作。它还具有解热作用。它通常以胶囊,片剂,栓剂和滴剂的形式提供,用于口服给药。它是各种抗感冒和流感产品的常见成分。
其低廉的价格和广泛的可用性导致经常过量的病例。在指定剂量下,对乙酰氨基酚对胃粘膜,血液凝固或肾脏没有影响,但肝脏可能受到严重影响。
AC的吸附能力取决于吸附剂的性质(孔结构,官能团,灰分含量)以及吸附物的性质(官能团,极性,分子大小和重量)。前体的类型和活化过程决定了AC的基本性质,例如表面积和孔径分布。AC具有强烈的异质表面,具有几何和化学特性。几何异质性是孔隙的大小和形状以及凹坑和空位的差异的结果。化学异质性与表面上的不同官能团(主要是氧)和各种表面污染物有关。两种异质性都有助于活性炭的独特吸附性能(Neuvonen&Olkkola 1989 ; Alaspaa et al。2000年 ; Ho等人。1989年 ; 池塘1986 ; McGoodwin&Schaeffer 2000 ; Cooper等。2005年 ; Hoegberg等。2003年 ; 莫迪等人。1994年 ; Hoegberg等。2002年 ; El-Kemary等。2011年 ; 美国临床毒理学会(AACT); 欧洲毒物中心和临床毒理学家协会(EAPCCT)1999 ; 布莱恩特等人。2003年 ; Neuvonen等。1984年 ; Neuvonen 1982 ; Neuvonen&Olkkola 1984 ; Yamamoto等人。2007年)。本研究的目的是研究AC去除溶解于模拟胃液(SGF)中的对乙酰氨基酚的功效。
对乙酰氨基酚(> 99%)购自Sigma-Aldrich。它是 具有芳族羟基的弱酸(pK a = 9.5),并且在20℃下在水中的溶解度为1.4g / 100mL。美国食品和药物管理局(FDA)建议在酸性水溶液中使用分光光度法UV,λmax = 245nm,作为其定量的参考方法。UV-可见光谱如图1所示 (El-Kemary等人2011 ; Gyamlani&Parikh 2002)。
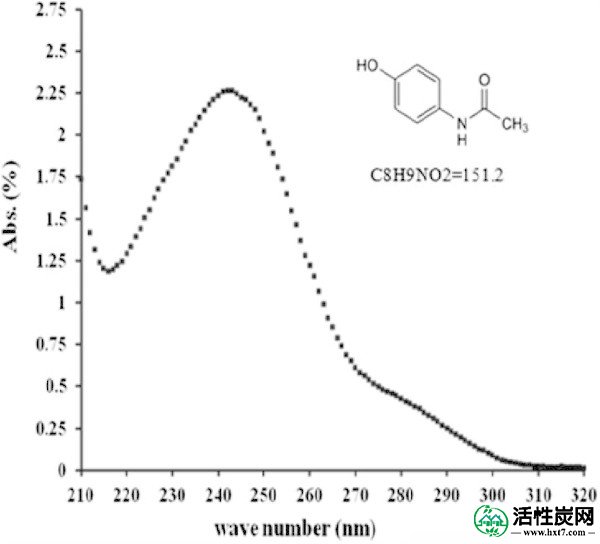
紫外 - 可见光谱的对乙酰氨基酚在SGF pH 1.2。
诺芮特B(NB)测试EUR(德国)和Norit E(NE)Supra USP(荷兰)作为参考。活性炭ML由Baracoa活性炭工厂(古巴)提供,并通过酸/碱处理(Rey-Mafull等人2007 ; Rey-Mafull等人2010)进行纯化。粒径对应于100%<250μm。所有碳原子按照标准的要求,按照美国药典(USP30-NF25,actived木炭2007年)。
根据USP 30如下制备SGF:将2g NaCl溶解在7mL浓HCl中,并用不含CO 2的蒸馏水填充至1L ,同时将溶液的pH调节至1.2。将对乙酰氨基酚加入到SGF溶液中,达到2500mg / L的浓度。使用UV / VIS分光光度计(来自Amersham Biosciences的Ultrospec 2100 pro)进行SGF中对乙酰氨基酚的校准曲线。 在Lambert Beer透射率区域中,在λmax = 245nm处的最大吸光度确定所有样品的光密度。使用线性或二次回归分析调整校准曲线。每个实验一式三份进行。
通过将对乙酰氨基酚溶解于1L重新调节至pH 1.2的SGF中,制备浓度为2500mg / L的对乙酰氨基酚的储备溶液。分析重复三次,并对每种类型的AC进行平均15次实验运行。对AC样品进行粒度分布分析。在吸附期间,碳的量在0.001至0.27g的范围内变化。将AC样品加入溶解在SFG中的对乙酰氨基酚溶液中,并在室温(37.0±0.1℃)下以100rpm恒定搅拌4小时。然后过滤样品,取5ml溶液提取物进行UV / VIS分析。通过质量平衡计算活性炭吸附的对乙酰氨基酚的量。先前建立的线性Beer-Lambert关系用于浓度分析。对于具有较高浓度的溶液,需要稀释以在Beer-Lambert区域中进行分析。从校准曲线中获取吸光度读数,该曲线确定对应于等温线的每个点的平衡浓度。平衡时的吸附量,q e(mg / g),通过方程式计算。 1。
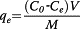
其中C 0(mg / mL)是初始浓度(t = 0),C e(mg / mL)是平衡浓度(t = 4 h),M是碳的质量(g),V是体积解决方案(L)。
通过使用在273K(来自Micromeritics的ASAP 2050 V1.00 E System)测量的CO 2吸附等温线来表征碳的微孔率。在实验之前,将样品在240℃下脱气24小时。吸附等温线参数,通过应用杜比宁-Radushkevich(DR)方程式计算(公式 2)(斯米谢克&Cerny的1970 ;布拉德利和兰德1995年 ; McEnaney 1987 ; Stoeckli 1998 ;杜比宁&Stoeckli 1980 ; Stoeckli等人2001):
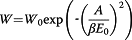
其中W(cm 3 / g)表示在温度T(K)下填充的体积,β是相似系数,E 0(kJ / mol)特征能量,W 0(cm 3 / g)是最大吸附容量。与微孔体积有关,A是差分摩尔功或吉布斯自由能ΔG的变化,由等式1定义。 3
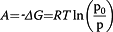
其中P 0 / P相对压力,R是理想气体常数(0.00831 kJ / mol K),T是温度(K)。通过以下表达式(等式4)计算微孔的体积 :
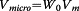
其中V m表示在273K下的CO 2摩尔体积。当孔径在0.45-2.5nm之间时,所谓的特征能量E 0与平均微孔宽度W m(nm)有关,通过以下表达式(公式 5)(Stoeckli 1998 ;杜比宁&Stoeckli 1980 ; Stoeckli等人2001)。
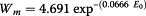
平均回转半径R g(nm)通过使用Dubinin-Steockli关系(等式 6)确定:
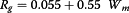
平衡等温线表示在恒定温度下以平衡单位质量的吸附剂从溶液中除去的吸附物的量之间的关系。在该研究中,对乙酰氨基酚吸附的平衡数据通过替代的双参数等温线处理,包括:Langmuir(TI和TII),Freundlich,Dubinin-Radushkevich(DR)和Temkin。这些等温方程的线性表达式和获得等温线参数的方法在表1中给出 。最小二乘法用于获得趋势线。特征参数由相应的线性形式确定(Quesada等人2009 ;Passé等人2009 ; Behnamfard和Salarirad 2009 ; Richard等人2009; 辛等人。2011年 ; Ahmad&Rahman 2011)。
等温线及其线性化表达式
| 等温线 | 表达式 | 线性表达式 | 地块 |
|---|---|---|---|
| 朗缪尔 |
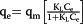 |
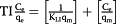 |
 |
| ΔG= - RTln [K L ] |
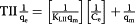 |
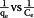 |
|
| 符合Freundlich |
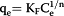 |
lnq e = lnK F + n - 1 lnC e | lnq e vslnC e |
| Dubinin-Radushkevih(DR ) |
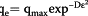 |
LNQ Ë = LNQ 最大值 - Dε 2 | LNQ ë VS ε 2 |
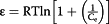 |
|||
| E 0 = [2D] - 0.5 | |||
| 特姆金 |
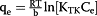 |
q e = BlnK TK + BlnC e | q e vslnC e |
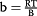 |
使用含有0.1wt%碳的KBr粒料,在FTIR分光光度计(Nicolet 50X)上记录不同活性炭样品(4000-400cm -1)的FTIR光谱。将这些粒料在100℃下干燥8小时,然后记录光谱。
将DR模型应用于CO 2等温线获得的结果总结在表 2中。对于DR等温线获得的R 2高于0.98。活化的碳NE和ML呈现非常相似的微孔性。
通过 在273K吸附CO 2 进行纹理表征
| 吸附剂 | W0(cm3 / g) | E0(kJ / mol) | Rg(nm) | Wm(nm) | Vmicro(cm3 / g) | R 2 |
|---|---|---|---|---|---|---|
| 诺芮特E Supra USP(NE) | 5.64 | 6.17 | 1.61 | 3.11 | 0.31 | 0.98 |
| 诺芮特B测试EUR(NB) | 14.15 | 8.28 | 1.37 | 2.64 | 0.68 | 0.99 |
| 古巴巴拉科阿(ML) | 5.65 | 7.87 | 1.44 | 2.78 | 0.39 | 0.99 |
鉴定了三种活性炭(3424,2852,2921和1125cm -1)的共同条带,图 2。3424cm -1的带用于羰基-OH拉伸。2852和2921cm -1处的峰是由于脂族CH,CH 2和CH 3基团的存在,并且预期在1125cm -1处的峰与羧基-OH基团有关。样品NB显示1737 cm -1的带,可以指定为内酯基,而样品NE则在1710 cm -1处观察到峰。其可以指定为内酯或非芳族羧基,据报道C = O拉伸发生在1712cm -1处。从1600到1650 cm -1的波段可以分配到C = O quinonics组。在这些范围中发现以下频段:1652厘米-1为NE,1629厘米-1为NB / NE,和1641厘米-1为ML。NB / NE常见的1578 cm -1频带尚未明确解释。这已被指定为高度共轭的羰基的芳环拉伸对。2900cm -1处的峰对应于以下官能团:CH,-CH 2,-CH 3。此外,波数1400和1700cm -1之间的一系列中等强度的峰可归因于由于酮,酯,醛和羧酸的存在,官能团C = O和C = C的伸长。在1038cm -1处, NE呈现出对应于酒精CO振动拉伸的峰值(Moreno等人2000 ; Moreno 2004 ; Pradhan&Sandle 1999 ; Terzyk等人2003 ; Terzyk 2002 ; Liu等人2009 ; Liu等人。2010)。
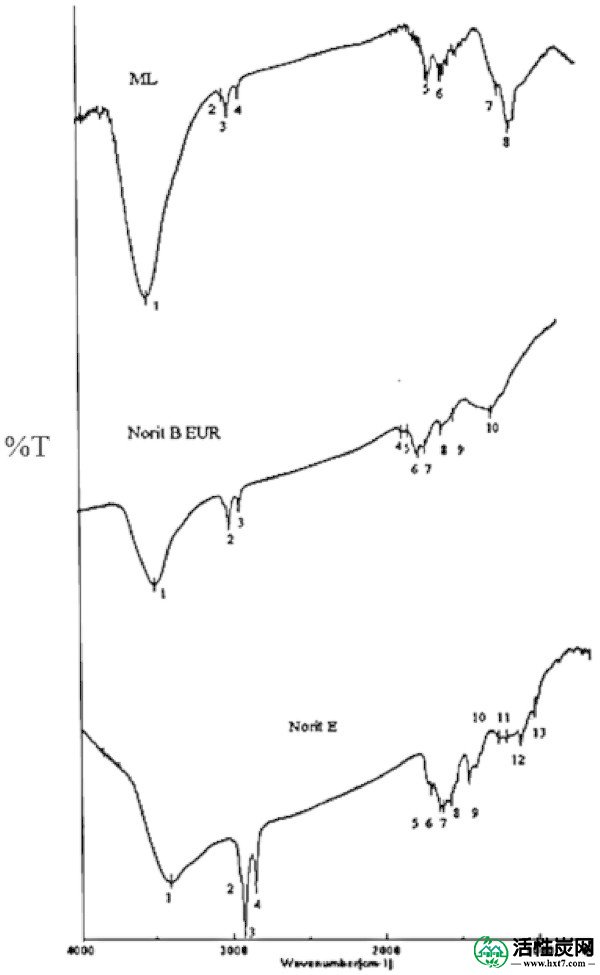
活性炭的FTIR光谱。
对乙酰氨基酚在37℃下对NE,NB和ML活性炭的实验吸附数据绘制在图 3中。等温线表明,NB具有最高吸附容量和最高V MICO(厘米3 /克),但是有微孔和吸附能力之间不存在线性关系,因为ML以较低的呈现类似的值Vmicro(表 2,, 33和AND4)。4)。该结果表明碳的吸附能力与其质地性质之间不存在简单的关系。(Moreno等人2000 ; Moreno2004),已经表明碳的表面化学必须被认为是稀释水溶液中吸附机理的重要因素。
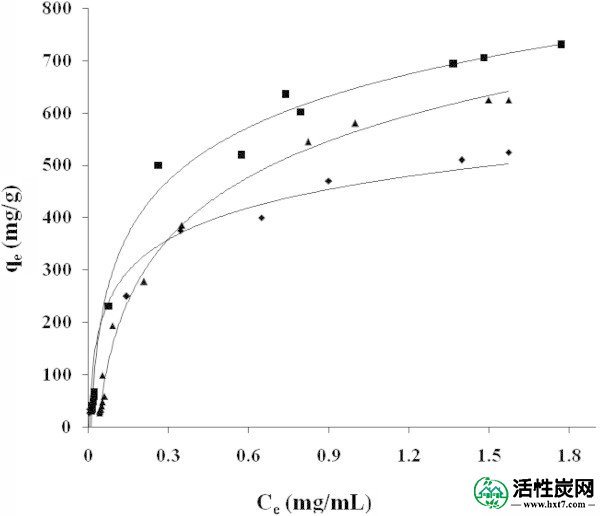
对乙酰氨基酚在SGF,NB(■)NE(◆)ML(▲)中吸附等温线的实验数据。
模型的特征参数
| 活性炭 | 朗缪尔 | 符合Freundlich | 杜比宁-Radushkevich | 特姆金 | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| TI | TII | |||||||||
| 参数 | R 2 | 参数 | R 2 | 参数 | R 2 | 参数 | R 2 | 参数 | R 2 | |
| q m = 840 | 0.99 | q m = 1315.8 | 0.99 | K F = 685 | 0.96 | q max = 685 | 0.99 | b = 17.5 | 0.99 | |
| NB | K LI = 3.6 | K LII = 2 | n = 1.6 | D = 0.018 | K TK = 82 | |||||
| q m = 555 | 0.99 | q m = 356 | 0.89 | K F = 503 | 0.98 | q max = 458 | 0.98 | b = 29.6 | 0.98 | |
| NE | K LI = 6 | K LII = 19 | n = 1.9 | D = 0.016 | K TK = 202 | |||||
| q m = 769 | 0.99 | q m = 1462 | 0.95 | K F = 605 | 0.88 | q max = 632 | 0.96 | b = 7.2 | 0.99 | |
| ML | K LI = 3.3 | K LII = 1 | n = 1.7 | D = 0.04 | K TK = 27 | |||||
由Langmuir和Temkin方程计算的自由能变化吉布斯(ΔG) 和 由Dubinin Radushkevich方程计算的特征能量(E)
| 参数 | 楷模 | NE | NB | ML |
|---|---|---|---|---|
| ΔG(kJ / mol) | 朗缪尔(TI) | - 4.6 | - 3.3 | - 3.25 |
| ΔG(kJ / mol) | 特姆金 | -13.7 | -11.4 | -8.5 |
| E(kJ / mol) | 杜比宁-Radushkevich | 五 | 五 | 4.8 |
为了阐明许多分子在不同吸附剂上的吸附机理,已经进行了大量工作(Passé等人2009 ; Behnamfard&Salarirad 2009 ; Richard等人2009 ; Xin等人2011 ; Ahmad&Rahman 2011 ; Moreno et人2000 ;莫雷诺2004年,普拉丹和八婆1999年 ; Terzyk等。2003)。这些出版物揭示了在碳基材料上从稀水溶液中吸附有机分子是静电力和非静电力之间的复杂相互作用。此外,两种相互作用取决于吸附剂和吸附物的特性,以及溶液的化学性质。观察到吸附容量受碱性表面基团的存在的负面影响。Terzyk等人。2003年报道,随着AC表面碱性基团和羰基化合物总量的增加,对乙酰氨基酚的最大吸附能力下降。据推测,对乙酰氨基酚分子通过OH相互作用-具有碳基本表面的基团,并且排斥效应发生在该分子的CO基团和附着于表面的类似基团之间(Yamamoto等人2007 ; Terzyk等人2003 ; Terzyk 2002)。
通过相关系数R 2评估等温线方程描述吸附过程的适用性。如图从图获得等温线的五个不同的线性化形式的相对参数 4,,5,5,6,6,77和AND88和表 3至TO4。4。吸附等温线模型按以下顺序拟合数据:LTI = LTII = T> F = DR(NB),LTI> F> T = DR(NE)和T> LTI> DR(ML)。
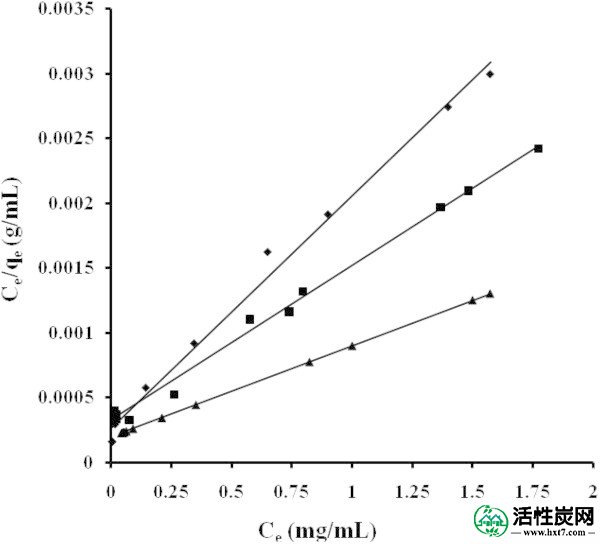
在Langmuir的TI坐标NB(■)NE(◆)ML(▲)中调整吸附等温线。
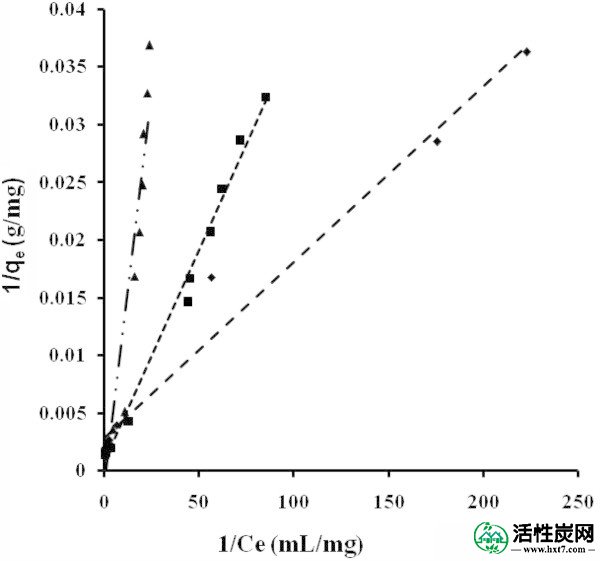
在Langmuir的TII坐标NB(■)NE(◆)ML(▲)中调节吸附等温线。
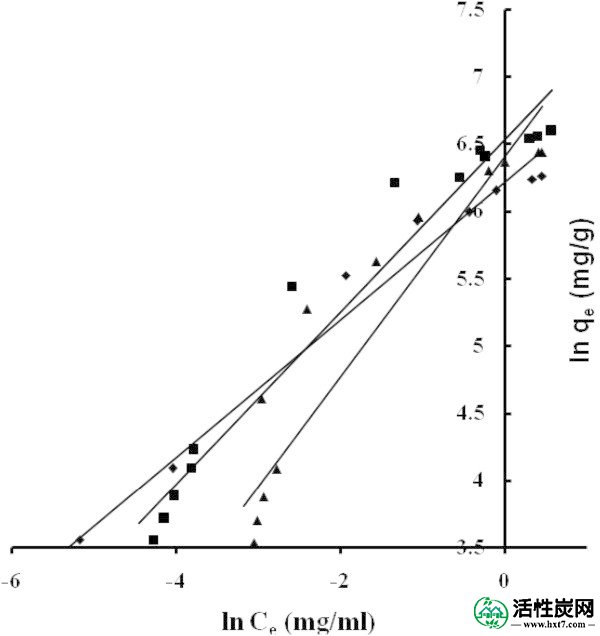
在Freundlich坐标NB(■)NE(◆)ML(▲)中调节吸附等温线。
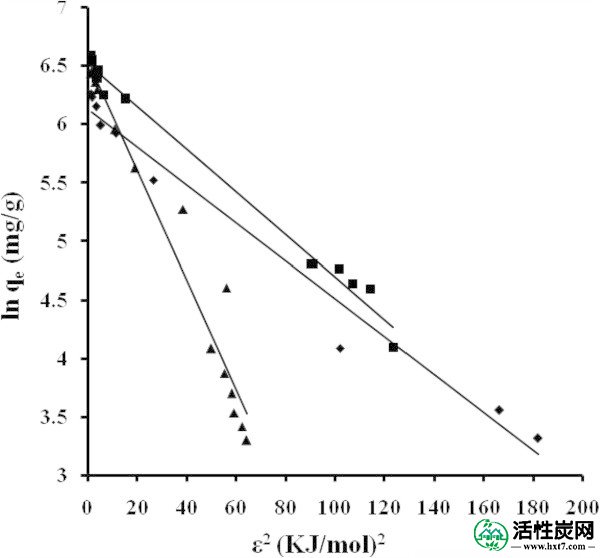
在 Dubinin-Radushkevich 坐标NB(■)NE(◆)ML(▲)中调节吸附等温线。
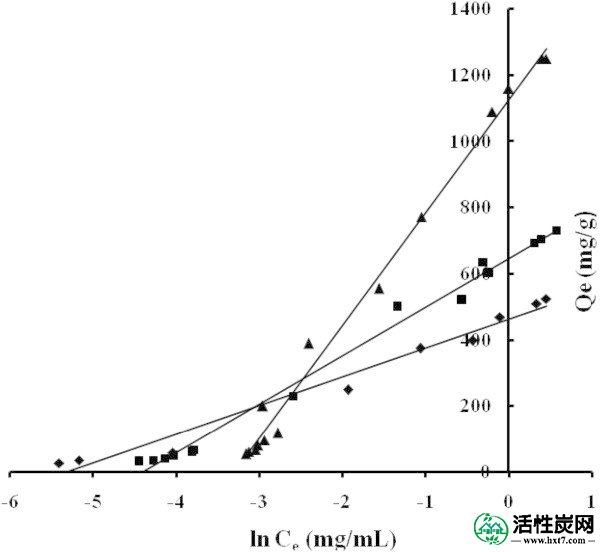
吸附等温线在Temkin坐标NB(■)NE(◆)ML(▲)中调整。
Langmuir吸附模型描述了吸附物单层吸附到均匀吸附剂表面上。此外,吸附分子与具有均匀能量的吸附位点之间的相互作用可忽略不计。Langmuir等温线通过平衡吸收和释放的相对速率来解释表面覆盖,前者与表面的分数成比例是开放的,而后者与覆盖的分数成比例。这些速率的平衡常数是K(L / mg),这也对应于亨利定律系数。当流体浓度非常高时,在吸附剂表面上形成单层,具有q max的载荷。(毫克/克)。
Langmuir方程的本质特征可以用无量纲分离因子Eq表示。 7。
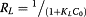
术语R L表示等温线的形状如下。当参数R L > 1(不利的等温线)时,R L = 1(线性等温线),0 < R L <1(有利的等温线)。在所有情况下,R L(3.99×10 -4)表示等温线具有良好的行为。
Dubinin-Radushkevich方程:假设对应于任何吸附质浓度的吸附量是Polanyi势的高斯函数。该理论的发展基于特征曲线和Polanyi吸附势的概念(∂E/∂T= 0用于描述微孔中的吸附。LN的线性图q ë针对ε 2(千焦/摩尔)2将给出的值q 最大值(毫克/克)和d(摩尔2千焦-2),从截距和斜率。的计算值ê(千焦/摩尔)被示出在表 3至TO44。
根据Langmuir和DR方程,估计了系统的自发性和吸附过程中涉及的能量。计算了与该系统相关的其他值,并报告了Terzyk(2002),作为浸没焓(16,11,8和6kJ / mol)。物理和化学吸附的ΔH值的大小分别在2.1至20.9和80至200kJ / mol的范围内。通常,对于物理和化学吸附,ΔG在0至-20kJ / mol和-80至-400kJ / mol的范围内(Liu等人,2009 ; Liu等人,2010 ; Li等人,2005)。由DR方程获得的对乙酰氨基酚的对乙酰氨基酚的特征曲线,图 9,表明先前预测的环境中的能量值。在覆盖度降低到0.1的程度上,能量值可以在7.5到12.5kJ / mol之间找到。它们达到涂层的平均值5kJ / mol q e/ q max = 0.4至0.5。
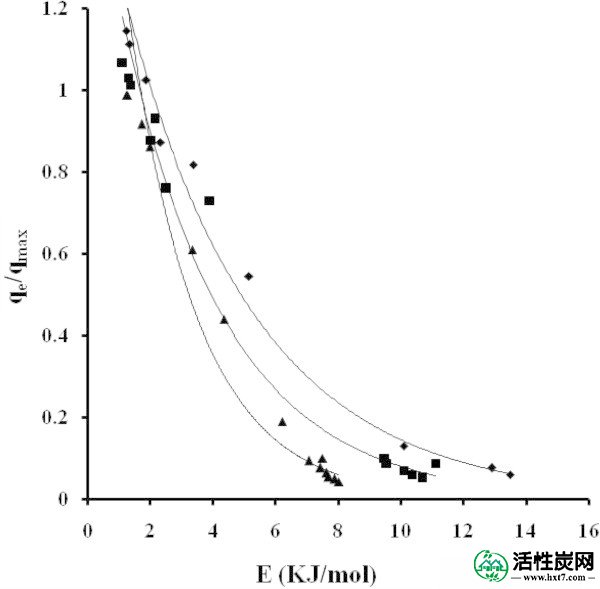
吸附溶于SGF的对乙酰氨基酚的特征曲线(pH 1.2,T = 310 K)NB(■)NE(◆)ML(▲)。
Terzyk等人。(2012)提出了对乙酰氨基酚的分子横截面积(MCSA)为60.2埃2。在表 5中,给出了通过Langmuir,DR和Freundlich方程估计的对乙酰氨基酚分子横截面积的值。为了计算对乙酰氨基酚的分子横截面面积(A 2)下列等式。 使用了8个:
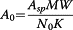
比表面积的对乙酰氨基酚分子取作基准的值60.2 A的值的估计的计算 2 提出 Terzyk等。(2012)
| 朗缪尔 | 杜比宁-Radushkevich | 符合Freundlich | ||||
|---|---|---|---|---|---|---|
| 吸附剂 | MCSA(2) | 相对误差(%) | MCSA(2) | 相对误差(%) | MCSA(2) | 相对误差(%) |
| NB | 42.7 | 20 | 55.5 | 7.8 | 52 | 14 |
| NE | 39.3 | 35 | 47.6 | 21 | 43.4 | 28 |
| ML | 23.5 | 62 | 28.3 | 50 | 29.8 | 50 |
其中A sp(m 2 / g)是活性炭的比表面积,由N 2蒸气吸附数据的BET分析得到,MW是对乙酰氨基酚的分子量,K是每克吸附的对乙酰氨基酚的摩尔数。吸附剂在最大表面覆盖率,N 0是Avogadro的数字(Wurster&Aburub 2006 ; Wurster等人2003)。
对乙酰氨基酚分子在活性炭表面上的压实程度的有效性与吸附位点在该分子的最大包装程度上的最佳分布有关。在SGF中以非离子化状态测定对乙酰氨基酚分子的面积在活性炭表面上显示出更好的取向,优先顺序为NB> NE> ML。原因可能是在纹理和功能平面上分别更好地分布吸附活性位点。但是,关于估计计算中的相对误差显示模型,顺序如下:Langmuir> Freundlich> DR。但在所有情况下,相对误差都大于10%。
Temkin模型考虑了一些间接吸附/吸附质相互作用对吸附等温线的影响。由于吸附剂/吸附物的相互作用,层中所有分子的吸附热随覆盖率线性降低。这是Langmuir方程的修正,并介绍了温度对吸附的影响。在这种情况下,b(J / mol)是与吸附热有关的Temkim常数,K TK是Temkin等温线常数(L / g)。吸附能B的变化量为正对所有研究的AC,表 3,这表明吸附反应是放热的(-ΔH 广告)(哈米德等人2008)。
经验Freundlich模型基于吸附剂在吸附剂的非均相固体表面上多层形成的假设,并假设首先占据较强的结合位点,并且结合强度随着位点占据的增加而降低。值Q max和1 / n分别是与吸附容量和吸附强度相关的Freundlich常数。1 / n [0 <(1 / n)<1] 的较低分数值表明弱吸附力对活性炭表面有效。n > 1的值表示有利的吸附条件,适用于高度不均匀的表面。在这项研究中,找到了值n在1.6和1.9之间,这证明吸附是有利的并且过程可以是物理性质的(Behnamfard&Salarirad 2009 ; Yan等人2008)。
该研究中报道的结果表明,可以设想活性炭ML作为从SGF中除去对乙酰氨基酚的替代吸附剂。ML与商业标准NB和NE没有显着差异。CO 2等温线表明ML是微孔材料,其纹理类似于NE图案。通过比较三种不同性质的活性炭,很明显微孔结构和表面化学在确定吸附容量方面起着关键作用。
确定对乙酰氨基酚在SGF中活性炭上的吸附过程是自发的(ΔG<0)。如大多数情况所见。根据活性炭的类型,模型非常适合分析的数据。对乙酰氨基酚的吸附可以发生在特定部位以及基部区域。虽然已经确定氧化过程是由氧表面基团进行的,但先前的结果表明,不仅这些氧基团的量和性质以及分布变得至关重要。对乙酰氨基酚分子横截面的区域的估计计算证明了该肯定。